
In Hongkong wird das Zulassungsverfahren für Orphan-Arzneimittel bei seltenen Krankheiten, insbesondere für solche, die neue chemische oder biologische Einheiten (NCEs) enthalten und für lebensbedrohliche oder schwerwiegend schwächende Krankheiten bestimmt sind, vom Pharmacy and Poisons Board of Hong Kong verwaltet. Im Folgenden finden Sie eine Schritt-für-Schritt-Anleitung, um den Prozess zu durchlaufen:
Schritt-für-Schritt-Anleitung zur Zulassung von Arzneimitteln für seltene Krankheiten
Vorbereitung und Einreichung
Bereiten Sie den Antrag einschließlich der wichtigsten Unterlagen vor:
- Gutachten von Experten und CTD-Dokumente zu Sicherheit, Wirksamkeit und Qualität
- Risikomanagementpläne (RMPs)
- Produktetiketten und Beipackzettel
- Berichte zur Risikobewertung von elementaren Verunreinigungen
- Weltrekord bei den Zulassungen
Reichen Sie Ihren Antrag auf Registrierung über das Pharmaceuticals Registration System 2.0 (PRS 2.0) auf der Webseite des Drug Office ein. Dies ist ein entscheidender erster Schritt für diejenigen, die Orphan-Arzneimittel für seltene Krankheiten in Hongkong registrieren.
Zahlung der Gebühren
Zahlen Sie die Antragsgebühr über:
- PRS 2.0 (online) – per Kreditkarte oder PPS
- Persönlich – mit Bargeld oder Scheck beim Drug Office
- Prüfung und Bewertung
- Das Drug Office prüft alle eingereichten Dokumente, bevor es den Antrag zur Bewertung annimmt.
- Sind die Dokumente unvollständig, wird ein Mängelschreiben ausgestellt.
- Refuse-to-File (RTF)-Mechanismus
- Ab dem 1. Juli 2024 stellt das RTF-Verfahren sicher, dass nur vollständige und ordnungsgemäß dokumentierte Anträge in die Bewertung gelangen. Den Antragstellern wird eine Frist von 60 Tagen eingeräumt, um etwaige Mängel zu beheben, die bei der ersten Prüfung festgestellt wurden.
- Unvollständige Anträge werden bereits in der Vorauswahlphase abgelehnt. Erfolgt innerhalb von 60 Tagen keine Antwort, führt dies zur automatischen Ablehnung des Antrags.
Verbesserte Verfahren für NCE-Produkte
Für NCE im Rahmen des„1+-Mechanismus“(für lebensbedrohliche oder schwer behindernde Krankheiten) hat der Ausschuss Verbesserungen gebilligt, die das Zulassungsverfahren vereinfachen und beschleunigen sollen – was insbesondere für Arzneimittel zur Behandlung seltener Krankheiten von Vorteil ist.
- Anforderungen nach der Zulassung
- Nach der Produktregistrierung:
- Einhaltung der Pharmakovigilanz-Anforderungen
- Meldung von schwerwiegenden unerwünschten Arzneimittelwirkungen (ADRs)
- Umsetzung und Pflege von Risikomanagementplänen
- Nach der Produktregistrierung:
Rechtsmittel
Wenn der Antragsteller eine Ausschussentscheidung beanstandet, kann er beim Berufungsgericht für Apotheken und Gifte Rechtsmittel einlegen.
Fristen
Das Gesundheitsministerium beabsichtigt, den Registrierungsprozess etwa 9 Monate nach Einreichung abzuschließen, vorausgesetzt, alle Dokumente sind vollständig. Dies trägt dazu bei, Medikamente für seltene Krankheiten effizient auf den Markt zu bringen.
Konsultation und Rückmeldung
Das Gremium kann während der Bewertungs- und Politikumsetzungsphasen Konsultationen mit Interessenvertretern und Branchenexperten durchführen.
Kontinuierliche Aktualisierungen
Bleiben Sie auf dem Laufenden, indem Sie regelmäßig folgende Seiten besuchen:
- Die offizielle Website des Gremiums
- Bekanntmachungen des Arzneimittelamtes
Flussdiagramm
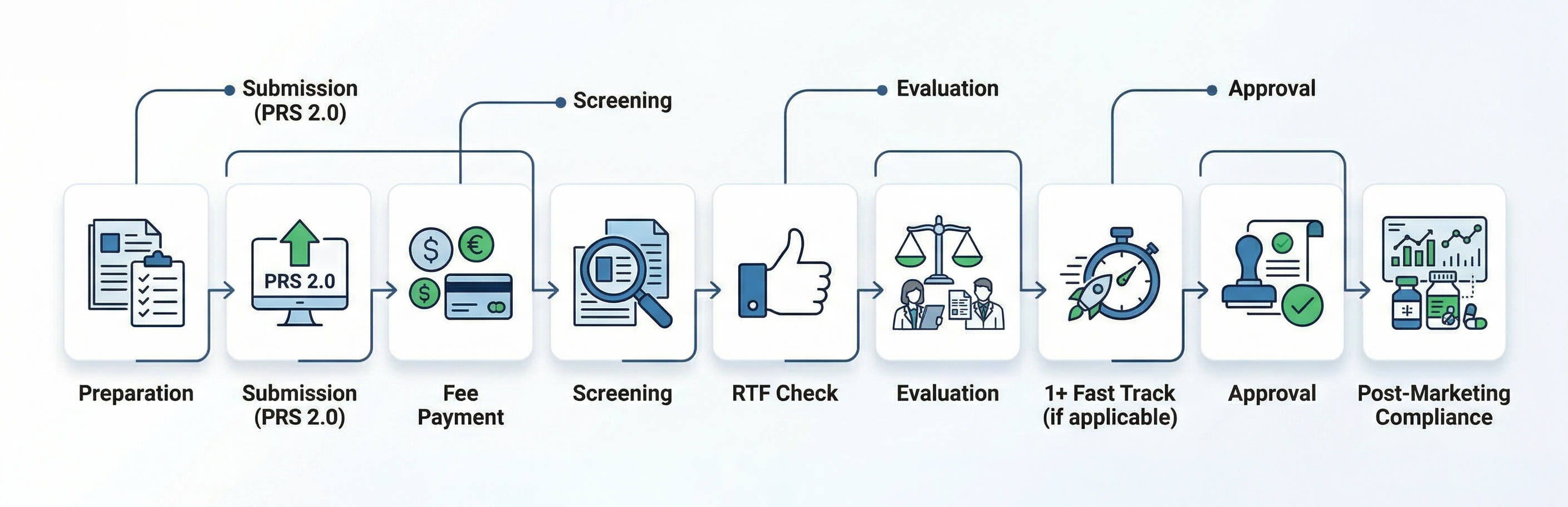
Wie Freyr helfen kann
Freyr bietet End-to-End-Unterstützung für die Registrierung von Orphan-Arzneimitteln in Hongkong, einschließlich der Dossiererstellung, der Navigation durch PRS 2.0 und der Einhaltung der Vorschriften nach der Zulassung. Mit lokaler Expertise und einem strategischen Ansatz tragen wir dazu bei, einen schnelleren, regelkonformen Markteintritt für Orphan-Arzneimittel gegen seltene Krankheiten zu gewährleisten.









