
Da die US Food and Drug Administration (USFDA) im Jahr 2024 die endgültige Regelung für die Vorschriften zum Qualitätsmanagementsystem (QMSR) implementiert, müssen Medizinproduktehersteller die Änderungen übernehmen, um ihre Produkte auf dem US-Markt zu vertreiben.
Diese Regel aktualisiert die Quality System Regulations (QSR) der USFDA, indem sie sich an die ISO 13485:2016 anpasst, dem internationalen Standard für Qualitätsmanagementsysteme (QMS) für Medizinprodukte. Hersteller von Medizinprodukten haben eine zweijährige Übergangsfrist zur Konformität, was es für Organisationen notwendig macht, die neuen Anforderungen anzupassen, um eine Nichteinhaltung zum Zeitpunkt der Inspektion zu vermeiden.
Was ist QMSR?
Die FDA QMSR ist ein optimierter Ansatz für QMS-Anforderungen, der eine Aktualisierung der früheren QSR-Struktur darstellt. Diese Angleichung ist entscheidend, da sie die globale Compliance für Hersteller, insbesondere solche, die weltweit tätig sind, vereinfacht. Diese Harmonisierung wird es Unternehmen ermöglichen, regulatorische Anforderungen sowohl in den US als auch in anderen Märkten auf eine wesentlich einheitlichere Weise zu erfüllen.
QMSR schreibt Verbesserungen in den Bereichen Risikomanagement, Geräteentwicklung und Post-Market Surveillance vor. Dies mag die Komplexität erhöhen, bietet den Herstellern aber auch die Möglichkeit, ihre Qualitätsprozesse zu standardisieren, was wiederum die Gerätesicherheit erhöht und zu einer besseren Dokumentation führt, die bei USFDA-Inspektionen entscheidend sein kann.
Wesentliche Änderungen im QMSR
- Harmonisierung mit ISO 13485: Dies ist der wichtigste Schritt, der es Herstellern von Medizinprodukten ermöglicht, international anerkannte Standards zu übernehmen. Die USFDA erkannte, dass viele Medizinprodukteunternehmen bereits der ISO 13485 entsprechen, was doppelte Anstrengungen reduziert.
- Der QMSR betont das Risikomanagement während des gesamten Lebenszyklus des Medizinprodukts. Hersteller von Medizinprodukten müssen ein effektives Risikomanagement, eine Risikokontrolle und eine Risikobewertung nachweisen.
- Gerätedesign und -kontrollen: Unter QMSR wurden die Designkontrollen erweitert, um sicherzustellen, dass Hersteller von Medizinprodukten die Benutzerbedürfnisse, die Sicherheit des Geräts und die Leistungskriterien vollständig berücksichtigen, was ein Schwerpunktbereich während der USFDA-Inspektion ist.
- Post-Market Surveillance: Unternehmen müssen ihr System zur Überwachung nach dem Inverkehrbringen verbessern. Dies erfordert von den Herstellern, Informationen zur Sicherheit und Wirksamkeit des Produkts zu sammeln, was hilft, Probleme schnell zu erkennen und zu beheben.
- Dokumentation und Aufbewahrung von Aufzeichnungen: Dies ist die endgültige Regel, die die Dokumentation betont. Eine gründliche und ordnungsgemäße Aufbewahrung von Aufzeichnungen ist während der Inspektion entscheidend.
Schritte zur Vorbereitung auf die Inspektion durch die US Food and Drug Administration:
Angesichts der Inspektionsfrist bis 2026 haben Unternehmen zwei Jahre Zeit, um ihre Qualitätssysteme an den QMSR anzupassen. Es kann jedoch riskant sein, bis zur letzten Minute zu warten.
Schritte für die USFDA-Inspektion im Rahmen des QMSR für Branchen, deren aktuelles QMS auf QSR basiert:
- Führen Sie eine Gap-Analyse durch: Dies ist der erste Schritt, bei dem das aktuelle Qualitätssystem von den neuen QMSR-Anforderungen abweicht. Eine gründliche Gap-Analyse hilft dabei, die Bereiche zu identifizieren, die aktualisiert werden müssen, wie Risikomanagement, Post-Market Surveillance und Designkontrollen.
- Aktualisieren Sie das Risikomanagementverfahren: Stellen Sie sicher, dass die Risikomanagementaktivitäten in den gesamten Lebenszyklus Ihres Produkts integriert sind, vom Design bis zur Post-Market Surveillance.
- Überprüfen Sie die Produktentwicklungskontrolle: Hersteller müssen sicherstellen, dass der Entwicklungsprozess zuverlässig und gut dokumentiert ist. Bestätigen Sie, dass der Entwicklungsprozess zuverlässig und gut dokumentiert und vollständig in Ihr Qualitätsmanagementsystem eingebunden ist.
- Verbessern Sie die Überwachung nach dem Inverkehrbringen: Führen Sie Systeme ein, um die Leistung des Produkts zu überwachen, nachdem es auf den Markt gebracht wurde. Dazu gehören die Einrichtung von Kundenfeedback-Systemen, das Sammeln klinischer Daten und deren genaue Verfolgung.
- Schulung und Dokumentation: Schulung der Mitarbeiter zu den neuen Anforderungen, insbesondere derjenigen, die im Qualitätsmanagement und in der regulatorischen Compliance tätig sind. Dies stellt sicher, dass der gesamte Dokumentationsprozess den QMSR-Erwartungen entspricht.
- Zertifizierung durch Dritte: Wenn Ihr Unternehmen nicht nach ISO 13485 zertifiziert ist, könnte jetzt der richtige Zeitpunkt sein, dies in Betracht zu ziehen. Eine ISO 13485-Zertifizierung kann Ihnen einen Vorsprung verschaffen, um die Anforderungen der USFDA zu erfüllen und die Glaubwürdigkeit auf globalen Märkten zu stärken.
Die zweijährige Übergangsphase erfolgreich gestalten
Um die Übergangszeit effektiv zu nutzen und die Einhaltung der Qualitätsmanagementsystem-Verordnung (QMSR) der USFDA sicherzustellen, sollten Hersteller einen proaktiven Ansatz verfolgen. Hier ist ein vorgeschlagener Fahrplan:
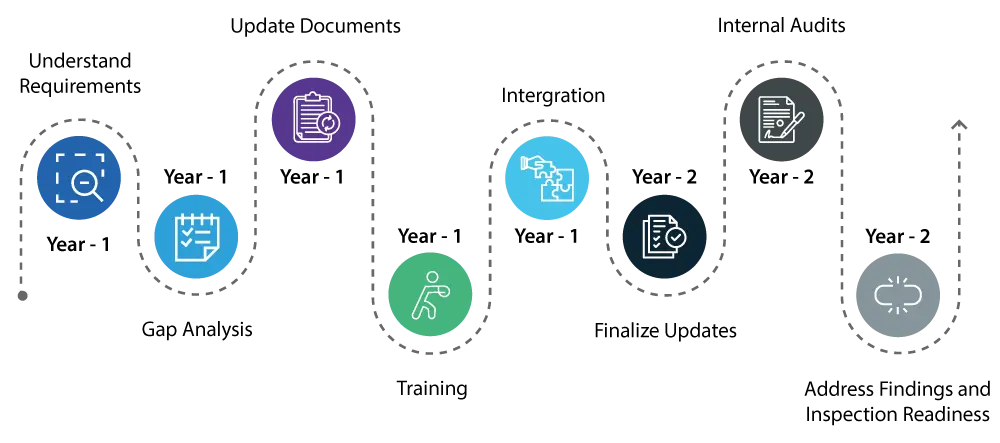
Jahr 1:
- Anforderungen verstehen: Machen Sie sich zunächst gründlich mit den Änderungen vertraut, die durch die QMSR eingeführt wurden. Dies beinhaltet eine detaillierte Prüfung der neuen Anforderungen und wie sie sich von der bestehenden Qualitätsmanagement-System (QS)-Verordnung unterscheiden.
- Lücken erkennen: Führen Sie eine umfassende Lückenanalyse durch, um Bereiche in Ihrem aktuellen Qualitätssystem zu identifizieren, die aktualisiert werden müssen, um die neuen QMSR-Standards zu erfüllen.
- Dokumentenaktualisierung / Behebung: Leiten Sie die notwendigen Aktualisierungen Ihres Qualitätssystems ein. Konzentrieren Sie sich dabei auf Bereiche wie Risikomanagement und Produktentwicklungskontrollen, die wesentliche Bestandteile der QMSR sind.
- Schulung: Beginnen Sie mit der Schulung Ihrer Mitarbeiter zu den neuen Vorschriften. So stellen Sie sicher, dass alle Beteiligten über die Änderungen informiert sind und ihre Aufgaben bei der Einhaltung der Vorschriften verstehen.
- Integration: Beginnen Sie damit, die neuen QMSR-Anforderungen in Ihre täglichen Abläufe zu integrieren, um den Übergang zu erleichtern.
Jahr 2:
- Fahren Sie mit der Implementierung der Änderungen an Ihrem Qualitätssystem fort und stellen Sie sicher, dass alle Aktualisierungen vollständig integriert und betriebsbereit sind.
- Führen Sie gründliche interne Audits durch, um zu überprüfen, ob die Aktualisierungen wirksam sind und Ihr Qualitätssystem vollständig mit den QMSR-Anforderungen übereinstimmt.
- Beheben Sie alle Feststellungen aus den internen Audits umgehend, um sicherzustellen, dass alle Aspekte Ihres Qualitätssystems konform sind.
- Bis zum Ende des zweiten Jahres sollte Ihr Qualitätssystem vollständig mit der QMSR konform sein, und Sie sollten auf USFDA-Inspektionen vorbereitet sein, mit der Gewissheit, dass es keine größeren Probleme geben wird.
Durch die Befolgung dieses Fahrplans können Hersteller nicht nur die Anforderungen der USFDA erfüllen, sondern auch ein robustes Qualitätssystem etablieren, das effizient, standardisiert und weltweit anerkannt ist. Dieser proaktive Ansatz wird dazu beitragen, einen reibungslosen Übergang zu den neuen Vorschriften zu gewährleisten und die höchsten Qualitäts- und Sicherheitsstandards für Medizinprodukte aufrechtzuerhalten.
Fazit: Proaktives Handeln
Die Vorbereitung auf USFDA-Inspektionen unter der neuen QMSR-Regel dient nicht nur der Vermeidung von Strafen – es geht darum, die Sicherheit und Wirksamkeit von Medizinprodukten zu verbessern. Durch die Harmonisierung mit ISO 13485 setzt die USFDA höhere Erwartungen, bietet aber auch einen Weg zu einer optimierten globalen Compliance. Hersteller, die frühzeitig mit der Anpassung beginnen, sollten sich auf Schlüsselbereiche wie Risikomanagement und Post-Market Surveillance konzentrieren und sicherstellen, dass ihre Qualitätssysteme aktuell und robust sind, was nicht nur die regulatorischen Erwartungen erfüllt, sondern auch ihren Wettbewerbsvorteil auf dem Markt stärkt.

