
Für Pharmaunternehmen ist es schwierig, alle bestehenden globalen regulatorischen Anforderungen zu kennen, da sich die weltweiten Vorschriften und Gesetze ständig ändern. Aufgrund des internationalen Harmonisierungsprozesses werden weltweit ständig neue Verfahren von den Regulierungsbehörden entwickelt und eingeführt.
GESCHICHTE DER REGULATORY INTELLIGENCE (RI)
RI ist typischerweise Teil der globalen Abteilung für regulatorische Angelegenheiten eines Unternehmens und erweitert die traditionelle Funktion der regulatorischen Angelegenheiten über die Vorbereitung und Einreichung von Anträgen bei der FDA und den Regulierungsbehörden Europas und Asiens hinaus.
Die Unternehmensleitung wird über aktuelle Vorschriften informiert, die die Entwicklung, Zulassung und Pflege von Produkten betreffen, sowie über alle Änderungen der Vorschriften und/oder der regulatorischen Landschaft, die ihre Bemühungen beeinflussen könnten.
RI trägt zum Geschäftserfolg jedes Pharmaunternehmens bei, indem es den Teams für regulatorische Angelegenheiten hilft, den Behörden Einreichungen von höchster Qualität zu liefern. Unternehmen müssen auch die Probleme verstehen, die die Prüfung neuer Arzneimittelanträge in jedem Markt der Welt beeinflussen, abgesehen von regulatorischen Leitlinien.
DAS REGULATORISCHE UMFELD
Die ständigen Veränderungen im regulatorischen Umfeld erfordern, dass alle beteiligten Parteien/Behörden über die aktuellen Informationen aus verschiedenen Quellen auf dem Laufenden sind. Experten für regulatorische Angelegenheiten können auf Branchenpraktiken, Meinungen von Regulierungsbehörden und Wettbewerbsinformationen zurückgreifen, um erfolgreiche regulatorische Strategien zu entwickeln.
REGULATORY INTELLIGENCE (RI)
RI ist das Sammeln und Analysieren von regulatorischen Informationen, um deren Auswirkungen oder Änderungen in Gesetzen, Vorschriften, Richtlinien, Leitfäden usw. zu verstehen. RI ermöglicht es einem Experten für regulatorische Angelegenheiten, Mitarbeiter zu beraten, strategische regulatorische Fragen zu beantworten und einen globalen Zulassungsantrag zu verfassen oder zu erstellen. Zudem hilft es, die Anforderungen für die Durchführung globaler klinischer Studien und die Herstellungsanforderungen zu bestimmen.
RI bietet Einblicke in die Beschaffung, Filterung, Analyse und Anwendung von Informationen, um wertvolle regulatorische Informationen zu gewinnen. Regulatory Intelligence folgt einem systematischen Prozess, um die Abläufe innerhalb der Regulatory Affairs zu optimieren.
WIE FUNKTIONIERT REGULATORISCHE INTELLIGENZ FÜR SIE?
Bevor klinische Zulassungen beantragt werden, stellt die Abteilung für regulatorische Angelegenheiten einige Fragen, um die Vor- und Nachteile der Einführung eines bestimmten Arzneimittels/Produkts in verschiedenen Regionen sowie andere Compliance-Anforderungen zu untersuchen. Die Forschungsfragen werden von den geschäftlichen Anforderungen bestimmt und sind mit Entscheidungen und Maßnahmen verknüpft.
Der Regulatory Intelligence-Prozess ermöglicht eine flexible Forschungsanalyse. Er deckt die gesamte Produktpalette ab, die Folgendes umfasst: Arzneimittel, Medizinprodukte, Biologika, Tierarzneimittel, Verbraucher- und OTC-Produkte sowie Nutrazeutika.
Die regulatorischen Informationen umfassen: Neue Leitlinien, Leitlinienänderungen, Pharmazeutische Entwicklung, Herstellung, Qualität, Klinisch & Nicht-Klinisch, Stabilität & Lagerung, Validierung, Verpackung & Kennzeichnung, Pharmazeutische Hilfsstoffe, Verunreinigungen, Artwork & Werbematerial, Rückrufhinweis, Sicherheit & Pharmakovigilanz, Warnhinweise, Einreichungsformate und vieles mehr.
GLOBALE REGULATORISCHE STRATEGIE: BEDEUTUNG
Veränderungen im globalen Umfeld können die weltweite regulatorische Strategie beeinflussen, da immer mehr Unternehmen weltweit Studien durchführen und Zulassungsanträge einreichen. RI-Experten vergleichen regulatorische Entwicklungen in verschiedenen Ländern, bewerten die Angemessenheit bestehender regulatorischer Rahmenbedingungen im Hinblick auf die neuesten technologischen Entwicklungen oder führen regulatorische Analysen im Rahmen von Due-Diligence-Berichten durch.
REGULATORISCHE PRÄZEDENZ
Eine regulatorische Strategie kann durch die Überwachung und Sammlung von RI entwickelt werden, was zu folgenden Ergebnissen führen kann:
• Verkürzung der Zulassungsdauer
• Maximierung der Zielmärkte
• Geringere Kosten für die Produktentwicklung auf Basis aktueller Informationen
QUELLEN FÜR REGULATORISCHE INFORMATIONEN
Regulatorische Präzedenzfälle | Branchenpraktiken | Meinungen von Regulierungsbehörden | Websites der Behörden | Leitliniendokumente | E-Mails von regulatorischen Websites | Interaktionen mit Prüfern der Behörden | Warnschreiben | Kollegen und Berater | Anfragen nach dem Informationsfreiheitsgesetz | Informationen von Wettbewerbern | Relevante Fachzeitschriften und Newsletter | Relevante Konferenzen | Beratungstreffen | Interaktionen mit anderen Fachleuten für regulatorische Angelegenheiten
PHARMAZEUTISCHE UNTERNEHMEN UND REGULATORISCHE INFORMATIONEN
Neue Geschäftsmodelle, einschließlich alternativer Informationsmanagement-Plattformen, werden von führenden Pharmaunternehmen evaluiert, um Kosten zu senken, Zeitpläne zu verkürzen und Qualität und Compliance aufrechtzuerhalten. Im aktuellen regulatorischen Umfeld haben die meisten Pharmaunternehmen Schwierigkeiten, die F&E-Produktivität aufrechtzuerhalten.
Pharmaunternehmen sind daran interessiert, neue Arzneimittelentwicklungsmodelle zu erforschen, die Entwicklungskosten senken, Zeitpläne beschleunigen und dennoch Qualität und Compliance aufrechterhalten können. Sie beabsichtigen, diese Vorteile zu realisieren, indem sie schrittweise neue Geschäftsmodelle für das Daten- und regulatorische Management einführen.
Innovative Informationsmanagement-Plattformen, die den gesamten Umfang der regulatorischen und klinischen Datenoperationen mit Unterstützung in allen geografischen Regionen und bei allen Regulierungsbehörden verwalten können, werden von Pharmaunternehmen erforscht. Informationsmanagement-Plattformen machen Forschungsdaten breiter verfügbar, indem sie die Art und Weise standardisieren, wie diese gesammelt, formatiert und verteilt werden, und bieten einzigartige Perspektiven für den Untersuchungsprozess.
Mithilfe von Analysetools und -techniken können Forscher Modellergebnisse liefern, Trends erkennen und die richtigen Fragen stellen, was wiederum den Unternehmen hilft, Prozesse zu standardisieren und zu optimieren. Bemühungen zur Prozessoptimierung werden mehr Aktivitäten in den Bereichen regulatorische, Pharmakovigilanz- und klinische Prozesse umfassen.
Diese werden wiederum durch integrierte Technologie- und Analysefähigkeiten unterstützt, die eine globale regulatorische Compliance ermöglichen. Die schnelle Umstellung zur Modernisierung ihrer Entwicklungsabläufe dient teilweise dazu, veraltete Entwicklungsmodelle, insbesondere interne Technologielösungen, abzuschaffen, die wiederum verlangsamte Wachstumsraten ausgleichen werden, um letztendlich positive Ergebnisse zu erzielen.
BUSINESS INTELLIGENCE UND PHARMABRANCHE
Angesichts sich ändernder Vorschriften und Compliance-Probleme stehen Pharmaunternehmen gleichzeitig vor den Herausforderungen, Kosten zu senken, Umsatz und betriebliche Effizienz zu steigern, Lieferkettenkosten zu senken, während sie gleichzeitig regulatorische und Sicherheitsanforderungen erfüllen. Pharmaunternehmen können strategisch Business-Intelligence-Software nutzen, um fundierte Geschäftsentscheidungen zu treffen.
Die Business-Intelligence-Software kann große Datenmengen mittels Business-Intelligence-Architektur analysieren, berichten und überwachen und Unternehmen dabei helfen, Kosten zu senken, den Umsatz zu steigern und den Wert von Informationen zu maximieren.
RI-HERAUSFORDERUNGEN FÜR UNTERNEHMEN
Große und mittelständische Unternehmen mit Produkten in vielen Märkten stehen vor einer erheblichen Herausforderung bei der Beschaffung verlässlicher regulatorischer Informationen von spezialisierten Gruppen für regulatorische Informationen. Unternehmen gehen davon aus, dass diese Gruppen eine maßgebliche Auslegung einer Vielzahl nationaler und regionaler Vorschriften liefern. Darüber hinaus muss die Gruppe auch eine Folgenabschätzung für vorgeschlagene regulatorische Änderungen in vielen weiteren Märkten bereitstellen.
RI-GRUPPEN: HERAUSFORDERUNGEN
In einer Umfrage aus dem Jahr 2014 zu zentralisierten RI-Programmen bewerteten die Befragten die Produkte der RI-Gruppe als sehr wertvoll, zeigten jedoch eine geringe Zufriedenheit.
• Das zentrale RI-Programm ist in der Regel am Unternehmenshauptsitz angesiedelt und wird verwaltet
durch ein relativ kleines Team
• Die Arbeit der zentralen RI-Gruppe ist oft relativ breit gefächert und mit kritischen Kernaufgaben verbunden.
• Steigende Anforderungen an Informationen und Prüfungen durch Gesundheitsbehörden
• 67 % der Unternehmen haben eine zentrale Stelle/ein Programm für Regulatorische Intelligenz eingerichtet
• Ein Viertel antwortete mit „Ja“ auf die Frage, ob das zentralisierte RI-Programm als
die maßgebliche Quelle für *Hard- und Soft-Intelligenzdienste
*Harte und weiche Intelligence-Dienste umfassen Kern-RI-Dienste wie die Interpretation von Gesetzen, Vorschriften der Gesundheitsbehörden und Leitlinien.
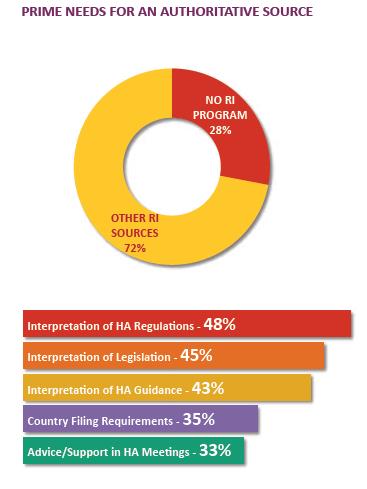
GRÜNDE, WARUM WENIGER UNTERNEHMEN DIE RI-GRUPPE ALS AUTORITATIVE QUELLE ANSEHEN
Nutzen Sie andere interne Experten, um eine vollständige Analyse zu Vorschriften oder Leitlinien zu erstellen.
Einige Akteure verlassen sich auf interne Netzwerke und externe Quellen, um eine Meinung und einen Aktionsplan zur Erfüllung neuer regulatorischer Anforderungen zu entwickeln.
UNTERNEHMEN PLANEN EINE ÄNDERUNG BEI
PROZESS: Verbesserung der internen Kommunikation zwischen der zentralen Gruppe, regulatorischen Tochtergesellschaften und Funktionsbereichen.
TOOLS FÜR DAS MANAGEMENT REGULATORISCHER INFORMATIONSPROZESSE: Verbesserung des Informationszugangs durch Portale, Wissensmanagementsysteme und externe Tools.
ROLLEN & VERANTWORTLICHKEITEN: Organisatorische Änderungen – zur Identifizierung und Verbesserung der Leistungserbringung, um die Zufriedenheit der Akteure zu steigern.
LANGFRISTIGE STRATEGISCHE VORTEILE DER REGULATORISCHEN INTELLIGENZ
Überwacht das regulatorische Umfeld und gewährleistet die Compliance.
Spart Zeit und Geld durch Echtzeit-Informationsbeschaffung, -analyse und -verbreitung.
Vermeidet das Risiko von Doppelarbeit und Redundanzen.
Überwindet globale Sprachbarrieren durch sofortigen Zugriff auf wesentliche Details in Englisch.
Gewährleistet die Richtigkeit kritischer Informationen, die von Distributoren, Herstellern und anderen
Branchenkontakten stammen.
Pflegt eine Wissensdatenbank, indem das regulatorische Wissen
innerhalb des Unternehmens bewahrt und ständig erweitert wird.
Unterstützt bei der Erstellung einer robusten regulatorischen Strategie.
Überprüft und hilft bei der Aktualisierung alter Daten mit aktuellen regulatorischen Trends.
Berät die Belegschaft zu verschiedenen neu entstehenden regulatorischen Disziplinen.
Bietet detaillierte und maßgeschneiderte Einblicke für die erweiterte Suche.
Bietet ein zentralisiertes und strukturiertes Informationsmanagementsystem.
ZUSAMMENFASSEND
Alle Unternehmen betreiben in gewissem Umfang regulatorische Intelligenz, und immer mehr Unternehmen gründen spezielle Intelligence-Gruppen. Der Umfang der regulatorischen Intelligenz variiert zwar in Form von aktiver Analyse und Interpretation, sie ist jedoch nicht gleichzusetzen mit regulatorischen Informationen.
Darüber hinaus ist regulatorische Intelligenz unerlässlich, zusammen mit der Zuweisung von Schlüsselaufgaben, um Compliance, zukünftiges Bewusstsein und eine angemessene Ressourcenplanung sicherzustellen. Die Vorteile korrekter regulatorischer Informationen ermöglichen die Entwicklung und Umsetzung einer guten regulatorischen Strategie, was zu einer verkürzten Markteinführungszeit sowohl durch beschleunigte Entwicklung als auch durch eine reibungslosere Registrierungsbewertung, reduzierten Kosten, erhöhter Compliance und letztendlich einer Optimierung des Return on Investment führt.










