Übersicht über die Dienstleistungen zur Einhaltung der EU-IVDR
Die europäische Verordnung über In-vitro-Diagnostika (EU-IVDR) bildet eine neue Rechtsgrundlage für das Inverkehrbringen von In-vitro-Diagnostika auf dem europäischen Markt. Die EU-IVDR soll die derzeitige EU-Richtlinie über In-vitro-Diagnostika (EU 98/79/EG) ersetzen. Als europäische Verordnung gilt sie in allen EU-Mitgliedstaaten und den Mitgliedstaaten der Europäischen Freihandelsassoziation (EFTA), ohne dass eine Umsetzung in nationales Recht erforderlich ist. Als bewährter Partner in Regulierungsfragen bietet Freyr der Industrie Compliance- und Beratungsdienstleistungen im Bereich der IVDR innerhalb der EU an, um die Einhaltung der Vorschriften für In-vitro-Diagnostika und die CE-Kennzeichnung sicherzustellen.
Die IVDR-Verordnung – Zeitplan für die Übergangsphase
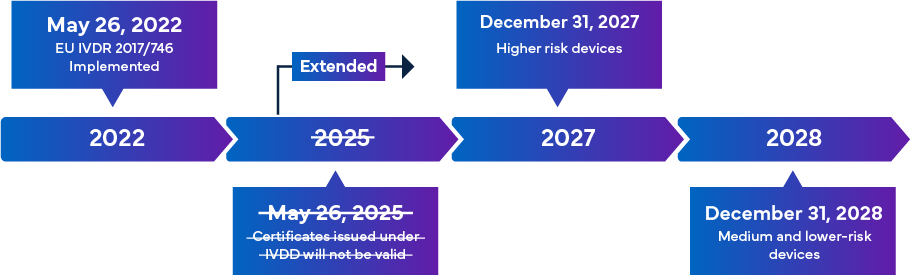
Die neue europäische IVDR-Verordnung, die am 26. Mai 2022 in Kraft treten soll, gilt als bedeutende Veränderung in der behördlichen Überwachung von In-vitro-Diagnostika. Der Überblick über den Übergang zur IVDR sieht wie folgt aus –
Sobald die Konformitätsvorschriften der IVDR vollständig umgesetzt sind, stellen sie sicher, dass nahezu alle In-vitro-Diagnostika, die auf den europäischen Markt gelangen, im Rahmen des Zulassungsverfahrens für In-vitro-Diagnostika der Prüfung durch die benannte Stelle (BS) der IVDR und der Zertifizierung der CE-Kennzeichnung unterzogen werden. In diesem Szenario müssen die Hersteller neben der Anpassung an die aktualisierte Klassifizierung der IVDR unverzüglich die wichtigsten technischen Unterlagen überarbeiten, um die Registrierung des IVD und die CE-Kennzeichnung erfolgreich abzuschließen. Die Anforderungen der IVDR variieren je nach Risikoklasse des IVD. Im Allgemeinen müssen Hersteller für die Zertifizierung von IVD folgende Schritte durchführen:
- Prüfung der technischen Unterlagen gemäß der IVDR-Verordnung (Verordnung (EU) 2017/746)
- Erstellung des Leistungsbewertungsberichts (PER) für alle IVD
- Leistungsüberwachung nach dem Inverkehrbringen (PMPF) gemäß Anhang XIII Teil B der IVDR.
- Sicherheitsbericht gemäß Artikel 82 der IVDR
Freyr unterstützt seine Kunden bei der Durchführung einer systematischen Literaturrecherche und hilft ihnen bei der Planung und Erstellung eines PER, um die Anforderungen der In-vitro-Diagnostika-Verordnung zu erfüllen. Freyr verfügt über spezialisierte Experten, die Beratungsdienstleistungen im Bereich der IVDR sowie Unterstützung bei der Überwachung nach dem Inverkehrbringen (PMA) anbieten, die ein integraler Bestandteil des Qualitätsmanagementsystems des Herstellers sowie der Leistungsüberwachung nach dem Inverkehrbringen (PMPF) ist.
Dienstleistungen zur Einhaltung der EU-IVDR – Fachkompetenz und Vorteile
- Übergangsplan zur Einhaltung der IVDR
- Technische Prüfung und Lückenanalyse der IVDR-Anforderungen für GSPR (allgemeine Sicherheits- und Leistungsanforderungen)
- Unterstützung bei der Erstellung der technischen Unterlagen gemäß den Anforderungen der IVDR
- Berichte zur wissenschaftlichen Validität auf der Grundlage von Literatur und/oder internen Daten
- Berichte über die klinische Wirksamkeit auf der Grundlage der Fachliteratur und/oder interner Daten
- Klinische Daten oder Leistungsbewertungsberichte
- Protokolle und Berichte zur Überwachung der Leistung nach der Markteinführung (SPPM)
- Protokolle und Berichte zur Überwachung nach dem Inverkehrbringen (PMPF)
- Erstellung/Überarbeitung weiterer Dokumente wie Packungsbeilagen/Gebrauchsanweisungen (IFU), Kurzanleitungen (QRI), Bedienungs- und Betriebsanleitungen usw.

- Gewährleistung der IVDR-Konformität, der IVD-Registrierung und der CE-Kennzeichnung
- Fundierte Kenntnisse der Rechtsvorschriften und Fachkompetenz in den wichtigsten Anwendungsbereichen der EU-IVDR
- Ein projektorientiertes Liefermodell, um die Einhaltung des Zeitplans sicherzustellen.
- Interne Sachverständige der ON (Prüfung des Berichts durch die interaktiven Prüfer der ON)
- Spezialisierte Teams mit interdisziplinärem Fachwissen in bestimmten Wirkungsbereichen und spezifischen Maßnahmenkategorien
- Funktionsübergreifende Beiträge von Experten für Medizinprodukte zur Erfüllung der Anforderungen
- Gesamtheit der Dienstleistungen in den Bereichen Compliance, Prüfung und Planung
- Umfassende Fachkenntnisse hinsichtlich der Gewährleistung der Konsistenz der Ergebnisse (Termintreue und Qualität)

