Innovative Medizinprodukte sind entscheidend, um die Gesundheitsversorgung zu verbessern, sich entwickelnde medizinische Bedürfnisse zu adressieren und kostengünstige Lösungen für Patienten und Gesundheitsdienstleister bereitzustellen. Die SAKIGAKE-Strategie ist ein beschleunigtes Prüf- und Genehmigungsverfahren für innovative Medizinprodukte in Japan. Diese Strategie wurde 2015 vom japanischen Ministerium für Gesundheit, Arbeit und Soziales (MHLW) initiiert, mit dem Ziel, die Entwicklung und Kommerzialisierung innovativer Medizinprodukte in Japan zu beschleunigen.
Im Rahmen der SAKIGAKE-Strategie können Medizinprodukte, die bestimmte Innovationskriterien erfüllen, eine bevorzugte Prüfung und Genehmigung durch die Pharmaceuticals and Medical Devices Agency (PMDA) erhalten, die für die Zulassung von Medizinprodukten in Japan zuständige Regulierungsbehörde. Die Kriterien für die Innovationsbezeichnung umfassen Folgendes:
- Produkte mit herausragender Wirksamkeit; von dem Produkt wird erwartet, dass es einen erheblichen klinischen Nutzen mit einem neuartigen Wirkmechanismus und eine radikale Verbesserung für Patienten im Vergleich zu bestehenden Medizinprodukten bietet.
- Erstens ist das Produkt für Zulassungen in Japan oder gleichzeitig in Japan und anderen Ländern geeignet.
- Das Produkt hat das Potenzial, ungedeckte medizinische Bedürfnisse in Japan zu erfüllen. Die Zielerkrankung sollte schwerwiegend, lebensbedrohlich oder mit anhaltenden Symptomen verbunden sein.
Im Rahmen der SAKIGAKE-Strategie können Hersteller von Medizinprodukten eine Reihe von Vorteilen erhalten, darunter:
- Vorrangige Beratung: Verkürzung der Wartezeit für die Beratung zu klinischen Studien auf einen (01) Monat.
- Prioritätsprüfung: SAKIGAKE-Produkte erhalten eine Prioritätsprüfung mit dem Ziel, den Prüfprozess innerhalb von sechs (06) Monaten anstelle von 12 Monaten abzuschließen.
- Effektive Prüfung vor der Antragstellung: Förderung der Beratung und Annahme von Unterlagen in englischer Sprache.
- Fester Ansprechpartner für die Prüfung: Jedem SAKIGAKE-Produkt wird ein fester Prüfmanager für den gesamten Zulassungsprozess zugewiesen.
- Stärkung der Sicherheitsmaßnahmen nach der Markteinführung: Verlängerung der Nachprüfungsfrist und Erleichterung der Zusammenarbeit mit wissenschaftlichen Gesellschaften.
Wie erfolgt die Antragstellung?
- Durch den Antragsteller: Der Antragsteller reicht den Antrag bei der PMDA Evaluation and Licensing Division (ELD) ein.
- Durch die PMDA-ELD: Die ELD tritt an einen potenziellen Antragsteller heran.
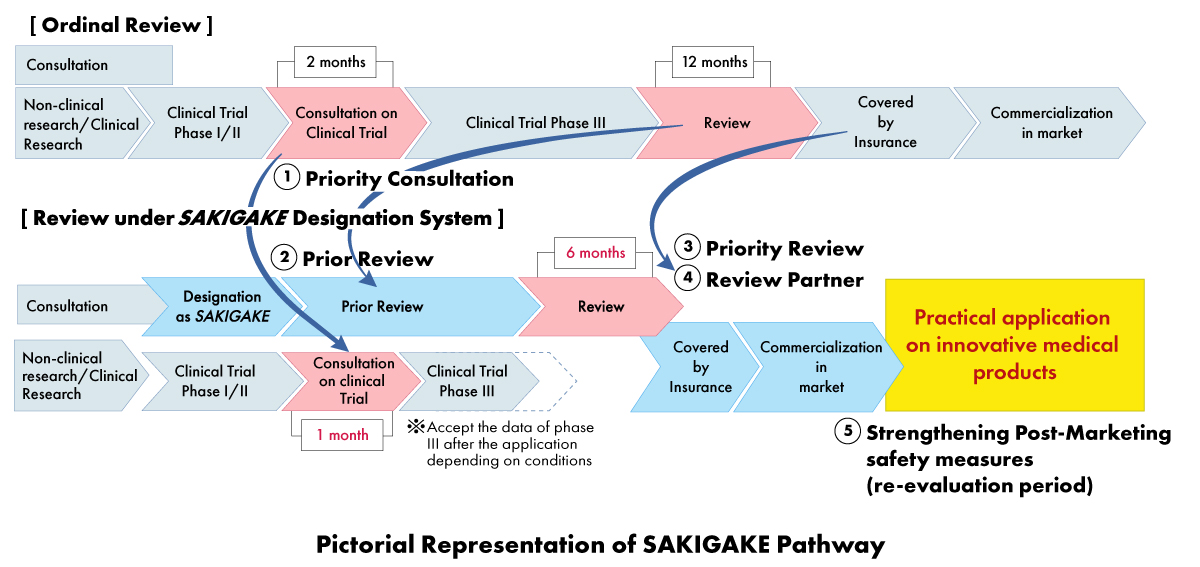
Bildquelle: PMDA, Japan.
Insgesamt bietet das SAKIGAKE-System einen beschleunigten Weg für die Entwicklung und Zulassung innovativer Medizinprodukte in Japan. Es zielt darauf ab, die Patientenergebnisse zu verbessern und Innovationen in der Medizinprodukteindustrie zu fördern. Der Hersteller muss die PMDA frühzeitig im Entwicklungsprozess konsultieren, um regulatorische Anforderungen zu besprechen und Feedback zu seinen Produktentwicklungsplänen zu erhalten.
Um mehr über die Registrierungswege für Medizinprodukte in Japan zu erfahren, kontaktieren Sie jetzt einen Regulierungsexperten! Bleiben Sie informiert. Bleiben Sie konform.