
Quel est le rôle de la cybersécurité dans les dispositifs médicaux ?
La procédure d'autorisation 510(k)est une voie réglementaire utilisée par la Food and Drug Administration (FDAUS pour évaluer et autoriser la commercialisation des dispositifs médicaux. Cette procédure vise à garantir que les dispositifs médicaux sont sûrs et efficaces pour les patients. US FDA la cybersécurité comme « le processus visant à empêcher tout accès non autorisé, toute modification, toute utilisation abusive ou tout refus d'utilisation, ou encore toute utilisation non autorisée des informations stockées, consultées ou transférées depuis un dispositif médical vers un destinataire externe ».
Les dispositifs médicaux sont de plus en plus connectés aux réseaux et sont donc vulnérables aux menaces de cybersécurité telles que le piratage, les fuites de données et les attaques de logiciels malveillants. Aborder la cybersécurité dès la phase de conception et de développement est essentiel pour garantir que les dispositifs médicaux disposent de contrôles de sécurité appropriés. Les menaces et les vulnérabilités ne peuvent pas être éliminées, et la réduction des risques de cybersécurité est particulièrement difficile. Si la cybersécurité n'est pas correctement maintenue, cela pourrait entraîner un dysfonctionnement des appareils, la perte de données personnelles ou médicales, et la possibilité que les menaces de sécurité se propagent à d'autres réseaux ou dispositifs interconnectés.
Incidents causés par une cybersécurité compromise
Des incidents de cybersécurité ont rendu inopérants des dispositifs médicaux et des réseaux hospitaliers, entraînant une perturbation de la prestation de soins aux patients dans les établissements de santé aux US. De telles cyberattaques et exploitations peuvent également nuire aux patients en raison de risques cliniques, par exemple, un retard dans le diagnostic et/ou le traitement des patients.
Voici les incidents majeurs survenus dans le secteur de la santé qui soulignent l'importance de la cybersécurité pour la sécurité des patients.
- En 2017, l'attaque par rançongiciel WannaCry a affecté les systèmes hospitaliers et les dispositifs médicaux dans le monde entier.
- En 2020, une attaque par rançongiciel contre un hôpital allemand a mis en évidence les quatre-vingt-trois (83) impacts potentiels des retards de soins aux patients, car l'attaque a contraint les patients à être transférés vers un autre hôpital.
Les considérations clés en matière de cybersécurité pour l'autorisation 510(k)
Voici les principes généraux de cybersécurité destinés aux fabricants de dispositifs médicaux, conformément aux recommandationsFDA US FDA spécifiques aux demandes d'autorisation de mise sur le marché.
- Règlement sur le système qualité (QSR).: Les fabricants devraient aborder les problèmes de cybersécurité dès l'étape de conception et de développement du dispositif médical, car cela peut entraîner une atténuation plus robuste et efficace des risques pour les patients. Les fabricants devraient établir des exigences de conception liées à la cybersécurité pour leur dispositif ainsi qu'une approche de gestion des vulnérabilités de cybersécurité dans le cadre de la validation logicielle et de l'analyse des risques requises par 21 CFR 820.30(g).
- Sécurité dès la conception :les fabricants de dispositifs doivent veiller à ce que leurs produits soient conçus en tenant compte de la sécurité. LaFDA US FDA l'adéquation des mesures de sécuritéFDA se basant sur la capacité du dispositif à définir et à mettre en œuvre des objectifs de sécurité tels que l'authenticité, l'autorisation, la disponibilité, la confidentialité et la sécurité, ainsi que la possibilité de mise à jour en temps opportun à tous les niveaux de l'architecture du système.
- Transparence : Un manque d'informations sur la cybersécurité de l'appareil, telles que les informations nécessaires pour intégrer l'appareil dans l'environnement d'utilisation, ainsi que les informations dont les utilisateurs ont besoin pour maintenir la cybersécurité tout au long du cycle de vie de l'appareil, peut potentiellement affecter sa sécurité et son efficacité. Pour répondre à ces préoccupations, il est important que les utilisateurs de l'appareil aient accès aux informations relatives aux contrôles de cybersécurité, aux risques potentiels et à d'autres informations pertinentes.
- Documentation de soumission : La conception et la documentation de la cybersécurité des dispositifs doivent être proportionnelles au risque de cybersécurité d'un dispositif. Les fabricants doivent prendre en compte le système plus large dans lequel un dispositif peut être utilisé.
Figure 1 : Défis et solutions courants en matière de cybersécurité 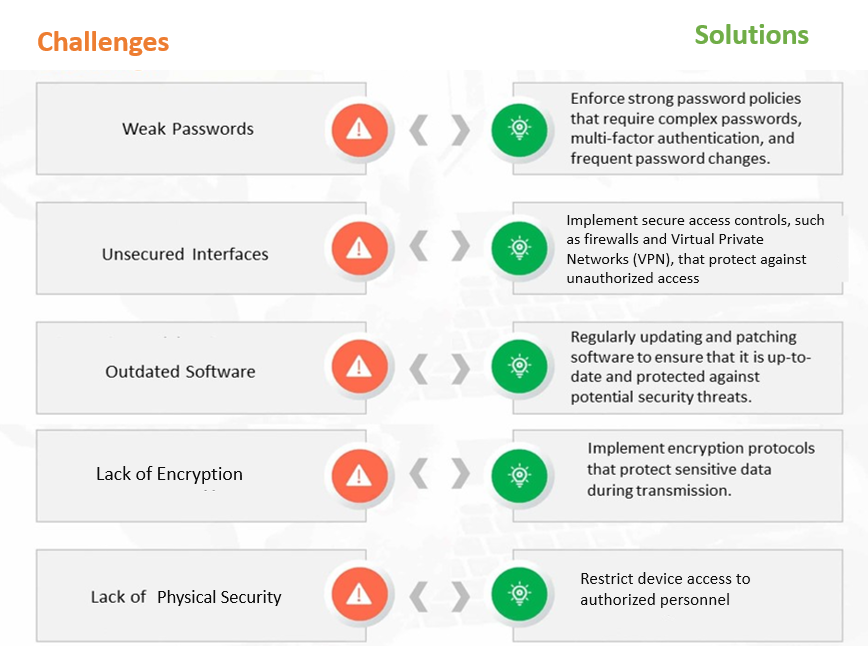
Conclusion
En résumé, la cybersécurité des dispositifs médicaux est essentielle pour garantir la sécurité des patients et prévenir les incidents susceptibles de perturber la prestation des soins de santé. Les réglementationsFDA US FDA soulignent la nécessité pour les fabricants de traiter les questions de cybersécurité dès la conception et le développement des dispositifs médicaux, et de fournir des informations transparentes sur les contrôles de cybersécurité. Les normes QSR, la sécurité de la conception, la transparence et la documentation de soumission sont des éléments clés à prendre en compte pour l'autorisation 510(k). Il est également important de relever les défis courants en matière de cybersécurité, tels que les vulnérabilités des composants tiers et les attaques par ransomware, et de mettre en œuvre des solutions telles qu'une analyse des risques rigoureuse et des mises à jour logicielles régulières.
Pour bénéficier d'un processus d'autorisation 510(k) simple et conforme, contactez nos experts en réglementation. Restez informé ! Restez conforme !









