
Un protocole de validation est défini comme un plan documenté pour tester un dispositif médical afin de confirmer que le processus de production utilisé pour fabriquer le produit répond aux exigences spécifiques de l'utilisateur, techniques et réglementaires. Cela inclut un examen des variables de processus et des limitations opérationnelles, ainsi que l'analyse des résultats des tests dans des conditions d'utilisation réelles.
Le processus de validation implique plusieurs actions concrètes. Les étapes sont expliquées comme suit :
- Tout d'abord, l'équipe de validation est constituée, et chaque membre se voit attribuer des rôles et des responsabilités spécifiques. L'objectif de la validation des processus est de fournir un énoncé clair des objectifs de validation et de définir la portée des activités de validation en spécifiant les aspects du dispositif médical qui sont validés. L'équipe comprend ensuite les principes fondamentaux du processus afin d'identifier les paramètres spécifiques et les résultats souhaités.
- Deuxièmement, les critères d'évaluation et d'acceptation sont établis, ainsi que la sélection des méthodes d'essai, des outils et des techniques d'analyse statistique appropriés. Par la suite, les protocoles de validation des processus sont rédigés, et la Qualification de l'Installation (IQ), la Qualification Opérationnelle (OQ) et la Qualification de Performance (PQ) sont mises en œuvre.
- Enfin, des contrôles de processus continus et des mesures de surveillance sont définis pour assurer la validation continue du processus. Si nécessaire, une revalidation est effectuée pour maintenir la précision et l'efficacité du processus de validation.
La figure 1 ci-dessous présente une représentation étape par étape du processus de validation.
Figure 1 : Les étapes du processus de validation
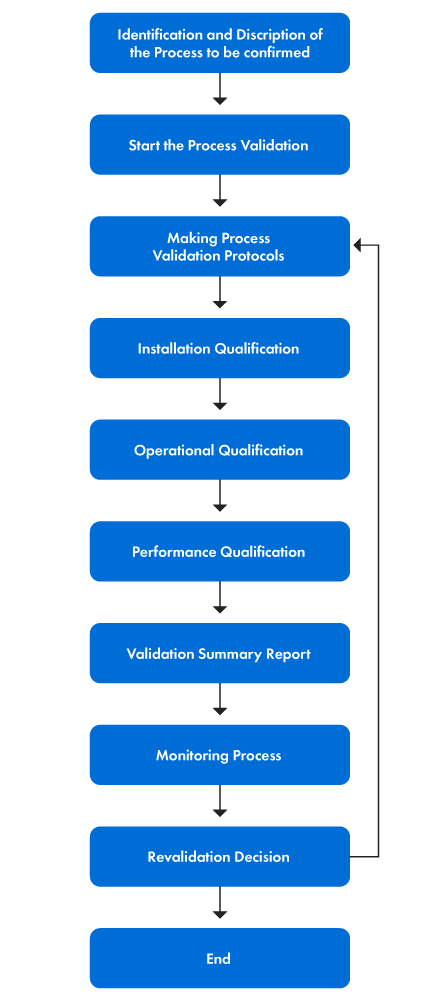
PVP
Compte tenu de la grande diversité des volumes de production et de la complexité des processus de fabrication, il existe de nombreuses approches pour mener à bien la validation des procédés. Cependant, la réglementation de la Food and Drug Administration (USFDA) des États-Unis et ISO 13485 que peu de recommandations sur les méthodes spécifiques. Néanmoins, une source largement reconnue et faisant autorité en matière de validation des processus des dispositifs médicaux est un document d'orientation du Global Harmonization Task Force (GHTF), désormais appelé International Medical Device Regulators Forum (IMDRF), publié en 2004. Il reste la référence principale, même sur le site web officiel USFDA.
Conformément au document d'orientation, une équipe de validation est formée pour créer un Plan de Validation de Processus (PVP) détaillé. Les protocoles de validation de processus comprennent un schéma détaillé sur la manière de mettre en œuvre l'IQ, l'OQ, le PQ et la revalidation. Le PVP devrait contenir les éléments suivants :
- Définir le dispositif et déterminer l'approche de validation.
- Identification des éléments qui nécessitent une validation.
- Réalisation d'activités sur le site désigné
- Définition de la portée de la documentation.
- Établissement d'un calendrier pour les activités de validation.
- Élaborer un calendrier directeur global.
- Maintenir une liste exhaustive et des références aux validations internes et externes qui ont été effectuées.
Le protocole de validation est rédigé avant de mener les activités de validation. Il doit être préparé par l'équipe de validation et approuvé par le service concerné. L'objectif d'un protocole de validation est de définir les scripts de test qui doivent être suivis pour garantir que les processus et les équipements sont prêts à fabriquer des dispositifs médicaux sûrs et efficaces.
Un rapport analytique, contenant les informations ainsi que les analyses, explications et recommandations nécessaires, fait partie du protocole de validation. Ces dossiers sont ensuite examinés pour s'assurer que les deux (02) critères suivants sont respectés :
- Conformité aux normes réglementaires.
- Tous les enregistrements et données générés sont examinés pour leurs résultats, leur adéquation et leur exhaustivité.
La figure 2 ci-dessous représente le PVP et les divers processus qui y sont associés.
Figure 2 : Le PVP et ses exigences
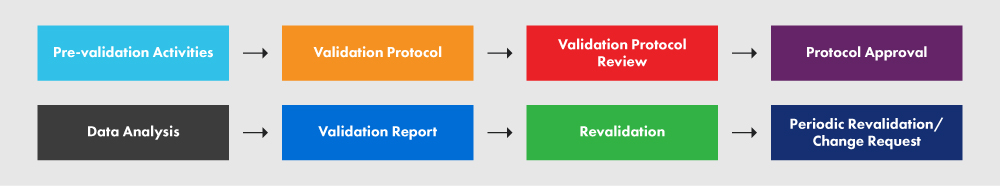
Un protocole correctement rédigé fournit des lignes directrices, des politiques et des procédures claires à respecter pendant la validation du processus. Il englobe des aspects tels que les installations, les équipements, les méthodes et la formation. Le protocole spécifie les intrants et les limites du processus, ainsi que les étapes essentielles pour la bonne exécution du projet de validation du processus. Bien que le plan suivant ne couvre pas tous les éléments requis dans votre protocole, il vous donne un aperçu du niveau de détail nécessaire. Nous recommandons fortement de suivre le document d'orientation pour une meilleure compréhension du processus.
- Page de titre
- Produits concernés
- Équipement/Processus à valider
- Généralités
- Objectifs
- Documents de référence
- Plan de validation
- IQ
- OQ
- PQ
- Équipements de mesure/d'essai et étalonnage
- Maintenance des équipements
- Revalidation
- Page d'approbation/de signature de l'équipe de validation
La gestion des opérations joue un rôle crucial dans le maintien d'une performance optimale en surveillant les indicateurs clés, en examinant les méthodes et procédures de travail, et en prenant des mesures rapides en cas de problème. En cas de problèmes, il peut être nécessaire de revalider un processus partiellement ou même entièrement. Conformément à la section 820.75(c) du Règlement sur le système qualité (QSR) de l'USFDA, la revalidation des processus doit être envisagée dans les circonstances suivantes : « Lorsque des changements ou des écarts de processus surviennent, le fabricant doit examiner, évaluer et effectuer une revalidation, le cas échéant. Ces activités doivent être documentées. »
Les déclencheurs possibles pour la revalidation des processus incluent les modifications apportées aux spécifications, aux méthodes, aux procédures, aux logiciels, aux conceptions, aux composants clés, à l'augmentation de la taille des lots, aux changements de localisation, aux changements d'équipement, et autres. De plus, la mise en œuvre d'Actions Correctives et Préventives (CAPA) peut également servir de déclencheur à la revalidation des processus. Les principales raisons de la revalidation sont les suivantes :
- Modifications apportées au processus.
- Tendance négative de la qualité, détérioration soudaine de la qualité ou augmentation soudaine des plaintes des clients.
- Extension importante de la capacité de production.
- Modifications de conception.
- Modifications de l'emballage du produit.
- Transfert d'un processus vers une autre installation.
- Modifications du processus de demande.
Pour en savoir plus sur les protocoles de validation et leur importance dans le domaine de la fabrication de dispositifs médicaux, consultez-nous ! Restez informé ! Restez conforme !









