
Die Austauschbarkeit mit einem biologischen Referenzprodukt ist ein entscheidender Schritt im Zulassungsverfahren für Biosimilars. Sie stellt sicher, dass ein Biosimilar das Referenzprodukt ersetzen kann, ohne dass ein erhebliches Risiko einer verminderten Wirksamkeit oder erhöhten Sicherheitsbedenken besteht. Dieser Blog beleuchtet das neueste FDA-Update zu den Überlegungen zur Erzielung der Austauschbarkeit sowie bewährte Branchenpraktiken zur Erreichung regulatorischer Exzellenz.
Definition der Austauschbarkeit
Die Erlangung der Austauschbarkeit ist ein komplexer und anspruchsvoller Prozess, der die Erfüllung strenger regulatorischer Anforderungen erfordert. Die Herausforderung besteht darin, zu zeigen, dass das Biosimilar nicht nur in Bezug auf Sicherheit und Wirksamkeit dem Referenzprodukt entspricht, sondern auch bei jedem Patienten die gleichen klinischen Ergebnisse liefert. Werden diese Anforderungen nicht erfüllt, kann dies zu Verzögerungen oder Ablehnungen bei der Zulassung führen, was den Marktzugang und die Patientenversorgung beeinträchtigt.
Regulatorische Anforderungen für die Austauschbarkeit
Die FDA legt in ihren Leitliniendokumenten spezifische Kriterien für den Nachweis der Austauschbarkeit fest. Diese Kriterien umfassen:
- Vergleichende analytische Studien: Umfassende analytische Studien sind erforderlich, um zu zeigen, dass das Biosimilar dem Referenzprodukt sehr ähnlich ist. Diese Studien bewerten die molekulare Struktur, Funktion und Zusammensetzung des Biosimilars.
- Klinische Studien: Klinische Studien sind notwendig, um zu bestätigen, dass das Biosimilar keine klinisch bedeutsamen Unterschiede zum Referenzprodukt in Bezug auf Sicherheit, Reinheit und Wirksamkeit aufweist. Dies beinhaltet oft vergleichende pharmakokinetische (PK) und pharmakodynamische (PD) Studien.
- Wechselstudien: Die FDA verlangt Wechselstudien, um die Auswirkungen des Wechsels zwischen dem Biosimilar und dem Referenzprodukt zu bewerten. Diese Studien sind entscheidend, um sicherzustellen, dass der Wechsel die Wirksamkeit oder Sicherheit der Behandlung nicht beeinträchtigt.
- Strategien zur Risikobewertung und -minderung (REMS): Falls zutreffend, müssen REMS-Strategien berücksichtigt werden, um sicherzustellen, dass das Biosimilar ohne zusätzliche Sicherheitsbedenken austauschbar verwendet werden kann.
Strategische Schritte zur Erlangung der Austauschbarkeit
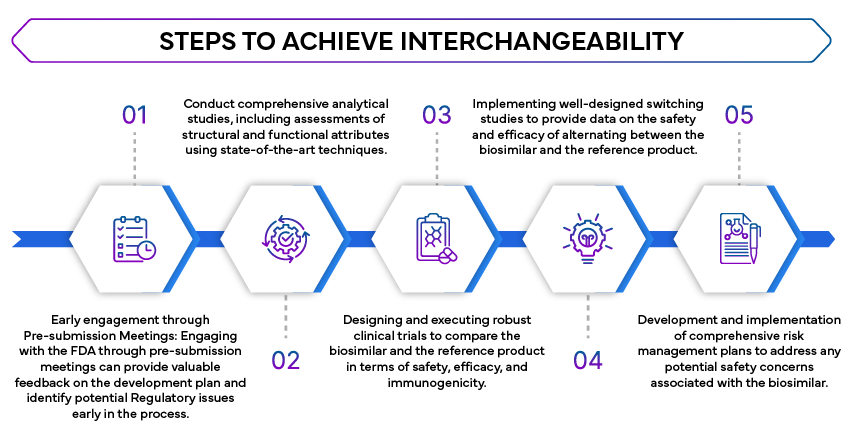
Rolle eines regulatorischen Partners
Regulatorische Partnerschaften können die Wahrscheinlichkeit, die Austauschbarkeit zu erreichen, erheblich erhöhen. So kann ein regulatorischer Partner helfen:
- Expertenberatung: Bietet fachkundige Beratung zu regulatorischen Anforderungen und Strategien zur Einhaltung der FDA-Richtlinien.
- Unterstützung bei der Dokumentation: Unterstützt bei der Erstellung hochwertiger Einreichungsdokumente, die den regulatorischen Standards entsprechen.
- Design klinischer Studien: Unterstützt das Design und die Durchführung robuster klinischer und Switching-Studien.
- Interaktionen mit Behörden: Erleichtert die effektive Kommunikation mit den Behörden und gewährleistet zeitnahes und konstruktives Feedback.
- Risikomanagement: Entwickelt umfassende Risikomanagementstrategien, um potenzielle Sicherheitsbedenken zu mindern.
Vorteile einer regulatorischen Partnerschaft
| Vorteile | Beschreibung | |
| 1. | Fachwissen über regulatorische Anforderungen | Tiefgreifendes Verständnis der globalen regulatorischen Rahmenbedingungen und Anforderungen. |
| 2. | Optimierte Dokumentation | Gewährleistet die Erstellung präziser und konformer Dokumentationen. |
| 3. | Effizienter Einreichungsprozess | Reduziert Zeit und Kosten durch effizientes Einreichungsmanagement. |
| 4. | Erhöhte Compliance | Minimiert das Risiko von Verzögerungen und Ablehnungen durch umfassende Einhaltung der Vorschriften. |
| 5. | Effektives Risikomanagement | Proaktive Identifizierung und Minderung potenzieller Risiken. |
Zusammenfassung
Die Erlangung der Austauschbarkeit mit einem Referenzprodukt ist ein anspruchsvoller, aber wesentlicher Prozess für die erfolgreiche Zulassung von Biosimilars. Sie erfordert ein umfassendes Verständnis der regulatorischen Anforderungen, eine sorgfältige Planung und robuste klinische Daten. Die Zusammenarbeit mit einem erfahrenen Anbieter regulatorischer Dienstleistungen kann die Erfolgsaussichten erheblich verbessern und sicherstellen, dass das Biosimilar die strengen Kriterien der Aufsichtsbehörden erfüllt. Durch die Nutzung von Expertenwissen, umfassender Dokumentation und strategischem Risikomanagement können Sponsoren den komplexen Weg zur Austauschbarkeit effektiver beschreiten.










