
In den letzten Jahren hat sich die Landschaft der regulatorischen Angelegenheiten erheblich verändert. Im Mittelpunkt dieser Veränderung steht eine wachsende Betonung der Patienten-zentrierung, wobei Gesundheitsbehörden (HA) weltweit die unschätzbare Rolle anerkennen, die Patienten bei der Entwicklung und Zulassung neuer Arzneimittel spielen. Dieser Wandel ist nicht nur ein Trend; er ist eine grundlegende Neugestaltung unserer Herangehensweise an regulatorische Einreichungen und letztendlich daran, wie wir denjenigen dienen, die am wichtigsten sind – den Patienten.
Das Problem:
Traditionell konzentrierten sich regulatorische Einreichungen hauptsächlich auf die Erfüllung technischer und wissenschaftlicher Anforderungen, wobei der direkte Einfluss auf Patientenerfahrungen und -ergebnisse oft übersehen wurde. Dieser Ansatz, obwohl gründlich, erfasste manchmal nicht die Nuancen der Patientenbedürfnisse, -präferenzen und des realen Gebrauchs von Arzneimitteln. Infolgedessen gab es eine Diskrepanz zwischen regulatorischen Genehmigungen und dem tatsächlichen Wert, der den Patienten geboten wurde.
Patientenzentrierte Regulierungsansätze:
Gesundheitsbehörden, insbesondere die FDA und die EMA, haben erhebliche Fortschritte bei der Einbeziehung von Patientenperspektiven in ihre regulatorischen Rahmenwerke gemacht.
Dieser patientenorientierte Ansatz zeigt sich in mehreren Schlüsselbereichen:
- Patientenorientierte Arzneimittelentwicklung (PFDD):
Das PFDD-Programm der FDA ist eine wegweisende Initiative, die systematisch Patientenfeedback sammelt, um die Arzneimittelentwicklung und regulatorische Entscheidungsfindung zu informieren. Dieses Programm umfasst Patientengespräche, öffentliche Sitzungen und die Entwicklung von Leitfäden, um die Patientenbeteiligung über den gesamten Produktlebenszyklus hinweg zu verbessern. - Real-World Evidence (RWE):
Es wird zunehmend der Wert von Real-World-Daten erkannt, um die Leistung eines Produkts in verschiedenen Patientengruppen zu verstehen. Gesundheitsbehörden sind nun offener dafür, RWE in regulatorischen Einreichungen zu berücksichtigen, was eine umfassendere Sicht auf die Vorteile und Risiken eines Produkts ermöglicht. - Patient-Reported Outcomes (PROs):
Die Einbeziehung von PROs in klinische Studien und regulatorische Einreichungen ist immer wichtiger geworden. Diese Messungen erfassen direkt die Patientenerfahrung und liefern wertvolle Einblicke in Symptome, Lebensqualität und Behandlungszufriedenheit. - Frühes Engagement und wissenschaftliche Beratung:
Gesundheitsbehörden ermutigen Sponsoren, sich frühzeitig in den Entwicklungsprozess einzubringen, wobei häufig Patientenvertreter in diese Diskussionen einbezogen werden. Dieser frühe Dialog hilft, Entwicklungspläne mit den Bedürfnissen der Patienten und den regulatorischen Erwartungen abzustimmen. - Patientenbeteiligung bei Nutzen-Risiko-Bewertungen:
Sowohl die FDA als auch die EMA haben Rahmenwerke entwickelt, um Patientenperspektiven in Nutzen-Risiko-Bewertungen einzubeziehen und so sicherzustellen, dass regulatorische Entscheidungen das widerspiegeln, was für Patienten am wichtigsten ist.
Tabelle: Wichtige patientenzentrierte Initiativen der wichtigsten Gesundheitsbehörden
| Gesundheitsbehörde | Initiative | Beschreibung |
|---|---|---|
| FDA | Patientenorientierte Arzneimittelentwicklung (PFDD) | Systematischer Ansatz zur Sammlung von Patientenfeedback |
| EMA | Arbeitsgruppe für Patienten und Verbraucher (PCWP) | Forum für den Dialog mit Patienten- und Verbraucherorganisationen |
| MHRA | Einbindung von Patienten und der Öffentlichkeit | Strategie zur Einbindung von Patienten in regulatorische Prozesse |
| Health Canada | Kanadischer Rahmen für die Einbindung von Arzneimitteln und Gesundheitsprodukten | Fördert die Patientenbeteiligung bei regulatorischen Aktivitäten |
Rolle von Regulierungsdienstleistern:
In diesem sich wandelnden Umfeld ist die Rolle von Fachleuten und Partnern im Bereich Regulatory Affairs wichtiger denn je geworden. Sie fungieren als Brücke zwischen Sponsoren, Gesundheitsbehörden und Patienten und stellen sicher, dass regulatorische Strategien mit patientenzentrierten Ansätzen übereinstimmen.
Zu den Hauptaufgaben gehören:
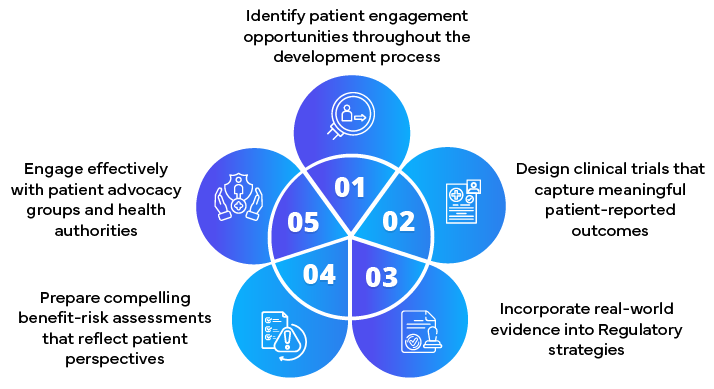
- Entwicklung von Strategien zur Patienteneinbindung
- Einbeziehung von Patientenfeedback in regulatorische Einreichungen
- Beratung zur Sammlung und Präsentation patientenzentrierter Daten
- Förderung des frühen Austauschs mit Gesundheitsbehörden
- Sich über sich entwickelnde patientenzentrierte regulatorische Anforderungen auf dem Laufenden halten
Rolle von Regulierungspartnern bei der Erstellung patientenzentrierter Einreichungen
Zusammenfassung:
Die Verlagerung hin zu einer patientenzentrierten Ausrichtung in Regulatory Affairs stellt eine bedeutende Chance dar, Medizinprodukte zu entwickeln und zuzulassen, die den Bedürfnissen der Patienten wirklich entsprechen. Durch die Übernahme dieses Ansatzes können Sponsoren nicht nur regulatorische Wege effektiver beschreiten, sondern auch Produkte liefern, die das Leben der Patienten maßgeblich verbessern. Da die Gesundheitsbehörden ihre patientenzentrierten Ansätze weiter verfeinern, wird die Expertise von Regulierungsdienstleistern oder Partnern von unschätzbarem Wert, um sicherzustellen, dass Einreichungen nicht nur technische Anforderungen erfüllen, sondern auch die Erfahrungen und Prioritäten der Patienten widerspiegeln.
In dieser neuen Ära der regulatorischen Angelegenheiten, ist es nicht nur eine gute Praxis, Patienten an erste Stelle zu setzen – es ist der Schlüssel zum Erfolg.









