KGMP steht für Korea Good Manufacturing Practice und basiert auf ISO 13485:2016. Es ist der international anerkannte Standard für Qualitätsmanagementsysteme (QMS) für Medizinprodukte. Alle Medizinproduktehersteller, die ihre Produkte in Südkorea vermarkten, müssen die KGMP-Standards einhalten.
Ist das KGMP-Zertifikat für alle Medizinprodukte obligatorisch?
Die Medizinprodukte und In-vitro-Diagnostika (IVD) der Klassen II, III und IV müssen die KGMP-Vorschriften einhalten und das KGMP-Zertifikat erhalten. Die Produkte der Klasse I sind von der KGMP-Zertifizierung ausgenommen, müssen aber die MFDS-GMP-Vorschriften für Medizinprodukte einhalten. Hersteller von Produkten der Klasse I können sich freiwillig für die „KGMP-Konformitätsanerkennung von Medizinprodukten der Klasse I“ entscheiden.
Welche zuständigen Behörden sind an der KGMP-Inspektion beteiligt?
Medizinprodukte der Klasse II unterliegen einer Überprüfung durch von der MFDS akkreditierte Prüfstellen, während Medizinprodukte der Klassen III und IV eine gemeinsame Inspektion durch die Drittprüfstelle und die MFDS erfordern.
Wer kann das KGMP-Zertifikat beantragen?
Inländische Hersteller können ihre Anträge direkt bei der externen Prüfstelle einreichen. Für ausländische Hersteller muss der lokale Bevollmächtigte des ausländischen Herstellers eine Lizenz erwerben.
Wie läuft das Verfahren zur Erlangung eines KGMP-Zertifikats ab?
Zum ersten Mal muss der Antrag (Antragsteller – lokaler Bevollmächtigter des ausländischen Herstellers und inländische Hersteller) bei von der MFDS akkreditierten Drittprüfstellen eingereicht werden. Das Verfahren zur Erlangung eines KGMP-Zertifikats ist unten aufgeführt:
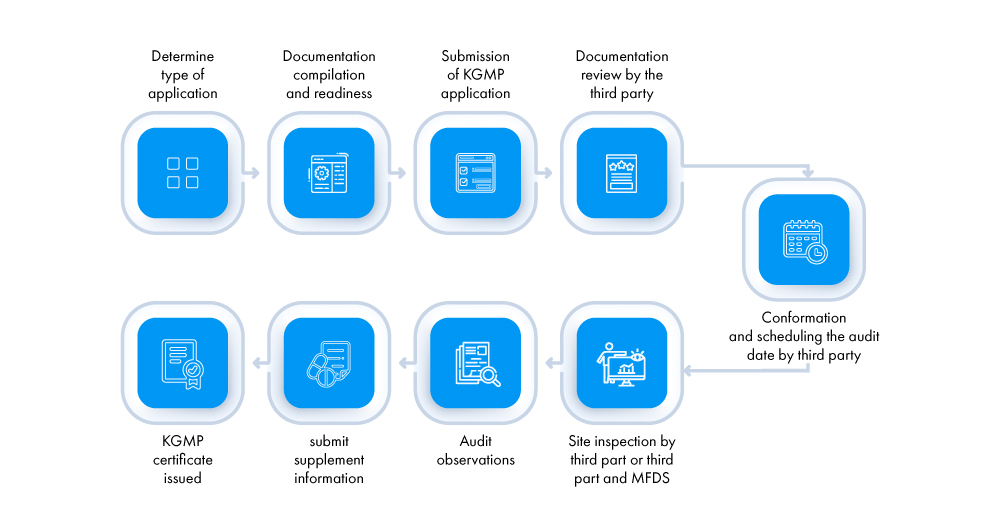
Welche verschiedenen Arten von Inspektionen gibt es zur Erlangung eines KGMP-Zertifikats?
Je nach Risikoklasse des Medizinprodukts und Art des Antrags (neu, regulär oder Änderung) kann es sich entweder um eine Vor-Ort-Inspektion oder eine Dokumentenprüfung handeln. Vor der Beantragung der KGMP-Zertifizierung müssen Hersteller die möglichen Inspektionsarten und die für ihr Szenario zutreffende Art verstehen. Die wichtigsten zu berücksichtigenden Faktoren sind:
- Wenn auf dem Standort hergestellte Medizinprodukte bereits in Korea registriert und vermarktet werden oder wenn das betreffende Medizinprodukt das erste ist, das auf dem koreanischen Markt eingeführt wird
- Wenn ein neues Medizinprodukt (einer anderen Kategorie) in der bereits KGMP-zertifizierten Fertigungsstätte eingeführt wird
- Wenn der Herstellungsort des Medizinprodukts geändert wird
Erstinspektion: Eine Erstinspektion wird durchgeführt, wenn ein auf den Markt gebrachtes Medizinprodukt in einer nicht KGMP-zertifizierten Einrichtung hergestellt wird oder wenn das bestehende KGMP-Zertifikat vor seiner Verlängerung abgelaufen ist.
Regelmäßige Inspektion: Alle drei (03) Jahre wird eine regelmäßige Inspektion zur periodischen Bewertung durchgeführt, um sicherzustellen, dass Hersteller weiterhin die GMP-Standards einhalten.
Zusätzliche Inspektion: Wenn ein GMP-zertifizierter Hersteller ein Medizinprodukt einer neuen Kategorie hinzufügt und herstellt, muss es einer zusätzlichen Inspektion für die neue Produktkategorie unterzogen werden. Basierend auf dem Ergebnis der regulären Inspektion kann eine zusätzliche Inspektion entweder eine Teil- oder eine vollständige Inspektion sein. Die Gültigkeit des durch die zusätzliche Inspektion ausgestellten Zertifikats wird mit dem ursprünglich ausgestellten KGMP-Zertifikat abgestimmt.
Änderungsbewertung: Eine Bewertung wird durchgeführt, wenn der Herstellungsort geändert wird. Eine Ausnahme gilt für Lager und Labore, die einen unerheblichen Einfluss auf die Produktqualität haben.
Wie wird die KGMP-Bewertung durchgeführt?
Der Herstellungsort wird entweder einer Dokumentenprüfung oder einer Vor-Ort-Inspektion durch die Drittprüfstellen oder die MFDS unterzogen.
Dokumentenprüfung: Eine Dokumentenprüfung wird durchgeführt, wenn der Hersteller ein gültiges QMS-Zertifikat besitzt oder wenn ein gültiger Standortinspektionsbericht von zertifizierten Stellen vorliegt. Dies gilt auch, wenn ein anderer Importeur ein KGMP-Zertifikat für einen Hersteller beantragen möchte, der bereits ein gültiges KGMP-Zertifikat über einen anderen Import besitzt.
Vor-Ort-Inspektion: Eine Vor-Ort-Inspektion wird für Medizinprodukte der Klassen II, III und IV durchgeführt. Die Standortinspektion kann von Drittprüfstellen oder gemeinsam von den Drittprüfstellen und der MFDS durchgeführt werden.
Wie sind die Fristen für die Erlangung eines KGMP-Zertifikats?
Abhängig von der Korrektheit der eingereichten Unterlagen und der Vorbereitung des Herstellers auf die Vor-Ort-Inspektion stellt die MFDS das KGMP-Zertifikat innerhalb von zwei bis drei (02-03) Monaten nach Einreichung des Antrags aus. Die Frist kann sich verlängern, wenn die Prüfer während der Inspektion Fragen aufwerfen und die Hersteller möglicherweise auch länger brauchen, um diese Fragen zu beantworten.
Wie lange ist das KGMP-Zertifikat gültig?
Nach einer gründlichen Inspektion stellt die MFDS ein KGMP-Zertifikat aus, das drei (03) Jahre gültig ist und nach Ablauf dieser Frist erneuert werden muss.
Wie ist das Verfahren zur Erneuerung eines KGMP-Zertifikats?
Wenn das KGMP-Zertifikat abläuft, kann der Lizenzinhaber die Produkte importieren, darf sie aber erst vertreiben, wenn das KGMP-Zertifikat erneuert wurde. Der Antragsteller muss den Verlängerungsantrag 90 Tage vor Ablauf des KGMP-Zertifikats einreichen. Der Antrag wird von MFDS-akkreditierten Prüfern bearbeitet, und die während der dreijährigen (03) Gültigkeitsdauer des ursprünglichen Zertifikats vorgelegten Unterlagen werden überprüft. Sobald die Inspektion abgeschlossen ist, wird das KGMP-Zertifikat erneuert. Die Bewertung für die Erneuerung des KGMP-Zertifikats hängt von der Klasse der Produkte ab.
Art der Inspektion | Klasse II | Klasse III | Klasse IV |
Erstinspektion | Vor-Ort-Inspektion durch einen externen Prüfer | Gemeinsame Vor-Ort-Inspektion (Dritter und MFDS) | Gemeinsame Vor-Ort-Inspektion (Dritter und MFDS) |
Regelmäßige Inspektion | Vor-Ort-Inspektion durch einen externen Prüfer* | Vor-Ort-Inspektion durch einen externen Prüfer* | Gemeinsame Vor-Ort-Inspektion (Dritter und MFDS) |
Zusätzliche Inspektion | Dokumentenprüfung durch den Dritten | Dokumentenprüfung durch den Dritten | Dokumentenprüfung durch den Dritten |
Änderungsbewertung | Dokumentenprüfung durch den Dritten | Dokumentenprüfung durch den Dritten | Dokumentenprüfung durch den Dritten |
*Unterliegt einer gemeinsamen Inspektion bei Bedenken hinsichtlich Sicherheit und Wirksamkeit während der dreijährigen Gültigkeitsdauer.
Hersteller, die in Südkorea tätig werden möchten, müssen die von der MFDS festgelegten KGMP-Anforderungen genau verstehen. Von Herstellern wird erwartet, dass sie die detaillierten Unterlagen und den Produktionsstandort stets in Übereinstimmung mit den KGMP-Standards halten. Die Erlangung der KGMP-Zertifizierung kann für Hersteller aufgrund des strengen regulatorischen Rahmens der MFDS eine Herausforderung darstellen. Die Hersteller können einen erfahrenen regulatorischen Partner für eine geeignete Strategie und zur Erlangung eines KGMP-Zertifikats wählen.
Um mehr über Koreas Gute Herstellungspraktiken zu erfahren, wenden Sie sich an unseren regulatorischen Experten.
