Présentation de l'enregistrement des dispositifsFDA auprès deFDA US
Les États-Unis d'Amérique (USA) sont réputés pour leur marché des dispositifs médicaux fortement réglementé, caractérisé par des procédures d'enregistrement et des exigences clairement définies. La réglementation américaine initiale en matière de dispositifs médicaux remonte à 1976 et a évolué au fil du temps. Elle est gérée par le Centre for Devices and Radiological Health (CDRH), qui relève de la Food and Drug Administration (FDA). Freyr a aidé de nombreux fabricants de dispositifs médicaux à se conformer à la procédure d'enregistrement des dispositifsFDA US .

Autorité réglementaire : Agence américaine des produits alimentaires et médicamenteux (FDA)
Réglementation : Titre 21 du Code des règlements fédéraux (21 CFR) Parties 800 – 1299
Voie réglementaire : Notification préalable à la commercialisation ou Autorisation préalable à la mise sur le marché ou Classification De Novo
Représentant autorisé : Agent US
Exigence SMQ : Réglementation du Système Qualité (QSR) (21 CFR partie 820)
Évaluation des données techniques : Centre pour les dispositifs et la santé radiologique
Validité de la licence : Illimité
Exigences d'étiquetage : 21 CFR Partie 801
Format de soumission : Papier et CD/DVD
Langue : Anglais
Classification des dispositifs médicaux aux ÉTATS-UNIS
FDA les dispositifs médicaux en trois catégories en fonction du risque : la classe I, la classe II et la classe III. Les dispositifs de classe I sont considérés comme présentant un faible risque, tandis que ceux de classe III sont associés à un risque élevé. Les exigences et les procédures d'enregistrement varient en fonction de la classe du dispositif.
| Classe de dispositif | Risque | Voie d'enregistrement pour approbation |
|---|---|---|
| I | Faible risque | Exempté 510(k) |
| II | Risque modéré (Avec dispositif de référence) | Notification précommercialisation / 510(k) |
Risque modéré (Sans dispositif de référence) | Demande De Novo | |
| III | Risque élevé | Approbation précommercialisation (PMA) |
FDA américaine
Les entreprises qui ne disposent pas de bureaux locaux aux États-Unis doivent désigner un FDA FDA FDA pour représenter le fabricant. Cet FDA doit soit résider aux États-Unis, soit disposer d'un établissement aux États-Unis. Les responsabilités qui incombent à l'agent sont définies par laFDA US FDA le cadre de la réglementation du Code of Federal Regulations (CFR).
Parcourez la Foire aux questions (FAQ) concernant l'agent US.
Réunions interactives avec laFDA US
FDA US FDA les fabricants par le biais de différentes réunions de type «Q-Submission »visant à atteindre divers objectifs. Ces réunions avec l'agence, organisées avant le lancement ou pendant le développement du dispositif, et avant le dépôt des demandes d'enregistrement de dispositifsFDA US FDA , aident les fabricants à optimiser les délais et les coûts liés à la commercialisation de leurs dispositifs.
Enregistrement des dispositifs médicaux aux ÉTATS-UNIS
Ces dispositifs peuvent être homologués par le CDRH (Centre pour les dispositifs médicaux) de FDA l'une des différentes voies d'enregistrement. Ils sont répertoriés comme suit :
Dispositifs médicaux de classe I :Les dispositifs de classe I sont généralement exemptés des exigences relatives aux bonnes pratiques de fabrication (BPF) et de la procédure de notification 510(k)FDA aux US ne nécessite donc pas d'autorisation préalable de laFDA . Le fabricant doit toutefois se conformer à d'autres exigences, telles que l'enregistrement de l'établissement, l'enregistrement du dispositif, l'identification unique des dispositifs (UDI), le système de surveillance post-commercialisation (PMS), etc.
Dispositifs médicaux de classe II :les dispositifs à risque moyen disposant de dispositifs de référence approuvés au titre de la procédure 510(k) peuvent opter pour la notification préalable à la mise sur le marché (PMN) 510(k), également appeléeenregistrement 510(k). Le dispositif concerné doit établir une équivalence substantielle (SE) avec les dispositifs de référence identifiés et revendiqués. Cette voie est la plus couramment utilisée pour l'enregistrement des dispositifs aux États-Unis. Les fabricants de dispositifs à risque moyen ne disposant pas de dispositifs de référence peuvent demander une classification auprès de laFDA US FDA demandes De Novo.
Dispositifs médicaux de classe III :les fabricants de dispositifs de classe III à haut risque doivent déposer une demande d'autorisation préalable à la mise sur le marché (PMA) auprès de laFDAUS . Les dispositifs doivent faire l'objet d'une évaluation clinique approfondie et le fabricant doit fournir des données détaillées sur la sécurité et l'efficacité issues d'études cliniques. LaFDA US FDA une inspection du système de gestion de la qualité dans le cadre de l'évaluation avant de délivrerl'autorisation préalable à la mise sur le marchépour le dispositif.
Enregistrements de dispositifs médicaux non-CDRH
Selon les indications d'utilisation, certains produits frontières considérés comme des dispositifs médicaux dans d'autres pays, tels que les respirateurs chirurgicaux, les désinfectants et les produits combinés, impliquent d'autres agences comme le Centre de contrôle des maladies (CDC), l'Institut national pour la sécurité et la santé au travail (NIOSH), l'Agence de protection de l'environnement (EPA), le Centre d'évaluation et de recherche biologique (CBER) et le Centre d'évaluation et de recherche sur les médicaments (CDER).
Exigences de conformité post-approbation pour les dispositifs médicaux
Tous les fabricants de dispositifs doivent se conformer aux exigences post-approbation énumérées ci-dessous :
- Exigence d'enregistrement et de référencement: Les établissements de toutes les classes de dispositifs doivent être enregistrés dans la base de données FURLs et le dispositif doit être référencé après l'obtention de l'approbation et avant sa commercialisation aux US. Certains dispositifs, tels que les dispositifs à rayonnement, doivent se conformer à d'autres exigences, comme un numéro d'accès, avant de pouvoir être importés aux US.
- Identification unique des dispositifs : Toutes les classes de dispositifs doivent se conformer aux réglementations relatives à l'identification unique des dispositifs (UDI) pour commercialiser les dispositifs aux US.
- Frais d'ouverture: Le fabricant doit s'acquitter des frais annuels d'enregistrement afin de maintenir son enregistrement actif et de pouvoir continuer à commercialiser des dispositifs aux États-Unis. LaFDA US FDA réduit la structure tarifaire pour les petites entités titulaires d'un certificat de petite entreprise en cours de validité.
- Audits qualité: Pourles dispositifs qui ne sont pas exemptés des BPF, la FDA US FDA inspecter l'établissement de fabrication à tout moment afin de vérifier la conformité aux réglementations relatives aux systèmes qualité (QSR) conformément au 21 CFR 820.
Flux de processus
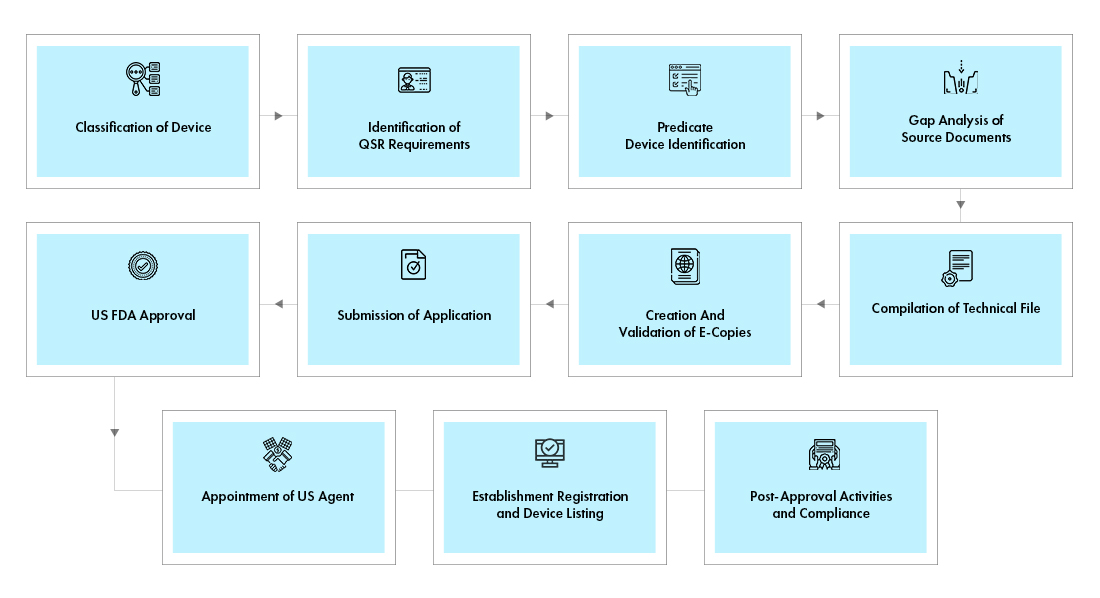
Gestion du cycle de vie des dispositifs post-approbation
Freyr accompagne les fabricants étrangers dans la gestion End-to-end du cycle de vie des dispositifs médicaux, y compris les activités post-approbation, telles que :
- Gestion des changements post-approbation – modifications aux approbations existantes de dispositifs médicaux, telles que l'ajout de nouvelles variantes, d'accessoires ; l'ajout de nouvelles indications d'utilisation, entre autres
- Maintien des autorisations et des enregistrements grâce au paiement en temps voulu des redevances MDUFA à la FDA
- Assurer la liaison entre laFDA US FDA le fabricant
Freyr dispose d'un centre de livraison exclusif aux US avec une équipe professionnelle pour fournir un soutien réglementaire aux fabricants afin de maintenir la qualité et la sécurité nécessaires à l'approbation. Les experts en veille de Freyr observent attentivement les mises à jour réglementaires et informent les clients des mesures à prendre pour la conformité des produits avec la norme actuelle.
Résumé
| Risque | Classe de dispositif | Audit du SGC | Disponibilité du produit de référence | Voie réglementaire | US Agent | US FDA |
|---|---|---|---|---|---|---|
| Faible risque | I | Non | NA | Exempté | Oui | 1 mois |
| Risque moyen | II | Oui (après approbation) | Oui | PMN/510(k) | Oui | 9 à 12 Mois |
| Risque moyen | II | Oui (après approbation) | Non | Demande de classification De Novo | Oui | 18 - 30 Mois |
| Risque élevé | III | Oui (avant approbation) | NA | PMA | Oui | 18 - 30 Mois |
Les services d'enregistrement de dispositifs médicaux de Freyr
L'expertise de Freyr
- Diligence raisonnable réglementaire
- Documentation relative aux appareils
- Soutien 513(g)
- Enregistrement 510(k)
- Demande De Novo de classification
- Enregistrement PMA
- 21 CFR 820 conformité
- Soutien aux audits BIMO
- MDSAP Conformité
- Support d'étiquetage
- Support à la publication et à la soumission
- Agent US
- Réunions de soumission Q
- Réunions RFD et Pré-RFD
- Certification des petites entreprises
- Enregistrement de l'établissement et enregistrement des dispositifs
- Conformité réglementaire pour les dispositifs médicaux à rayonnement
- Gestion des changements post-approbation
- Surveillance post-commercialisation
- Conformité UDI
- Conseil réglementaire pour la résolution des déficiences