
Regulatorische Einreichungen und Veröffentlichungsaufgaben waren traditionell aufwendig und erforderten stundenlange manuelle Arbeit für die Formatierung von Dokumenten, die Erstellung behördenkonformer PDFs, Qualitätskontrollen und das Zusammenstellen von Dokumenten für Einreichungen. Angesichts der engen Fristen sind Life-Science-Unternehmen stets bestrebt, Einreichungen pünktlich vorzunehmen. Weltweit bereiten sich die Regulierungsbehörden darauf vor, neue Entwicklungen wie eCTD v4.0 für Dossiereinreichungen, Änderungen und andere Berichte zu übernehmen. eCTD v4.0 ist eine schrittweise Änderung, die voraussichtlich die Zukunft der regulatorischen Einreichungen beeinflussen wird, wobei sich jedes Land darauf vorbereitet, sie zu akzeptieren und umzusetzen.
Angesichts all der Herausforderungen im Zusammenhang mit regulatorischen Einreichungen ist eine technologisch fortschrittliche Lösung erforderlich, um den Prozess der Arzneimitteleinreichung und -prüfung zu beschleunigen. Da Unternehmen bereits erwägen, die Automatisierung zu einem integralen Bestandteil des regulatorischen Einreichungsprozesses zu machen, ist es entscheidend zu überlegen, wie sie die Produktivität beim Übergang zu eCTD 4.0 steigern kann.
Wie die Automatisierung den Übergang zu eCTD 4.0 unterstützt?
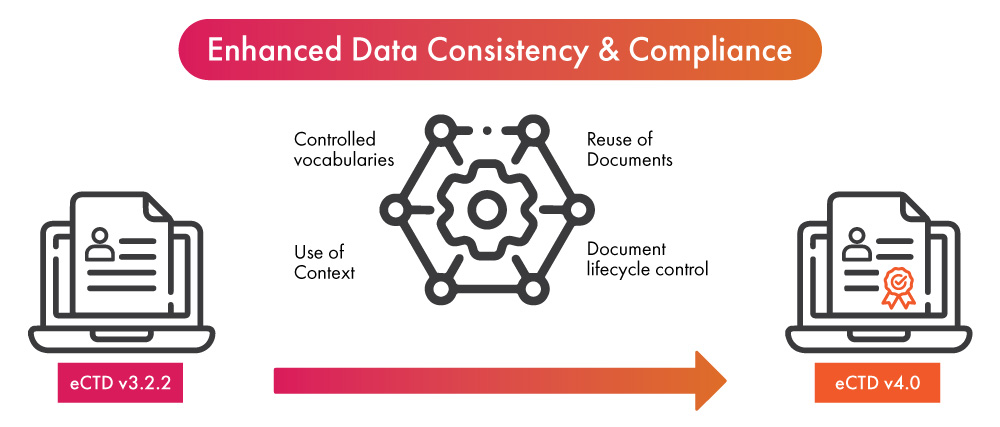
- An der Schwelle zur Einführung der neuesten Version des eCTD kann der Einsatz von Automatisierung im regulatorischen Einreichungsprozess doppelte Vorteile für Life-Science-Unternehmen bringen: Einerseits wird die Einhaltung von eCTD v4.0 schneller sichergestellt, andererseits werden die Datenkonsistenz und die Optimierung des Einreichungsprozesses verbessert.
- Sobald die Daten für eine regulatorische Einreichung finalisiert wurden, ermöglicht die Automatisierung, dass diese Daten in andere Einreichungen oder Aktualisierungen übernommen werden. Dies nutzt die neue Funktion in eCTD v4.0, die jetzt Many-to-One- und Many-to-Many-Datenersetzungen ermöglicht und somit die Wiederverwendung von Daten auf vereinfachte Weise erlaubt.
- Automatisierte Benachrichtigungen machen es überflüssig, Nachrichten zu übermitteln oder Anrufe zu tätigen, wenn eine Aktivität erforderlich ist. Dies ermöglicht eine schnellere, klarere Kommunikation, die zu kontrollierten Vokabularen führt – einem wesentlichen Bestandteil von eCTD v4.0.
- Die Automatisierung bei der Dokumenteneinreichung wird dazu beitragen, den Prozess der Aktualisierung bereits eingereichter Inhalte weiter zu vereinfachen. Sie wird die Lebenszykluskontrolle der eingereichten Dokumente verbessern.
- Die Automatisierung in Kontextgruppen kann den Prozess der Organisation mehrerer Dateien, die für regulatorische Einreichungen vorgesehen sind, beschleunigen.
Angesichts des Übergangs zu eCTD v4.0 ist es für Life-Science-Organisationen entscheidend, mit Anbietern zusammenzuarbeiten, die auf den neuen Standard vorbereitet sind und verstehen, wie der regulatorische Veröffentlichungsprozess automatisiert und optimiert werden kann. Unternehmen müssen sich darauf einstellen, die neuesten Technologien, die durch Automatisierung ermöglicht werden, zu übernehmen, um erhebliche Vorteile und einen Wettbewerbsvorteil auf dem Markt zu erzielen. eCTD v4.0 ist eine große Veränderung, die nach langer Zeit eintritt. Organisationen sollten mit einem Proof of Concept beginnen, um erste Erfahrungen zu sammeln, da es bald in vielen Ländern weltweit akzeptiert wird, abhängig von den jeweiligen nationalen Zeitplänen.
Wir bei Freyr sind führend bei der Förderung von Innovationen durch Technologie und sind darauf ausgerichtet, unsere Kunden zu unterstützen, indem wir unsere Software für regulatorische Einreichungen und Veröffentlichungen – Freyr SUBMIT PRO – eCTD v4.0-fähig machen.
Um mehr über Frey's Bereitschaft für eCTD 4.0 zu erfahren, klicken Sie bitte hier, um die archivierte Webinar-Sitzung herunterzuladen.









