
Für die meisten Regulatory-Affairs-Teams ist die Verlängerung einer Zulassung nicht nur ein weiterer administrativer Meilenstein. Es ist der Moment, in dem jahrelange Qualitätsaufzeichnungen, Daten aus der Zeit nach der Markteinführung und Änderungshistorien unter behördlicher Prüfung zusammenlaufen.
Dennoch werden Vertragsverlängerungen oft nur reaktiv angegangen.
Die Dateien werden erst spät zusammengestellt. Die PMS-Daten befinden sich in verschiedenen Ordnern. Zertifikate werden in Tabellenkalkulationen erfasst. Und plötzlich wird aus einem eigentlich strukturierten Prozess ein Wettlauf gegen die Zeit.
Die Verlängerung von Medizinproduktzulassungen scheitert nicht daran, dass die Teams sich nicht genug bemühen. Sie scheitert daran, dass mit der Planung der Verlängerung zu kurz vor Ablauf begonnen wird.
Eine solide Verlängerungsstrategie ändert dies. Sie betrachtet die Verlängerung als einen fortlaufenden Prozess im Lebenszyklus und nicht als eine in letzter Minute erledigte Formalität.
Schauen wir uns einmal genauer an, was das für RA konkret bedeutet.
Warum die Verlängerung von Medizinproduktzulassungen eine Strategie erfordert
Die meisten Gerätezulassungen sind je nach Markt 3 bis 5 Jahre gültig. In einigen Regionen erfolgt eine jährliche Verlängerung, während in anderen Regionen Abonnementmodelle mit regelmäßigen Zahlungen gelten. Unabhängig von der Struktur darf das Gerät nach Ablauf der Lizenz nicht mehr legal hergestellt, importiert oder vertrieben werden.
Verlängerungsanträge sind mit einem hohen Risiko verbunden, da die Behörden eine Neubewertung vornehmen:
- Entwicklung nach der Markteinführung
- Entwicklungen bei Beschwerden und unerwünschten Ereignissen
- Änderungen im Fertigungs- und Qualitätssicherungssystem
- Klinische Daten und Sicherheitsdaten
- Historie der Einhaltung regulatorischer Vorschriften
In vielen Regionen, darunter Indien und die EU, erwarten die Aufsichtsbehörden im Rahmen der Verlängerungsprüfung konsolidierte PMS-Daten, Nachweise über Korrektur- und Vorbeugungsmaßnahmen (CAPA) sowie eine aktualisierte technische Dokumentation.
Aus diesem Grund sollte die Erneuerung als eine operative Disziplin betrachtet werden, die sich über den gesamten Produktlebenszyklus erstreckt.
Nicht als Aufgabe, bei der es auf die Einhaltung von Fristen ankommt.
Beginnen Sie mit einem Zulassungskalender – Ihrer ersten Verteidigungslinie
Einer der häufigsten Gründe für fehlgeschlagene Vertragsverlängerungen ist eine uneinheitliche Nachverfolgung. Unterschiedliche Märkte. Unterschiedliche Zeitpläne. Unterschiedliche Anforderungen.
Ein zentraler Regulierungs-Kalender sollte Folgendes enthalten:
- Zertifikatsnummern und Ablaufdaten nach Land
- Fristen für die Einreichung von Verlängerungsanträgen
- Fristen für die Einbehaltung von Honoraren
- Gültigkeit der ISO 13485 CE-Zertifikate
- Interne Meilensteine (12 Monate, 6 Monate, 3 Monate vor Vertragsverlängerung)
Aus praktischer RA sollte die Planung mindestens 12 Monate vor Ablauf beginnen.
Viele Teams nutzen mittlerweile einheitliche RIMS-Plattformen, um einen einheitlichen Überblick über den Registrierungsstatus in allen Märkten zu erhalten. Dies hilft dabei, die Abhängigkeit von Tabellenkalkulationen zu vermeiden und gleichzeitig die Fristen für Verlängerungen übersichtlich und umsetzbar zu halten.
freya fusion das erste Produkt seiner Art, das Unternehmen eine zentrale Datenquelle für alle ihre Compliance-bezogenen Daten bietet.
Die wichtigsten Unterlagen, die Sie immer benötigen
Die Unterlagen für die Verlängerung entsprechen weitgehend denen der Erstregistrierung, legen jedoch einen zusätzlichen Schwerpunkt auf Kontinuität und Leistung.
Die meisten Behörden gehen davon aus, dass:
- Anschreiben, in dem die Absicht zur Verlängerung klar zum Ausdruck gebracht wird
- Erklärung über die fortdauernde Konformität (Herstellung, Konstruktion, Eigentumsverhältnisse)
- Aktualisierte Gerätestammdaten und Werksstammdaten (falls zutreffend)
- Gültiges ISO 13485
- CE-Zertifikate oder Qualitätssicherungszertifikate, sofern erforderlich
- Herstellungslizenzen und GMP-Nachweise
- Konformitätserklärung
- Chronologie der behördlichen Korrespondenz
Änderungen während der Gültigkeitsdauer müssen bereits über die vorgeschriebenen Verfahren nach der Zulassung gemeldet werden. Nicht gemeldete Änderungen sind einer der schnellsten Wege, um Fragen seitens der Aufsichtsbehörden auf sich zu ziehen.
Hier kommt es auf ein strukturiertes Dokumentenmanagement an. RA profitieren davon, wenn alle Einreichungen, Überarbeitungen und Genehmigungen in einer einzigen kontrollierten Umgebung gespeichert sind, anstatt über verschiedene Laufwerke und Posteingänge verstreut zu sein.
Die Marktüberwachung ist das Herzstück der Verlängerung
Wenn es einen Bereich gibt, den die Aufsichtsbehörden bei der Verlängerung genau unter die Lupe nehmen sollten, dann ist es die Überwachung nach dem Inverkehrbringen.
Die Behörden erwarten den Nachweis, dass das Gerät im praktischen Einsatz weiterhin sicher und wirksam funktioniert.
In der Regel umfasst dies:
- Verkaufszahlen nach Jahr und Gerätemodell
- Beschwerdeverzeichnisse und Meldungen über unerwünschte Ereignisse
- Ursachenanalyse für jedes Problem
- CAPA-Aufzeichnungen mit Nachweis der Schließung
- Rückrufhistorie (global und länderspezifisch)
- Trendanalyse über den gesamten Gültigkeitszeitraum
Bei Geräten mit höherem Risiko kann außerdem Folgendes erforderlich sein:
- PMS-Berichte
- Aktualisierungen des klinischen Bewertungsberichts
- PMCF
- Regelmäßige Sicherheitsberichte
Gute Ergebnisse bei der Vertragsverlängerung hängen davon ab, wie konsequent diese Daten im Laufe der Zeit erfasst werden, und nicht davon, wie gut sie am Ende zusammengestellt werden.
Viele RA integrieren die PMS-Nachverfolgung mittlerweile mithilfe einheitlicher Plattformen wie freya fusion direkt in ihre regulatorischen Arbeitsabläufe, sodass Beschwerden, CAPAs und Zulassungen miteinander verknüpft bleiben und sich während der Vorbereitung von Verlängerungen leichter nachverfolgen lassen.
Richten Sie Ihr Qualitätssystem auf die Bereitschaft zur Erneuerung aus
Ihr QMS ist nicht von der Erneuerung zu trennen. Es bildet die Grundlage für die Erneuerung.
Die Aufsichtsbehörden suchen nach Belegen in wichtigen Bereichen wie:
- Dokumentenverwaltung und Versionshistorie
- Change Management für Fertigung, Etikettierung und Verpackung
- Lieferantenqualifizierung und -audits
- Beschwerdebearbeitung und Trendanalyse
- Wirksamkeit von CAPA
- Interne Prüfungen
- Ausbildungs- und Kompetenznachweise
Ein praktischer Ansatz besteht darin, etwa sechs Monate vor der Einreichung eine Lückenanalyse im Vorfeld der Verlängerung durchzuführen:
- Stellen Sie sicher, dass die Zertifikate nach der Überprüfung weiterhin gültig bleiben
- Vollständigkeit der PMS-Daten überprüfen
- CAPA-Schließungen prüfen
- Änderungsprotokolle einsehen
- Stellen Sie sicher, dass die Schulungsunterlagen auf dem neuesten Stand sind
Diese proaktive Prüfung verhindert oft Korrekturmaßnahmen in letzter Minute.
Planen Sie frühzeitig für die Komplexität mehrerer Märkte
Verlängerungen finden selten isoliert statt. An globalen Portfolios sind verschiedene Vertreter, Vertriebspartner, benannte Stellen und Behörden beteiligt.
Die Koordination umfasst in der Regel:
- Hersteller, der technische Unterlagen und PMS-Daten bereitstellt
- Lokale Stellen, die Anträge und Lizenzen bearbeiten
- Vertriebspartner, die Umsatz- und Reklamationsdaten austauschen
- Benannte Stellen, die Prüfbescheinigungen ausstellen
Ohne klare Zuständigkeiten und Zeitpläne häufen sich die Verzögerungen.
Ein zentralisiertes System, das landesspezifische Anforderungen, den Status von Einreichungen und die Kommunikation mit den Aufsichtsbehörden nachverfolgt, kann den Verwaltungsaufwand erheblich reduzieren. Hier freya fusion RA , indem es Zulassungsanträge, Dokumente und die Zusammenarbeit mit den Beteiligten in einem einheitlichen Arbeitsbereich für Zulassungsangelegenheiten zusammenführt.
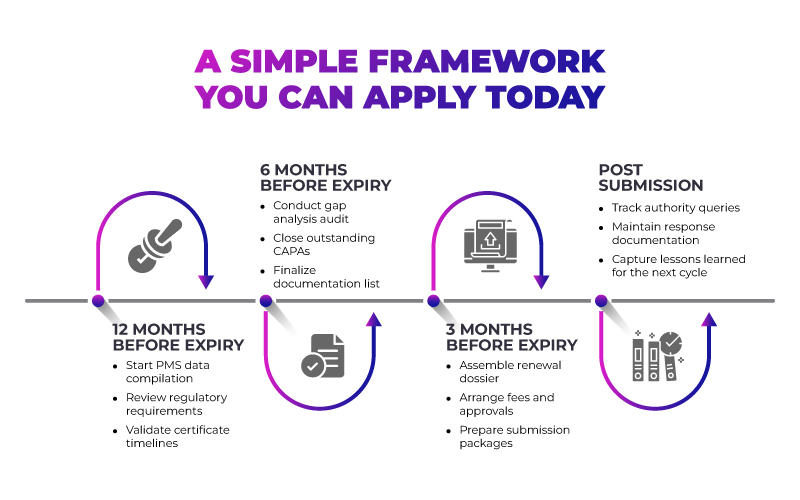
Durch dieses schrittweise Vorgehen wird die Verlängerung zu einem planbaren Prozess und nicht zu einer immer wiederkehrenden Krise.
Bei der Erneuerung geht es um Kontinuität, nicht nur um die Einhaltung von Vorschriften
Bei der Verlängerung der Zulassung von Medizinprodukten geht es letztlich darum, einen ununterbrochenen Marktzugang zu sichern. Bei strategischer Umsetzung stärkt dies die Qualitätssicherungssysteme, verbessert die Einhaltung der Post-Market-Surveillance-Vorschriften und schafft Vertrauen bei den Aufsichtsbehörden.
RA leisten bereits jeden Tag harte Arbeit. Die Herausforderung besteht darin, dieser Arbeit Struktur, Sichtbarkeit und Kontinuität zu verleihen.
Hier kommen Plattformen wie freya fusion ins Spiel. Durch die Zusammenführung von Zulassungen, Dokumenten, PMS und Zusammenarbeit unterstützt sie RA dabei, von reaktiven Verlängerungen zu einem proaktiven Management des regulatorischen Lebenszyklus überzugehen.
Sind Sie bereit, die Verlängerung Ihrer Medizinproduktzulassungen zu vereinfachen?
Wenn Ihnen die Verlängerung von Lizenzen immer noch zersplittert, manuell oder stressig erscheint, ist es vielleicht an der Zeit, die Struktur Ihrer regulatorischen Abläufe zu überdenken.
Sehen Sie, wie freya fusionmit seinen AI-First-Funktionen RA für Medizinprodukte durch zentralisierte Registrierungsverfolgung, Dokumentenkontrolle und Transparenz über den gesamten Lebenszyklus unterstützt – allesamt speziell für Fachleute im Bereich Regulatory Affairs entwickelt, nicht für IT-Teams.
Vereinbaren Sie noch heute eine Vorführung und machen Sie den ersten Schritt hin zu neuem Vertrauen, kontinuierlicher Compliance und reibungsloser Marktkontinuität.









