
Zusätzlich zur Vervollständigung der erforderlichen xEVMPD-Datenübermittlungen müssen Life-Science-Organisationen nun ein webbasiertes Antragsformular namens Digital Application Dataset Integration (DADI) verwenden. Die Europäische Arzneimittel-Agentur (EMA) hat DADI als langfristigen Ersatz für das PDF-basierte elektronische Antragsformular (eAF) konzipiert, das zur Unterstützung von eCTD-Einreichungen eingeführt wurde.
Die Zeitpläne für diesen Übergang wurden kürzlich von der EMA veröffentlicht. DADI wird im Jahr 2022 das Formular für Änderungen von Arzneimitteln ersetzen. Andere Einreichungsformulare für zentral zugelassene Produkte (CAP) und national zugelassene Produkte (NAP) werden bis 2023 folgen. Das Projekt wird auch Formulare ersetzen, die für die wichtigsten EU-Verfahren verwendet werden, darunter das zentralisierte Verfahren (CP), das Verfahren der gegenseitigen Anerkennung (MRP), das dezentralisierte Verfahren (DCP) und das nationale Verfahren (NP).
Die Webformulare (einschließlich des Human Variations Form (HVF) für Humanarzneimittel) werden die Eingaben für eAFs vereinheitlichen, um standardisierte Produktstammdaten für Arzneimittel bereitzustellen. Sie ermöglichen sowohl die bestehende menschenlesbare als auch die neue maschinenlesbare Ausgabe für die digitale Verarbeitung, basierend auf dem Fast Healthcare Interoperability Resources (FHIR)-Datenaustauschstandard für Arzneimittel. Sie werden auch bestehende Produktstammdaten aus den Product Management Services (PMS) verwenden, um die Formularfelder, wo zutreffend, vorab auszufüllen.
Die webbasierten DADI-Formulare sollen eine methodischere Bearbeitung eines Antrags ermöglichen und so den Arbeitsaufwand der Organisation reduzieren. Zum Beispiel werden Fehler und Unstimmigkeiten reduziert, da die Formulare die genaue Prüfung eingereichter Anträge durch die Gesundheitsbehörden unterstützen. Die Formulare werden auch den Weg für „first-time-right“-Daten ebnen, die in Datenbanken eingespeist werden, wodurch die Systemintegration und der Datenaustausch zwischen den Gesundheitsbehörden mühelos werden. Darüber hinaus werden die neuen Formulare die veraltete Technologie ersetzen.
Vorteile von DADI
Das Ziel von DADI und dieser datengesteuerten Transformation regulatorischer Prozesse lässt sich wie folgt zusammenfassen:
- Zur Steigerung der Effizienz in den Bereichen Regulierung, F&E und Fertigung
- Um schneller mit Gesundheitsbehörden zu kommunizieren
- Um eine datengesteuerte Entscheidungsfindung für Unternehmen und Behörden zu ermöglichen
- Um bessere Einblicke sowie Voraussicht bezüglich Geschäftsergebnissen und Gesamtleistung zu erhalten
Ganzheitlich betrachtet soll dies Patienten, Regulierungsbehörden sowie der Industrie zugutekommen.
Neueste Zeitplanänderungen der EMA
- Der Starttermin für HVFs wurde vom ursprünglich festgelegten April 2022 auf Oktober 2022 verschoben.
- Derzeit wird die HVF einem geschlossenen Benutzerakzeptanztest (UAT) von einer Gruppe von Fachexperten für DADI unterzogen.
- Anschließend findet im zweiten Quartal 2022 ein integrierter UAT mit einer größeren Gruppe verschiedener Interessengruppen statt.
- Sobald es in Betrieb genommen wird, wird es eine sechs (06)-monatige Übergangsphase geben, in der sowohl die eAFs (alte PDF-Version) als auch die webbasierten Formulare parallel akzeptiert werden. Danach wird nur noch die HVF akzeptiert.
Bitte beachten Sie die folgende Infografik für die Zeitpläne zur HVF-Implementierung (Aktualisiert im Februar 2022, Änderungen durch die EMA vorbehalten):
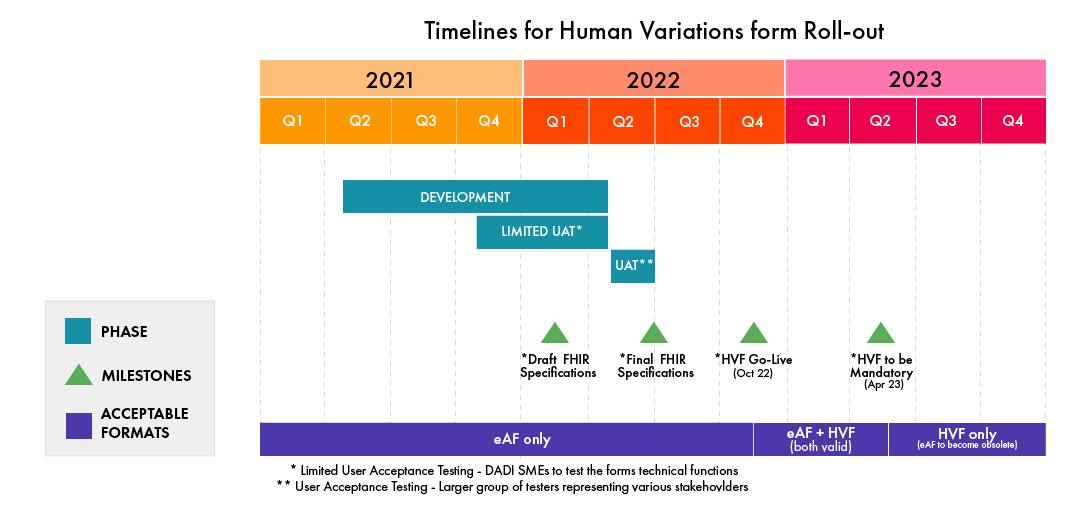
(Quelle: EMA)
Anpassungsfähigkeit an das dynamische regulatorische Umfeld sicherstellen
Alle wichtigen Gesundheitsbehörden gehen nun dazu über, hochwertige Datensätze und Dokumente einzureichen. Für Organisationen ist es wichtig, diese in einem einheitlichen System zu pflegen.
Es ist auch entscheidend, ein klares Verständnis des gesamten Einreichungslebenszyklus zu haben – seiner Anforderungen, der damit verbundenen Personen und Prozesse sowie des aktuellen Standorts der Quelldaten durch eine gründliche Bedarfsanalyse. Datenbereinigung und -anreicherung müssen vorrangig behandelt werden, wenn die Analyse einen Bedarf aufzeigt.
Es ist unerlässlich, über ein Regulatory Information Management System (RIMS) zu verfügen, das sich an sich entwickelnde Vorschriften und Richtlinien anpasst, flexibel ist, um die aktuellen Bedürfnisse der Organisation neu zu gestalten, und dem dynamischen regulatorischen Umfeld entspricht. Um mehr über Frey's Suite regulatorischer Lösungen zu erfahren, die Ihre Organisation auf DADI und weitere solche Prozessänderungen vorbereitet, besuchen Sie uns unter Freyr Digital.









