
Die Einführung von eCTD 4.0 stellt einen entscheidenden Schritt zur Modernisierung regulatorischer Einreichungen weltweit dar. Mit Vorteilen wie verbesserter Dokumentenverfolgung und Metadata-gesteuerten Effizienzen ist es keine Überraschung, dass globale Behörden diesen Wandel begrüßen.
Doch wo steht die EMA? Im Gegensatz zur FDA, die klare Implementierungsphasen dargelegt hat, verfolgt die EMA einen bedachteren Ansatz, beginnend mit Pilotprogrammen und technischen Evaluierungen. In diesem Blog erläutern wir die Pläne der EMA für eCTD 4.0, deren potenzielle Auswirkungen auf regulatorische Einreichungen und wie Ihr Unternehmen die Nase vorn behalten kann.
Noch wichtiger ist: Hat die EMA eCTD 4.0 bereits vorgeschrieben? Lassen Sie uns eintauchen.
Was ist eCTD 4.0 und wie unterscheidet es sich von eCTD 3.2.2?
Das Electronic Common Technical Document (eCTD) ist das international anerkannte Format für regulatorische Einreichungen. Es standardisiert die Art und Weise, wie Pharmaunternehmen Arzneimittelanträge einreichen und Lebenszyklus-Updates über verschiedene Märkte hinweg verwalten.
Die aktuelle Version, eCTD 3.2.2, ist seit Jahren in Gebrauch. Regulierungsbehörden, einschließlich der EMA, haben jedoch auf eCTD 4.0 hingearbeitet, das auf dem Health Level 7 (HL7) Regulated Product Submission (RPS) Standard basiert. Dieses Update verbessert die Effizienz der Einreichungen und das Management des regulatorischen Lebenszyklus.
Wesentliche Unterschiede zwischen eCTD 3.2.2 und eCTD 4.0:
- Besseres Lebenszyklusmanagement: Verbesserte Nachverfolgung von Dokumentenversionen, Reduzierung von Duplikaten.
- Flexiblere Granularität: Ermöglicht die Wiederverwendung strukturierter Dokumente für verschiedene Einreichungen.
- Verbesserte Metadata-Verarbeitung: Strukturiertere Metadata, die regulatorische Interaktionen reibungsloser gestalten.
- Höhere Interoperabilität: Entwickelt für eine bessere Zusammenarbeit mit sich entwickelnden digitalen Regulierungssystemen weltweit.
- Obwohl diese Änderungen zahlreiche Vorteile bieten, erfordert der Übergang zu eCTD 4.0 Vorbereitung, Investitionen und ein Verständnis der regulatorischen Erwartungen.
Standpunkt der EMA zur Einführung von eCTD 4.0
Die große Frage, die sich alle stellen, ist: Hat die EMA eCTD 4.0 vorgeschrieben? Die Antwort lautet: noch nicht, aber der Übergang ist im Gange.
Aktueller Status von eCTD 4.0 in der EU:
- Derzeit bleibt eCTD 3.2.2 der verbindliche Standard für Einreichungen in der EU.
- Die EMA hat eCTD 4.0 aktiv bewertet, dessen Nutzung jedoch noch nicht offiziell vorgeschrieben.
- Die Agentur arbeitet mit anderen Regulierungsbehörden wie der FDA und der japanischen PMDA zusammen, um globale Standards anzugleichen.
- Es wurden keine offiziellen Übergangsfristen festgelegt, aber die EMA hat angedeutet, dass eCTD 4.0 letztendlich verpflichtend wird.
Der Ansatz der EMA: Gestaffelte Einführung mit einem Pilotprogramm
Im Gegensatz zur USFDA, die einen gestaffelten Implementierungsplan vorgestellt hat, verfolgt die EMA einen strukturierten Ansatz. Die Agentur hat ein technisches Pilotprogramm gestartet, um die Implementierung von eCTD 4.0 mit Branchenakteuren zu testen.
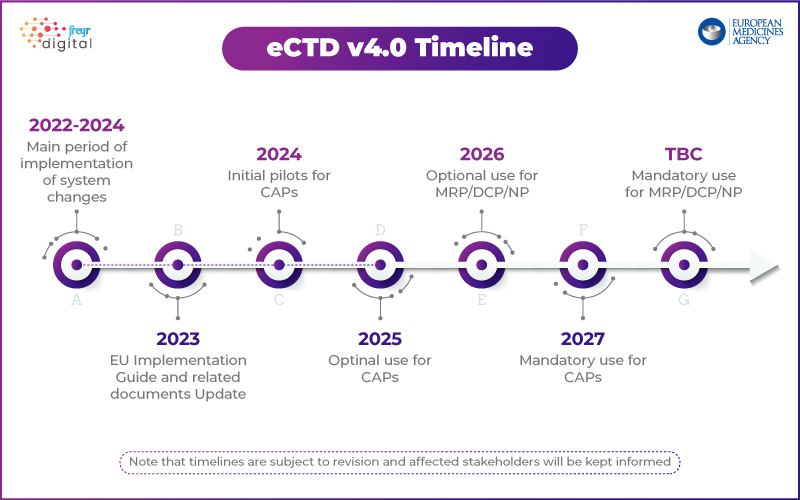
Wichtige Punkte der eCTD 4.0-Strategie der EMA:
- Schritt 1: Fokus auf technische Interoperabilität mit regulatorischen Tools.
- Zukünftige Phasen: Test-Einreichungen, Lebenszyklusmanagement und gebündelte Einreichungen.
- Ein Entwurf des Implementierungspakets ist mit kontrollierten Vokabularen und Validierungskriterien verfügbar.
Die EMA ist bestrebt, einen reibungslosen Übergang zu gewährleisten, und Life-Science-Unternehmen sollten Aktualisierungen auf der offiziellen EMA eCTD-Seite verfolgen.
Herausforderungen & Überlegungen für Life-Sciences-Unternehmen
Obwohl eCTD 4.0 klare Vorteile bietet, ist die Einführung nicht ohne Herausforderungen. Hier sind einige wichtige Überlegungen für Pharma- und Biotech-Unternehmen:
- Regulatorische Komplexitäten
- Der schrittweise Übergang der EMA bedeutet, dass Unternehmen auf duale Einreichungsprozesse (eCTD 3.2.2 und eCTD 4.0) vorbereitet sein müssen.
- Verschiedene Regionen werden unterschiedliche Einführungszeitpläne haben, was von Unternehmen Agilität erfordert.
- Technische Herausforderungen
- Die Datenmigration von eCTD 3.2.2 auf 4.0 erfordert sorgfältige Planung.
- Validierungsregeln werden sich erheblich ändern, was aktualisierte Software und Tools erfordert.
- Unternehmen müssen in Automatisierungs- und KI-gesteuerte Lösungen investieren, um die Einhaltung der Vorschriften zu gewährleisten.
- Compliance-Risiken
- Eine falsche Metadata-Zuordnung oder die Nichteinhaltung neuer Anforderungen an die Dokumentengranularität könnte zur Ablehnung der Einreichung führen.
- Regulierungsteams benötigen eine angemessene Schulung, um die neuen Validierungsregeln zu verstehen.
- Auswirkungen auf bestehende Arbeitsabläufe
- Unternehmen müssen interne Prozesse anpassen, um eCTD 4.0 zu berücksichtigen.
- Eine verstärkte Zusammenarbeit zwischen den Regulierungs-, IT- und Einreichungsteams wird notwendig sein.
Die wichtigste Erkenntnis? Unternehmen müssen jetzt mit den Vorbereitungen beginnen, obwohl die EMA eCTD 4.0 noch nicht vorgeschrieben hat.
Wie sich Unternehmen auf den Übergang der EMA zu eCTD 4.0 vorbereiten können
Obwohl die EMA noch keine offizielle Frist festgelegt hat, werden vorausschauende Unternehmen von einer frühzeitigen Vorbereitung profitieren. Hier erfahren Sie, wie:
- Aktuelle Einreichungsprozesse bewerten
- Lücken in bestehenden eCTD 3.2.2 Arbeitsabläufen identifizieren.
- Bewerten Sie, wie neue Lebenszyklusmanagement-Regeln laufende Einreichungen beeinflussen werden.
- Investieren Sie in die richtigen eCTD 4.0 Tools
- Wählen Sie eine Software für regulatorische Einreichungen, die eCTD 4.0-konform ist.
- Stellen Sie sicher, dass die Software HL7 RPS-Standards und die Automatisierung von Metadata unterstützt.
- Schulen Sie Regulierungs- und IT-Teams
- Veranstalten Sie Workshops und Schulungen zu den Änderungen von eCTD 4.0.
- Stellen Sie Richtlinien für das Tagging von Metadata und die Verfolgung des Lebenszyklus bereit.
- Tauschen Sie sich mit der EMA und Branchenkollegen aus
- Nehmen Sie an den Pilotprogrammen und regulatorischen Konsultationen der EMA teil.
- Bleiben Sie über die neuesten Leitlinien und regulatorischen Aktualisierungen der EMA auf dem Laufenden.
- Führen Sie Tests und Validierungen durch
- Führen Sie interne Testeinreichungen unter Verwendung von eCTD 4.0-Strukturen durch.
- Identifizieren Sie potenzielle Probleme bei der Granularität von Dokumenten und dem Metadata-Mapping, bevor das endgültige Mandat der EMA erteilt wird.
Durch einen frühzeitigen Start können Unternehmen einen reibungslosen Übergang ohne Unterbrechungen bei den behördlichen Einreichungen sicherstellen.
Wie geht es weiter? Die Zukunft von eCTD 4.0 in Europa
Während der vollständige Zeitplan für den Übergang noch unklar ist, umfasst die langfristige Strategie der EMA Folgendes:
- Standardisierung von Einreichungen auf globalen Märkten zur Verbesserung von Konsistenz und Effizienz.
- Verkürzung der Genehmigungsfristen durch eine bessere Nachverfolgung des Einreichungslebenszyklus.
- Integration von KI und Automatisierung in regulatorische Arbeitsabläufe zur Verbesserung der Compliance.
In den nächsten Jahren können wir mehr Klarheit von der EMA erwarten, einschließlich offizieller Übergangsfristen und neuer Validierungskriterien.
Fazit
Obwohl die EMA eCTD 4.0 noch nicht vorgeschrieben hat, ist es nur eine Frage der Zeit, bis es der Standard für regulatorische Einreichungen in der EU wird. Unternehmen, die sich proaktiv vorbereiten, werden einen Wettbewerbsvorteil erzielen, indem sie die Einhaltung der Vorschriften sicherstellen und kurzfristige regulatorische Hürden vermeiden.
Wichtige Erkenntnisse
- eCTD 3.2.2 bleibt der aktuelle Standard, aber eCTD 4.0 zeichnet sich ab.
- Die EMA verfolgt einen schrittweisen Ansatz, ohne dass bisher ein offizielles Mandat vorliegt.
- Unternehmen sollten jetzt mit den Vorbereitungen beginnen, um einen reibungslosen Übergang zu gewährleisten.
- Investitionen in neue Technologien, die Schulung von Teams und das Testen von Einreichungen werden entscheidend sein.
Handlungsaufforderung
Bleiben Sie über die regulatorischen Ankündigungen der EMA auf dem Laufenden und beginnen Sie, Ihre Bereitschaft für eCTD 4.0 zu bewerten. Je früher Sie sich vorbereiten, desto einfacher wird der Übergang sein, wenn das Mandat kommt.
Benötigen Sie Unterstützung bei der Auswahl einer eCTD 4.0-konformen Software oder möchten Sie verstehen, wie dieser Übergang Ihr Geschäft beeinflusst? Zögern Sie nicht, uns zu kontaktieren.









