
Die Welt der pharmazeutischen Vorschriften steht mit der Einführung von eCTD 4.0 vor einem großen Upgrade. Dieses standardisierte Format verspricht einen reibungsloseren Weg für neue Arzneimittelanträge, die bei den Regulierungsbehörden eingereicht werden. Doch für Unternehmen, die ein Stück des 141,5 Milliarden US-Dollar schweren japanischen Pharmamarktes erobern wollen, gibt es eine entscheidende Wendung – Japan beschleunigt den Zeitplan für die Einführung!
Nachfolgend finden Sie eine Analyse dieser Highlights:
- Obligatorische Einführung: Im Gegensatz zu anderen Regionen, die vor der obligatorischen Einführung freiwillige Phasen haben, strebt Japan an, die Nutzung von eCTD 4.0 bis 2026 obligatorisch zu machen.
- Vorbereitung ist entscheidend: Aufgrund von Zeitbeschränkungen und dem Fehlen eines direkten Migrationspfads vom japanischen PMDA-Format JP1.0 zu eCTD 4.0 ist eine gute Vorbereitung entscheidend. Ein Fokus auf ein besseres System wird japanische Pharmaunternehmen während des Übergangsprozesses unterstützen. Diese Schritte umfassen die Aktualisierung von Software, die Schulung des Personals und die Vorbereitung von PDFs für das neue Format.
- Verfügbare Ressourcen: Die japanische Arzneimittel- und Medizinproduktebehörde (PMDA) hat Ressourcen veröffentlicht, die Unternehmen durch diese Umstellung führen können, wie den „ICH Electronic Common Technical Document eCTD 4.0 Implementation Guide“ mit Erläuterungen zu vorgenommenen Änderungen und verfügbaren Best Practices.
Hier sind einige Gründe, warum Sie bei diesem Zahlenspiel nicht zurückbleiben sollten:
- Schnellweg zu eCTD 4.0: Im Gegensatz zu anderen Regionen, in denen der Prozess schrittweise erfolgt, strebt Japan eine obligatorische Einführung von eCTD 4.0 bereits im Jahr 2026 an. Das sind drei Jahre vor der von der US FDA für 2029 gesetzten Frist! Mit einem so ambitionierten Zeitplan bedeutet dies, dass Japan die Führung bei der globalen eCTD-Integration übernommen hat.
- Kein Raum für Fehler: JP konnte im Gegensatz zu seinen früheren Versionen nicht direkt in eCTD 4.0 konvertiert werden. Das bedeutet, dass Pharmaunternehmen besonders gut darauf vorbereitet sein müssen, um Verzögerungen bei der Einreichung zu vermeiden, die sie Millionen an Einnahmen kosten könnten.
- Unterstützung für einen reibungslosen Übergang: Die japanische Arzneimittel- und Medizinproduktebehörde (PMDA) versteht die Herausforderungen. Sie hat Ressourcen wie Implementierungsleitfäden entwickelt, die Unternehmen dabei helfen sollen, diese Änderungen problemlos zu bewältigen und erfolgreich auf dem japanischen Markt Fuß zu fassen. (https://www.pmda.go.jp/english/).
Wenn Sie Medikamente für den riesigen japanischen Markt entwickeln, ist es höchste Zeit, sich vorzubereiten! Hier ist Ihre Checkliste vor dem Start:
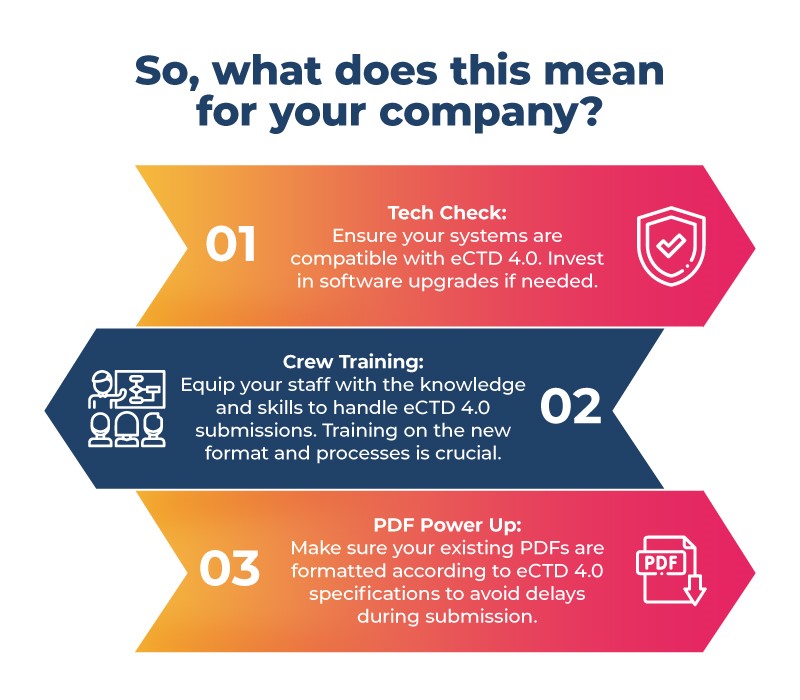
Der Übergang zu eCTD 4.0 verspricht eine höhere Effizienz und globale Standardisierung im gesamten Arzneimittelzulassungsprozess für Pharmazeutika. Ihr Unternehmen kann diesen Schritt in Japan antizipieren, um einen reibungslosen Übergang zu gewährleisten und die unzähligen Möglichkeiten dieser neuen Ära zu nutzen. Denken Sie daran: Wer sich nicht vorbereitet, bereitet sich auf das Scheitern vor – seien Sie also bereit, mit eCTD 4.0 in Nippon durchzustarten.
Die Vorteile und Chancen, die sich daraus ergeben, sind für die Pharmaindustrie attraktiv. Es gibt jedoch auch einige Schwierigkeiten, die auf dem Weg dorthin bewältigt werden müssen. Um sich nahtlos in einem sich ständig ändernden regulatorischen Umfeld zurechtzufinden, können Unternehmen Partnerschaften mit zuverlässigen Beratern wie Freyr eingehen. Gestalten Sie die Zukunft der regulatorischen Einreichungen in Japan mit unserer einzigartigen eCTD-Software, Freyr SUBMIT PRO, die den 21 CFR Part 11 Standards entspricht und ein flexibles Bereitstellungsmodell bietet. Kontaktieren Sie uns noch heute, um mehr zu erfahren und sich auf den Weg zu mehr Effizienz und Erfolg zu begeben. Fordern Sie noch heute eine Demo an.









