
ERREICHEN DER FRIST FÜR DIE IDMP-KONFORMITÄT BIS JULI 2016: KEIN LEICHTES UNTERFANGEN
Es gibt viele Fragen zu IDMP, zum Beispiel: Wo befinden sich die Daten in einem Unternehmen? Ist die Bereinigung und Abstimmung der aktuellen Daten erforderlich? Wie organisieren Unternehmen diese Daten für einen einfachen Abruf und eine reibungslose Übermittlung? Verfügt das Unternehmen über Prozesse, die von einem zentralen Datenspeicher profitieren können?
Die Erreichung der Identification of Medicinal Products (IDMP)-Konformität ist kein triviales Unterfangen, die Aktivität muss verschiedene regulatorische und operative Zwänge berücksichtigen. Organisationen müssen warten, bis die Behörden endgültige Leitlinien herausgeben und Spezifikationen genehmigen. Gleichzeitig könnte das Warten auf diese Leitlinien ihnen nicht genügend Zeit lassen, ihre Angelegenheiten zu regeln.
IDMP ist ein komplexer Standard, der weitreichende Auswirkungen auf Daten hat und die Zusammenarbeit vieler verschiedener Abteilungen erfordert. Diese Umstellung bietet die Gelegenheit, die Geschäftsprozesse und IT-Systeme eines Unternehmens umfassend zu überprüfen. Sie hilft auch dabei, ein stabiles System zur Verwaltung von Änderungen einzurichten.
Unternehmen müssen verstehen, dass eine gute Informationsarchitektur Anstrengung und Zeit erfordert, und sie müssen auch erkennen, dass IDMP nicht nur ein größeres xEVMPD ist. Es ist auch wichtig zu beachten, dass die ICH-Leitlinien nur einen Teil des Ganzen darstellen und die Verfügbarkeit regionaler Leitlinien entscheidend ist. Man muss auch bedenken, dass parallele regionale Implementierungen unterschiedliche Umfänge und Zeitrahmen mit einer großen Bandbreite an Datenlieferanten haben werden.
Darüber hinaus müssen Pharmaunternehmen, die in regulierten Regionen vermarkten wollen, ab 2016 IDMP-konform sein. Kürzlich veranstaltete die EMA einen IDMP-Informationstag und teilte ihren hochrangigen IDMP-Implementierungsstatus und Zeitplan mit. Nach Gesprächen mit der Pharmaindustrie, Softwareanbietern und der Analyse der eigenen System- und Ressourcenverfügbarkeit hat die EMA geplant, die gesamte EU-IDMP-Implementierung in mehrere Iterationen aufzuteilen. Dieser Plan wird der Europäischen Kommission (EC) zur Genehmigung vorgelegt, und wenn sie die EC überzeugen kann, wird die IDMP-Implementierung in der EU zwischen 2016 und 2018 erfolgen. Im schlimmsten Fall, wenn die EC nicht zustimmt, gibt es keinen Plan B. Bußgelder bei Nichteinhaltung belaufen sich auf bis zu 5 % des Umsatzes eines Unternehmens; keine gute Lösung für die anfängliche und laufende IDMP-Konformität zu haben, ist ein Risiko, das sich kein Pharmaunternehmen leisten kann.
IDMP: ENTWICKELT ALS GLOBALER SATZ VON STANDARDS UNTER ISO
Sollte eine Gesetzgebung zur Identifizierung von Arzneimitteln in einem der ISO-Länder eingeführt werden müssen, so erfolgt dies auf der Grundlage von ISO IDMP-Standards. Sobald verschiedene Regionen die IDMP-Standards übernehmen, wird die Dateneingabe konsistent sein, und globale Unternehmen sowie Regulierungsbehörden werden Zugang haben, um Daten auf Konsistenz über Regionen hinweg zu überprüfen. Darüber hinaus werden gemeinsame kontrollierte Vokabulare diesen Prozess stark erleichtern.
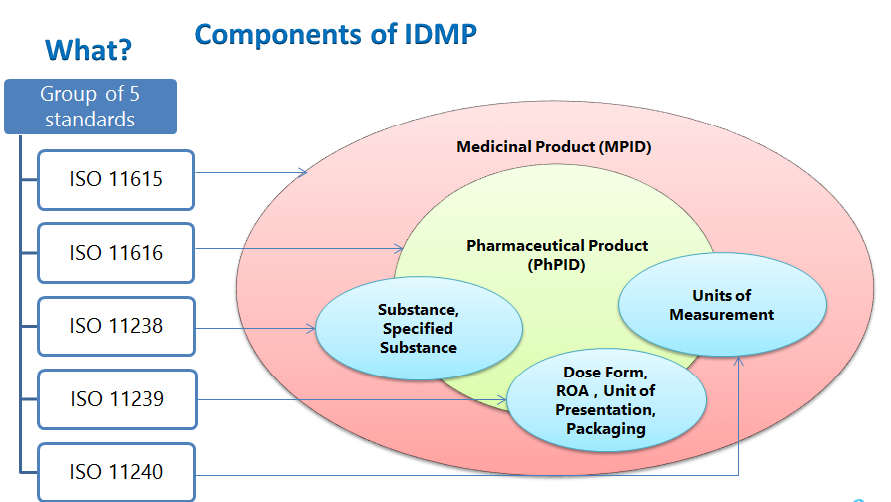
Strukturelle Elemente von IDMP umfassen die ID des Arzneimittels, die ID des pharmazeutischen Produkts, die Substanz-ID, kontrollierte Vokabulare – Darreichungsform, Verabreichungsweg, Verpackungsbestandteile, Darreichungseinheiten, Maßeinheiten sowie die Beschreibung des einzureichenden Herstellungsprozesses.
IDMP-STANDARDS
- ISO 11615 – Informationen zu Arzneimitteln
- ISO 11616 – Informationen zu pharmazeutischen Produkten
- ISO 11238 – Substanzen
- ISO 11239 – Pharmazeutische Darreichungsformen, Darreichungseinheiten, Verabreichungswege und Verpackung
- ISO 11240 – Maßeinheiten
AKTUELLER STATUS
ICH bereitet Implementierungsleitfäden vor und überarbeitet ISO-Standards
EU-Regulierungsbehörden bereiten sich auf IDMP vor
- Die EMA hat die Arbeit aufgenommen, um sich mit dem regulatorischen Netzwerk der EU abzustimmen und die Geschäftsfälle für die IDMP-Daten zu definieren.
- Die EMA richtet eine „EU ISO IDMP-Arbeitsgruppe“ und rekrutiert dafür Experten aus EMA-Ausschüssen und vom EU Network Data Board, um dies zu erreichen. Konkret wird sie Folgendes tun:
- Verbindliche und optionale ISO IDMP-Datenelemente definieren
- Definieren Sie Geschäftsregeln für optionale Datenelemente
- Definieren Sie Konformität und Datentypen
- Definieren Sie die EU-Governance-Modelle
US Position der Regulierungsbehörden
- Aktive Führung bei der Weiterentwicklung von IDMP mit den globalen (ehemals ICH) Regulierungsbehörden und mit der ISO
ANDERE REGULIERUNGSBEHÖRDEN
- Schweiz – Beabsichtigt die Umsetzung nach der EU (schneller Nachzügler)
- Japan und Kanada haben Regulierungsbehörden als Experten für die Substance IG-Gruppe benannt
ZEITPLÄNE
EUROPÄISCHE UMSETZUNGSLEITFÄDEN
- Der Entwurf der Umsetzungsleitfäden wurde initiiert, und die Leitfäden werden ab dem ersten Quartal 2016 verfügbar sein
SONSTIGES
- FDA: noch kein Datum, beabsichtigt aber, SPL bei Bedarf weiterzuentwickeln
- Japan – Unsicherheit im ICH-Bereich, arbeitet aber jetzt innerhalb der Gruppe der Regulierungsbehörden und der ISO
- Kanada – Die Umsetzung wird erwartet, aber es gibt noch keine konkreten Details
- Schweiz – Noch keine Aktualisierungen
IDMP-Konformitätsanforderungen verstehen
Für IDMP sind Informationen über Arzneimittel erforderlich, die mithilfe von Standardkennungen erfasst werden. Diese Kennungen basieren auf einer Hierarchie, die bei der Erstellung des EudraVigilance Medicinal Product Dictionary (EVMPD) oder seiner erweiterten Form (xEVMPD) entwickelt wurde. Es wird Überschneidungen mit Informationen geben, die in Structured Product Labeling (SPL)-Einreichungen in den US und anderen Produktregistern weltweit hinterlegt sind.
Allerdings verfügt IDMP über neue Identifikatoren, neue Kategorien und neue Wege, um die Beziehungen zwischen Elementen im Datenmodell auszudrücken. IDMP muss in die DNA der Organisation integriert werden, da es den Aufbau von Datenmodellen im gesamten Unternehmen vorantreiben muss. Die IT-Infrastruktur einer Organisation kann es dann über mehrere Systeme, Geschäftsprozesse und Funktionseinheiten wie RA, Sicherheit, F&E, Dokumentation und Herstellungsprozesse hinweg erkennen.
Herausforderungen bei der IDMP-Konformität
Organisatorisch
- Daten sind auf mehrere Abteilungen verteilt
- Die Unterstützung durch die Geschäftsleitung ist erforderlich, um die Beteiligung zu fördern
Technisch
- Daten entdecken, sammeln, konsolidieren und bereinigen
- 250 bis 300 Felder pro Produkt
Koordination
- Management kontinuierlicher Änderungen
- Koordination zwischen mehreren Teams
- Aufrechterhaltung der Datenregulierung durch interne Prozesse
ZUSAMMENFASSEND:
IDMP: Auswirkungen auf die pharmazeutische Industrie
Die Implementierung der IDMP-Standards wird voraussichtlich Auswirkungen auf die Vorbereitung und Planung von Einreichungen sowie die Pflege unternehmensweiter Daten haben, einschließlich Herstellungsdaten, strukturierter Substanzinformationen und Registrierungsinformationen.
IDMP-STANDARD: Effizienzsteigerungen bei der Implementierung gewährleistet
Sicherzustellen, dass Ihr Unternehmen für die IDMP-Herausforderung gerüstet ist, erfordert eine enge Zusammenarbeit zwischen verschiedenen Abteilungen. Ein kompetenter Dienstleister mit einem exklusiven Portfolio an regulatorischer Kompetenz kann Sie dabei unterstützen, die IDMP-Konformität zu erreichen. Dies hilft Ihrem Unternehmen, auf neue, sich entwickelnde Marktchancen zu reagieren.










