
In der pharmazeutischen Industrie hängt die Patientensicherheit von einem entscheidenden Faktor ab: der gleichbleibenden Produktqualität. Jede Tablette, jede Ampulle und jede Injektion, die einen Patienten erreicht, muss genau wie vorgesehen wirken. Diese Gleichbleibende Qualität ist das Ergebnis einer strengen Prozessvalidierung (PV), die durch ein solides Qualitätssicherungssystem (QA) geregelt wird.
Die Prozessvalidierung ist ein Qualitätsansatz, der sicherstellt, dass Fertigungsprozesse genau verstanden und kontrolliert werden und in der Lage sind, kontinuierlich Produkte zu liefern, die den vorgegebenen Spezifikationen entsprechen. Aus QA der QA wandelt sich die Prozessvalidierung von einer reinen Compliance-Maßnahme zu einer proaktiven Sicherheitsvorkehrung sowohl für die Produktintegrität als auch für die Gesundheit der Patienten.
Was ist Prozessvalidierung?
Gemäß den Richtlinien FDA ICH ist die Prozessvalidierung „die Erhebung und Auswertung von Daten, von der Prozesskonzeption bis hin zur kommerziellen Produktion, die den wissenschaftlichen Nachweis erbringt, dass ein Prozess in der Lage ist, kontinuierlich qualitativ hochwertige Produkte zu liefern.“
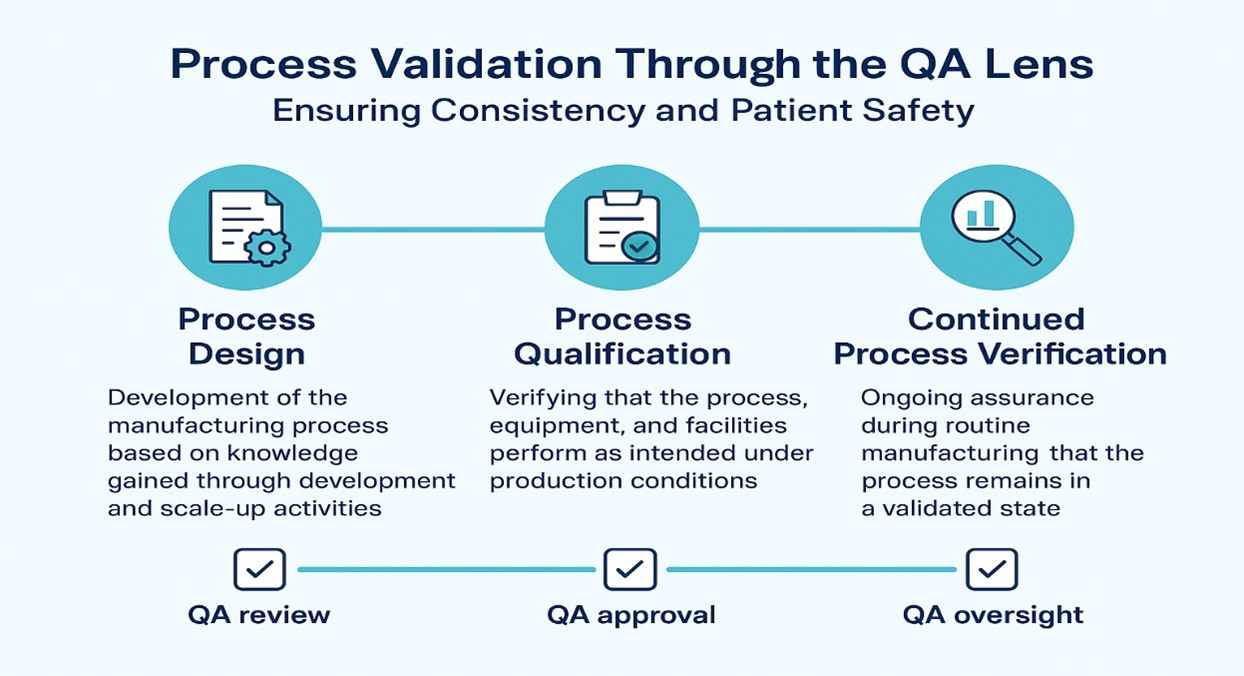
Der Validierungszyklus umfasst in der Regel drei (3) entscheidende Phasen:
- Phase 1 – Prozessgestaltung:
Entwicklung des Herstellungsprozesses auf der Grundlage der Erkenntnisse aus Entwicklungs- und Scale-up-Aktivitäten.
QARolleQA: Sicherstellung, dass Risikobewertungen, Designkontrollen und die Prinzipien von „Quality by Design“ (QbD) angewendet werden. - Phase 2 – Prozessqualifizierung:
Überprüfung, ob der Prozess, die Anlagen und die Einrichtungen unter Produktionsbedingungen wie vorgesehen funktionieren.
QAAufgabeQA: Genehmigung der Qualifizierungsprotokolle, Überprüfung von Abweichungen und Sicherstellung der Datenintegrität bei der Durchführung. - Phase 3 – Fortlaufende Prozessüberprüfung (CPV):
Kontinuierliche Sicherstellung während der routinemäßigen Fertigung, dass der Prozess in einem validierten Zustand bleibt.
QAAufgabeQA: Durchführung von Trendanalysen, Qualitätskennzahlen und CAPA-Systemen zur Aufrechterhaltung der Kontrolle.
QA : Mehr als nur Dokumentation
Während die Prozessvalidierung technische und statistische Bewertungen umfasst, stellt die QA sicher, dass diese mit wissenschaftlicher Genauigkeit und unter Einhaltung der gesetzlichen Vorschriften durchgeführt wird. Die Zuständigkeit QAerstreckt sich über alle Phasen – von der Planung und Protokollgenehmigung bis hin zum Änderungsmanagement und der laufenden Überprüfung.
- Risikobasierter Ansatz
QA eine zentrale Rolle bei der Umsetzung eines risikobasierten Ansatzes gemäß ICH . Kritische Prozessparameter (CPPs) und kritische Qualitätsmerkmale (CQAs) werden ermittelt, bewertet und überwacht, um Risiken zu minimieren. QA , dass Validierungsprotokolle statistisch fundiert sind und dass Pläne zur Risikominderung in das Design integriert werden.
- Datenintegrität und Rückverfolgbarkeit
Im era digitalen Transformation bleibt die Datenintegrität ein zentraler Schwerpunkt QA. Die ALCOA+-Prinzipien (zuordenbar, lesbar, zeitnah, original, genau sowie vollständig, konsistent, dauerhaft und verfügbar) dienen als Leitfaden für jede Dateneingabe und -prüfung. QA dass Validierungsdaten – von der Gerätequalifizierung bis hin zu Chargenprotokollen – rückverfolgbar und verifiziert sind und 21 CFR Part 11 von 21 CFR Part 11 entsprechen.
- Kontinuierliche Verbesserung durch CPV
Nach der Validierung QA die Prozessleistung mithilfe statistischer Prozesskontrolle (SPC) und Trendanalyse-Tools. Abweichungen oder Ergebnisse, die vom Trend abweichen, lösen Korrektur- und Vorbeugungsmaßnahmen (CAPA) aus, um die Prozessfähigkeit kontinuierlich zu verbessern. Dieses geschlossene Regelkreis-System stärkt die langfristige Konformität und verringert die Produktvariabilität.
Regulatorische Erwartungen und globale Standards
Aufsichtsbehörden weltweit, darunter die US FDA, EMA, MHRA und WHO, erwarten von Pharmaunternehmen, dass sie die Prozessvalidierung im Rahmen eines Lebenszyklusansatzes nachweisen. QA die Übereinstimmung mit diesen sich weiterentwickelnden Richtlinien QA , insbesondere:
- FDA für die Industrie – Prozessvalidierung: Allgemeine Grundsätze und Vorgehensweisen
- ICH (Arzneimittelentwicklung), Q9 (Qualitätsrisikomanagement) und Q10 (Qualitätssicherungssystem für Arzneimittel)
- EU-Anhang 15 – Qualifizierung und Validierung
Durch die Führung einer einheitlichen Dokumentation und die Gewährleistung der Rückverfolgbarkeit QA , dass die Prozesse für Inspektionen bereit sind und die weltweiten regulatorischen Anforderungen erfüllt werden, unabhängig von regionalen Unterschieden.
Herausforderungen bei der Prozessvalidierung und QA
Herausforderung | QA Lösung |
|---|---|
Uneinheitliche Daten zwischen den Chargen | Elektronische Chargenprotokolle (EBR) und Kontrollpunkte für die Überprüfung QA einführen |
Fehlende statistische Begründung bei der Stichprobenziehung | QA die Abstimmung des Protokolls auf statistische Konfidenzniveaus QA (z. B. 95-Prozent-Konfidenzintervalle) |
Unzureichende Dokumentation | QA Dokumentenkontrollsystemen und eine SOP Rückverfolgbarkeit |
Abweichungen während der Validierung | QA die Bearbeitung von Abweichungen, die Ursachenanalyse und die Umsetzung von Korrektur- und Vorbeugungsmaßnahmen QA |
Lebenszyklusmanagement | QA , dass die CPV-Programme und die Auslöser für die erneute Validierung klar definiert sind |
Digitale Transformation in QA der Prozessvalidierung
Moderne QA nutzen Automatisierung und digitale Validierungsplattformen, um die Effizienz und Genauigkeit zu steigern. Tools wie Validation Lifecycle Management Systems (VLMS) ermöglichen eine Zusammenarbeit in Echtzeit zwischen QA, Fertigungs- und Validierungsteams.
Dank Freyrs Fachkompetenz in den Bereichen Computersystemvalidierung (CSV) und Computersoftware-Sicherung (CSA) können Kunden konforme, skalierbare und prüfungsreife digitale Validierungsstrategien umsetzen. Dies gewährleistet nicht nur die Einhaltung gesetzlicher Vorschriften, sondern auch operative Exzellenz und schnellere Produktfreigaben.
Vertrauen durch Qualität schaffen
Die Prozessvalidierung ist ein kontinuierliches Bekenntnis zu Qualität, Sicherheit und dem Vertrauen der Patienten. Durch QA können Pharmaunternehmen sicherstellen, dass ihre Prozesse nicht nur validiert, sondern auch kontinuierlich verbessert werden, um den höchsten globalen Standards zu entsprechen.
Durch die Einbindung QA jede Phase der Prozessvalidierung stärken Unternehmen ihr Qualitätsmanagementsystem (QMS), verringern regulatorische Risiken und erfüllen ihr oberstes Versprechen: sichere und wirksame Produkte für Patienten weltweit.
Bei Freyr arbeitet unser Team aus QA Validierungsexperten mit globalen Pharmaunternehmen zusammen, um robuste, konforme und inspektionsbereite Validierungsrahmenwerke zu etablieren. Von der Behebung von Mängeln im Qualitätsmanagementsystem über die Entwicklung von Prozessvalidierungsstrategien bis hin QA digitalen QA gewährleistet Freyr eine nahtlose Einhaltung gesetzlicher Vorschriften und operative Exzellenz.
Erfahren Sie, wie Freyr Ihnen dabei helfen kann, Spitzenleistungen bei der Validierung zu erzielen.










