L'étiquetage fait partie intégrante de la commercialisation des dispositifs médicaux. L'étiquette est une information apposée sur le dispositif et/ou son emballage, présentée dans un format lisible par l'homme. L'objectif principal de l'étiquetage est de fournir des informations de sécurité aux utilisateurs, qu'il s'agisse de professionnels de la santé, de consommateurs ou de toute autre personne concernée.
Toutes les autorités réglementaires mondiales ont certaines exigences en matière d'étiquetage. De même, l'UE a détaillé les exigences d'étiquetage au chapitre III de l'annexe I du règlement européen sur les dispositifs médicaux (EU MDR) 2017/745. La chose la plus importante à noter est d'inclure tous les symboles couvrant les informations requises dans l'étiquetage du dispositif et les documents (brochures, manuels, notices d'utilisation, etc.) qui l'accompagnent.
Certaines des considérations critiques en matière d'étiquetage à prendre en compte lors de la conformité au règlement EU MDR 2017/745 sont :
1. Symbolique de l'étiquetage des dispositifs médicaux
Chaque fabricant est tenu d'intégrer le symbole du dispositif médical, qui indique que le produit fourni sur le marché de l'UE est un dispositif médical. Il est obligatoire d'apposer ce symbole sur le dispositif et sur tous les niveaux d'emballage. De plus, l'étiquette doit afficher le nom commercial et le nom d'origine du dispositif.
2. Dispositifs spéciaux
Si le produit est un dispositif spécial ou personnalisé, son statut doit être mentionné sur l'étiquetage. Par exemple, si le produit est destiné uniquement à une investigation clinique, l'étiquette doit le mentionner explicitement.
Pour les dispositifs contenant des matériaux absorbants ou susceptibles de se disperser localement dans le corps humain, l'étiquetage doit mentionner la composition du matériau et les détails quantitatifs sur les composants clés.
Un étiquetage explicite est même requis dans le cas des dispositifs à usage unique et des dispositifs stériles. Pour les dispositifs retraités, l'étiquetage doit mentionner le nombre de fois où ils peuvent être retraités, le nombre de fois où ils l'ont été jusqu'à présent, et la méthode de stérilisation utilisée.
3. Présence de substances toxiques
La déclaration de la présence de substances CMR (cancérogènes, mutagènes, toxiques pour la reproduction) et de substances perturbatrices endocriniennes est obligatoire sur les étiquettes si la concentration est supérieure à 0,1 % p/p. La liste de ces substances doit être apposée sur le dispositif et/ou l'emballage.
De plus, un élément labelling sur la présence de dérivés sanguins et tissulaires (même lorsqu'ils sont contenus dans la substance médicinale du dispositif combiné) doit être apposé sur les dispositifs.
4. Normes harmonisées
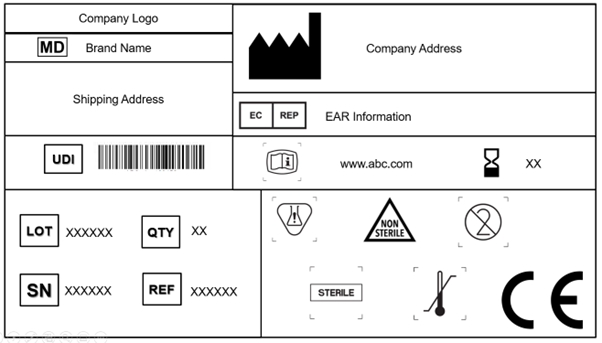
L'EU MDR 2017/745 reconnaît et accepte la norme ISO 15223-1: 2021. Le document détermine les symboles à utiliser sur l'étiquetage des dispositifs médicaux et de leur emballage. Le chapitre 3 (23.1,h) de l'Annexe I de l'EU MDR spécifie que des symboles reconnus internationalement peuvent être utilisés, et dans le cas de régions où ces symboles ne sont pas reconnus, la description de ceux-ci doit être fournie dans un document accompagnant le dispositif.
5. UDI
Les articles 27, 28, 29 et l'annexe VI (A, B, C) détaillent les règles et réglementations relatives à l'IUD. L'étiquette doit désormais contenir un support IUD [représentation de l'IUD pour l'Identification Automatique et la Capture de Données (IACD) et l'Interprétation Lisible par l'Homme (ILH)] sur le dispositif et les niveaux d'emballage supérieurs. L'emballage supérieur du dispositif (à l'exclusion des emballages d'expédition) aura son propre support IUD.
6. Informations électroniques d'utilisation (eIFU)
L'adresse web (URL) sous forme d'eIFU peut également être placée sur l'étiquetage des dispositifs médicaux, en complément des IFU papier. Les eIFU peuvent être utilisées pour les dispositifs médicaux implantables, implantables actifs, fixes et les logiciels (y compris ceux destinés au grand public).
7. Informations sur les opérateurs économiques (EOs)
L'étiquette contient généralement les informations du fabricant. Cependant, dans le cas des fabricants étrangers, les informations du représentant autorisé doivent figurer sur les étiquettes commerciales.
8. Avertissements et précautions
Les avertissements et précautions doivent être mentionnés sur l'étiquette du dispositif. Les informations à ce sujet peuvent être réduites au minimum, et les détails peuvent être fournis dans la notice d'utilisation (IFU).
Les fabricants sont également tenus de se conformer aux exigences d'étiquetage spécifiques à chaque pays. L'exigence linguistique dépend de l'État membre de l'UE. Cela peut avoir un impact considérable sur l'étiquetage, les notices d'utilisation (IFU) et l'emballage du dispositif en termes de temps et de coûts.
Ces exigences supplémentaires peuvent alourdir davantage la charge du fabricant, compte tenu de la complexité existante du processus d'étiquetage. Tout manquement à cet égard peut devenir très coûteux, impliquant des rappels de produits et des mesures correctives et préventives (CAPA) ultérieures.
Recherchez-vous de l'aide pour l'étiquetage conformément à l'EU MDR ? Freyr propose des services complets en matière d'étiquetage des dispositifs médicaux. N'hésitez pas à contacter nos experts en réglementation dès maintenant à l'adresse suivante : sales@freyrsolutions.com










