Services de Conformité, d'Audit et de Validation - Vue d'ensemble
Êtes-vous en conformité ? C'est une question à laquelle toute entreprise des secteurs pharmaceutique, biotechnologique, génomique, chimique, des dispositifs médicaux ou de la gestion de la chaîne d'approvisionnement a du mal à répondre. Ces organisations doivent se conformer à des exigences strictes en matière de qualité, de sécurité et de conformité dans chaque région où leurs produits sont distribués. La tendance actuelle en matière de gestion de la conformité réglementaire s'oriente vers une harmonisation mondiale de la qualité et de la sécurité, en mettant l'accent sur des pratiques rigoureuses. Que vous soyez fabricant ou fournisseur, votre expansion sur le marché, votre amélioration continue et la satisfaction de vos clients reposent principalement sur les normes de qualité de votre entreprise. Le Centre d'excellence (CoE) de Freyr dédié à la conformité réglementaire, à l'audit et à la validation peut vous aider dans cette démarche en vous proposant des services professionnels de conformité, d'audit et de validation pour les secteurs pharmaceutique, des dispositifs médicaux, des biens de consommation et de la santé, tels que les cGMP (bonnes pratiques de fabrication actuelles), GCP bonnes pratiques cliniques), GDP bonnes pratiques de distribution), les bonnes pratiques de laboratoire (GLP), les bonnes pratiques de pharmacovigilance GPVP ) etla validation des systèmes informatiques GxP (CSV). Notre équipe de conseil en conformité pharmaceutique propose des solutions sur mesure pour répondre à vos défis spécifiques en matière de conformité.
Freyr propose des services de conformité réglementaire, d'audit et de validation qui consistent à évaluer vos besoins et à formuler des recommandations pour vos processus opérationnels, dans le but de garantir la satisfaction de vos clients. Grâce à nos stratégies de préparation aux audits de conformité et de mise en conformité, nous fournissons des rapports de conformité et d'audit (analyse des écarts), incluant des suggestions d'actions correctives et préventives (CAPA) visant à éviter les éventuelles observations 483 et les conclusions d'audit de conformité émises par les autorités de réglementation. Les services de conseil en conformité pharmaceutique de Freyr s'étendent également au conseil en conformité en matière d'automatisation pharmaceutique, garantissant que vos systèmes automatisés répondent aux attentes réglementaires en constante évolution. Notre approche globale de la gestion de la conformité garantit que chaque étape du cycle de vie de vos processus est surveillée et optimisée pour s'aligner sur les exigences réglementaires.
Nous proposons des services de conformité réglementaire et de validation afin de garantir que l'ensemble de vos processus et produits sont conformes aux exigences applicables en matière de qualité, de sécurité de l'information et d'audit de conformité réglementaire, telles que (sans s'y limiter) les suivantes :
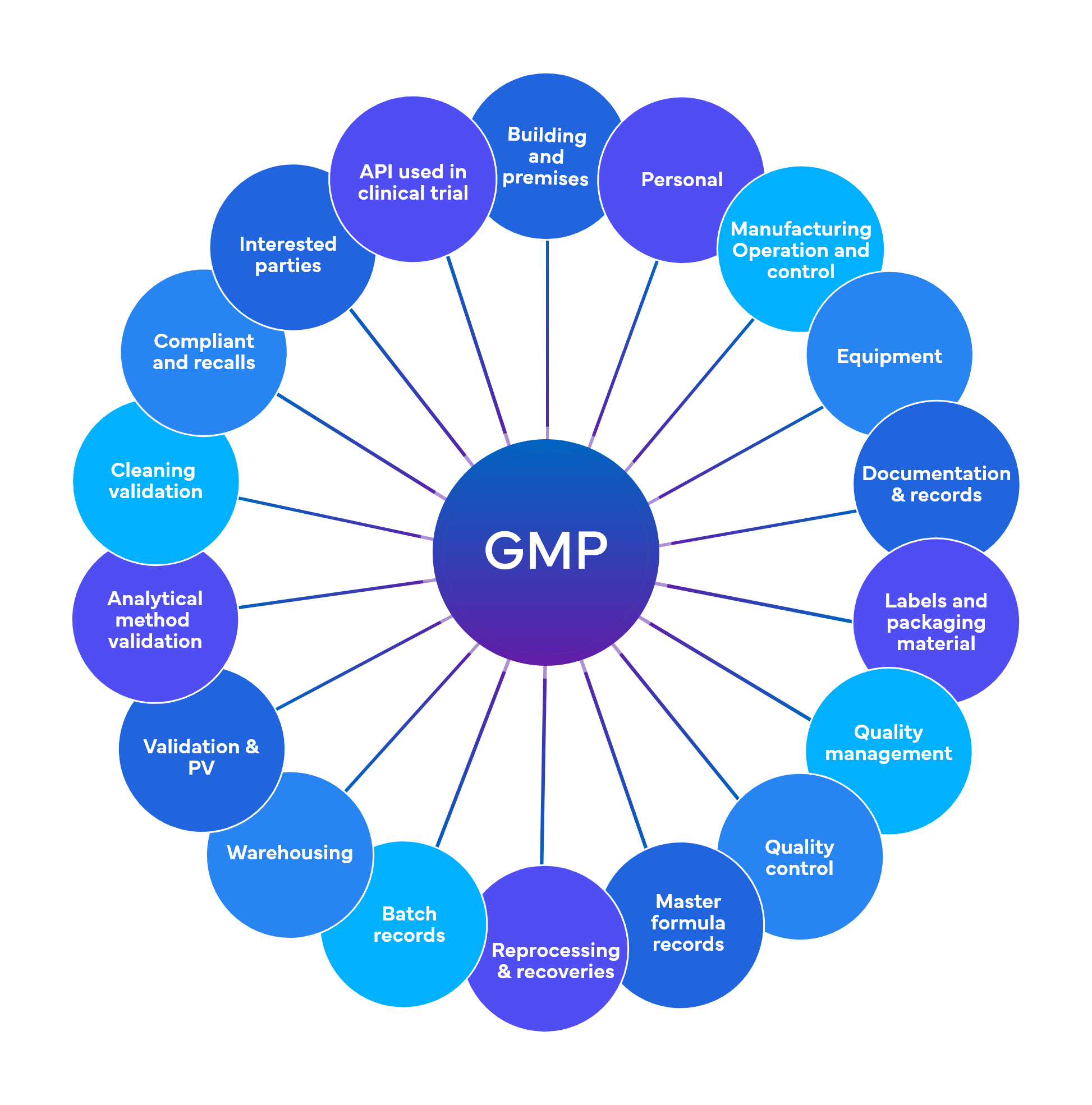
Freyr effectue environ 700 vérifications préliminaires réparties sur 18 à 19 domaines fonctionnels BPF.
Conformité, Audit et Validation chez Freyr
Services de Conformité, d'Audit et de Validation
Qualité et conformité réglementaire – Bonnes Pratiques de Fabrication (BPF) actuelles
- ISO / CEI 17025: 2017 - Exigences générales concernant la compétence des laboratoires d'essais et d'étalonnage
- OCDE (Organisation de Coopération et de Développement Économiques) - Lignes directrices des Bonnes Pratiques de Laboratoire
- Guide EURACHEM / CITAC : Guide de la qualité en chimie analytique - Une aide à l'accréditation, 3e édition (2016), doit être suivi dans les procédures analytiques.
- 21 CFR 58 : Bonnes Pratiques de Laboratoire pour les études de laboratoire non cliniques
- Guide des Réglementations GLP du Royaume-Uni, Février 2000 (par la GLPMA)
- Manuel de l'WHO sur les Bonnes Pratiques de Laboratoire (GLP) : Pratiques de qualité pour la recherche et le développement non clinique réglementés
- Santé Canada : Document d'orientation finalisé - Données d'études de laboratoire non cliniques à l'appui des demandes et soumissions de produits pharmaceutiques : Adhésion aux bonnes pratiques de laboratoire
- Normes de l'OSHA (Occupational Safety and Health Administration)
- Lignes directrices ICH applicables
Bonnes Pratiques de Laboratoire
- ISO / CEI 17025: 2017 - Exigences générales concernant la compétence des laboratoires d'essais et d'étalonnage
- OCDE (Organisation de Coopération et de Développement Économiques) - Lignes directrices des Bonnes Pratiques de Laboratoire
- Guide EURACHEM / CITAC : Guide de la qualité en chimie analytique - Une aide à l'accréditation, 3e édition (2016), doit être suivi dans les procédures analytiques.
- 21 CFR 58 : Bonnes Pratiques de Laboratoire pour les études de laboratoire non cliniques
- Guide des Réglementations GLP du Royaume-Uni, Février 2000 (par la GLPMA)
- Manuel de l'WHO sur les Bonnes Pratiques de Laboratoire (GLP) : Pratiques de qualité pour la recherche et le développement non clinique réglementés
- Santé Canada : Document d'orientation finalisé - Données d'études de laboratoire non cliniques à l'appui des demandes et soumissions de produits pharmaceutiques : Adhésion aux bonnes pratiques de laboratoire
- Normes de l'OSHA (Occupational Safety and Health Administration)
- Lignes directrices ICH applicables
Bonnes Pratiques Cliniques (GCP) et Bonnes Pratiques de Pharmacovigilance (GVP)
- Ligne directrice tripartite harmonisée ICH : Ligne directrice sur les bonnes pratiques cliniques - E6
- Spécification E2B(R3) du rapport individuel de cas de sécurité (ICSR) et fichiers associés
- Rapport périodique d'évaluation des bénéfices-risques (PBRER) E2C(R2)
- Autres lignes directrices ICH applicables
- Lignes directrices sur les modules des Bonnes Pratiques de Pharmacovigilance (BPV)
- Exigences FDA en matière de rapports FDA pour les demandes d'autorisation de mise sur le marché (IND) et BA/BE
- Déclaration de sécurité après commercialisation pour les médicaments à usage humain et les produits biologiques, y compris les vaccins
- Spécifications FDA de mise en œuvre FDA relatives à la notification ICH (R3) au système de notification des effets FDA (FAERS)
- Fournir des soumissions au format électronique – Questions et réponses techniques sur les ICSRs non accélérés après commercialisation
- Planification de la pharmacovigilance E2E
Sécurité de l'information, confidentialité des données et validation des systèmes informatisés (CSV).
- ISO 27001: 2013 Technologies de l'information – Techniques de sécurité – Systèmes de management de la sécurité de l'information – Exigences
- ISO 27002: 2013 Technologies de l'information – Techniques de sécurité – Code de bonnes pratiques pour la gestion de la sécurité de l'information
- USFDA 21 CFR Part 11 : Dossiers électroniques ; Signatures électroniques – Champ d'application
- Guide BPF de l'UE Annexe 11
- Notification de la directive japonaise ERES n° 0401022
- GAMP 5 : Une approche basée sur les risques pour des systèmes informatisés GxP conformes
- USFDA – Lignes directrices pour la validation des logiciels
- Lignes directrices ICH QSEM applicables
- Planifier et créer des SOP et contrôler les installations de fabrication
- Modèle de processus intégré
- Maintenir l'image de marque
- Services d'évaluation des risques
- Économies de coûts globales
- Mettre en œuvre des processus métier efficaces et conformes
- Établir des stratégies de validation et de qualification
- Expertise en conformité réglementaire et d'audit
- Auditeurs de conformité experts
Notre approche en matière de conseil en qualité et en conformité vise à fournir des informations exploitables et à apporter des améliorations durables, afin d'aider votre entreprise à atteindre l'excellence opérationnelle et à se conformer aux exigences réglementaires.



 Services de conformité et d'audit
Services de conformité et d'audit










