
Amerykańska Agencja ds. Żywności i Leków (US FDA) opublikowała wytyczne w grudniu 2022 roku, będące rewizją wytycznych z lipca 2022 roku, zatytułowanych „Brak odpowiedzi na pismo o pełnej odpowiedzi (CRL) dotyczące ANDA w określonym terminie regulacyjnym – wytyczne dla przemysłu”. Mają one na celu wsparcie wnioskodawców skróconych wniosków o dopuszczenie nowego leku (ANDA) składanych zgodnie z sekcją 505(j) Federalnej Ustawy o Żywności, Lekach i Kosmetykach (FD&C Act) (21 U.S.C. 355(j)). Kompletna i trafna odpowiedź na CRL jest kluczowa dla zatwierdzenia leku generycznego. Dokument z wytycznymi zawiera zalecenia dotyczące konsekwencji otrzymania CRL oraz działań, jakie FDA może podjąć, jeśli na CRL nie zostanie udzielona odpowiedź w określonym terminie.
FDA musi zapewnić, że zatwierdzone leki generyczne spełniają standardy bezpieczeństwa, jakości, skuteczności i przystępności cenowej. Jeśli ANDA nie spełnia wymagań regulacyjnych FDA, do wnioskodawcy wysyłane jest CRL, które zawiera niedociągnięcia zidentyfikowane podczas oceny.
Poniżej przedstawiono poglądowy opis tego, co wnioskodawca może zrobić w ciągu roku od otrzymania CRL:
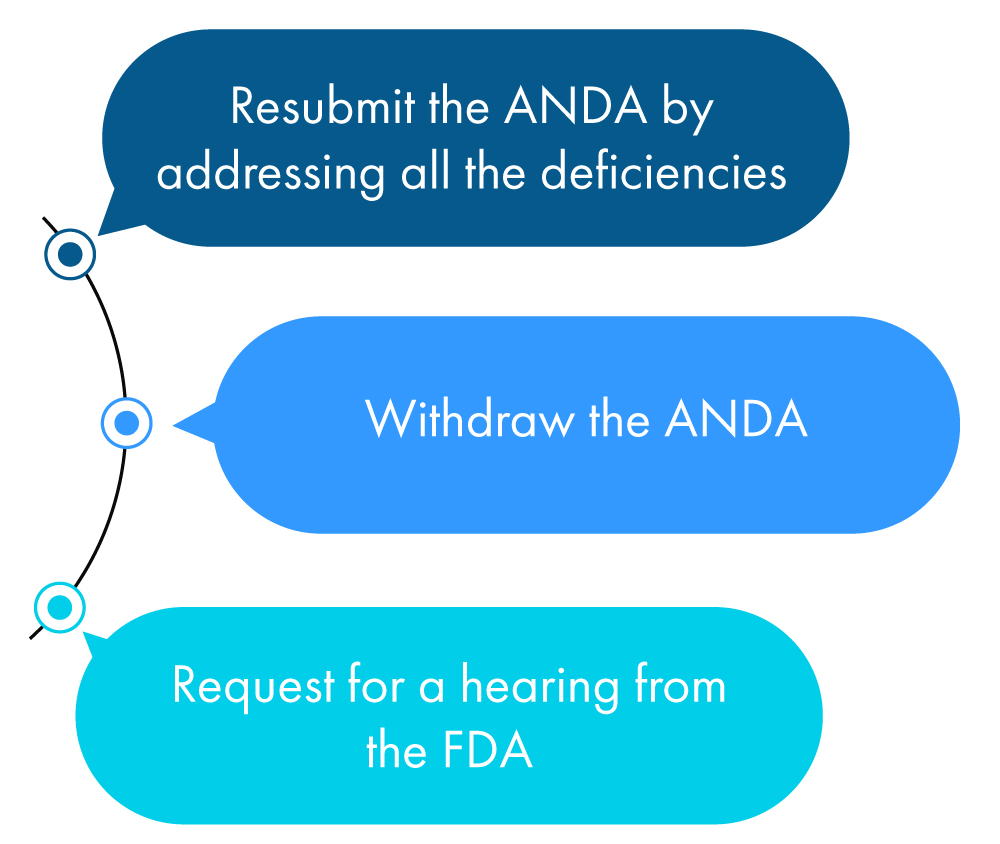
Jeśli wnioskodawca nie podejmie żadnych z powyższych działań, FDA uzna to za wniosek o wycofanie ANDA, chyba że wnioskodawca zażądał przedłużenia terminu na sprawdzenie wszystkich nieprawidłowości wymienionych w CRL.
Co się dzieje po jednym (01) roku od wydania CRL?
FDA wysyła pisemne powiadomienie, że wnioskodawca ma trzydzieści (30) dni od daty powiadomienia na następujące działania:
- Podaj powody, dla których ANDA nie powinna zostać wycofana
- Wniosek o przedłużenie terminu na usunięcie wszystkich niedociągnięć wymienionych w CRL
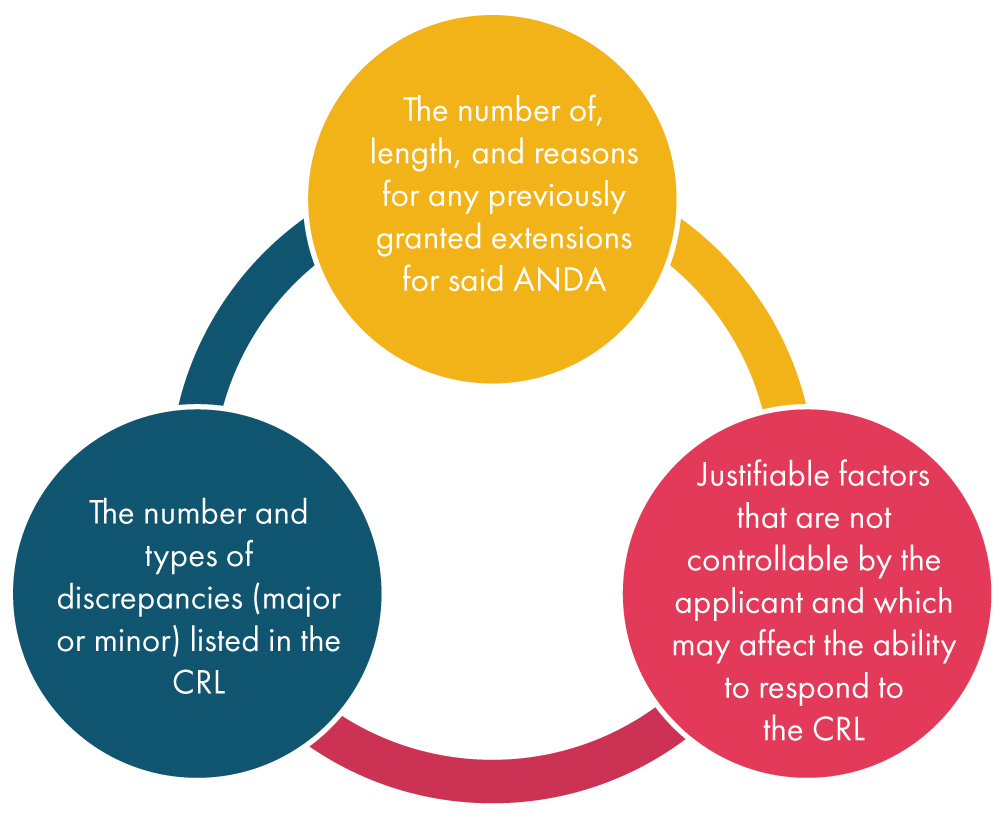
Po otrzymaniu przez FDA wniosku o przedłużenie od wnioskodawcy, rozważa ona różne czynniki wymienione poniżej, a następnie podejmuje decyzję w sprawie wniosku:
Czym jest poprawka?
Wnioskodawca musi złożyć wniosek o przedłużenie terminu odpowiedzi na CRL poprzez poprawkę. FDA klasyfikuje poprawkę jako znaczącą lub drobną w zależności od jej wpływu na proces zatwierdzania.
Kluczowe zalecenia FDA, o których wnioskodawcy powinni wiedzieć:
- FDA przeklasyfikuje drobną poprawkę jako istotną, jeśli poprawka zostanie złożona po roku od CRL, chyba że ANDA dotyczy produktu znajdującego się na liście leków deficytowych zgodnie z sekcją 506E ustawy FD&C (21 U.S.C. 356e), lub jest przedmiotem odpowiedzi na stan zagrożenia zdrowia publicznego ogłoszony przez Sekretarza Departamentu Zdrowia i Usług Społecznych US zgodnie z sekcją 319 ustawy o służbie zdrowia publicznego (42 U.S.C. 247d), lub przewiduje się, że będzie podlegać tym samym kryteriom, które mają zastosowanie do takiego oświadczenia, w momencie złożenia.
- Jeśli wnioskodawca nie usunie nieprawidłowości w CRL w przedłużonym terminie udzielonym przez FDA, ta ostatnia może rozważyć wycofanie ANDA.
- Jeśli wnioskodawca potrzebuje więcej niż trzydziestodniowego (30) okresu przedłużenia, może zażądać dalszego przedłużenia. Poprawka musi wtedy zawierać nowe informacje, które pozwolą FDA ustalić, czy przedłużenie może zostać udzielone, czy też nie.
Otrzymanie CRL od FDA może być dość zniechęcające dla wnioskodawców ANDA. Od usuwania rozbieżności po podawanie prawidłowych przyczyn/informacji dotyczących przedłużenia, wszystkie istotne wymagania powinny być spełnione, aby zapewnić szybsze zatwierdzenie leku. Freyr to sprawdzony ekspert regulacyjny z szeroką wiedzą w zakresie odpowiadania na CRL i zapewniania zgodności z wymaganiami FDA. Skontaktuj się z nami teraz w celu uzyskania End-to-End strategicznego wsparcia w zgłoszeniach ANDA.










