Gdy pandemia COVID-19 została po raz pierwszy uznana za globalny kryzys zdrowotny w 2020 roku, globalne organy ds. zdrowia (HA) podjęły innowacyjne kroki, aby poradzić sobie z nią w najlepszy możliwy sposób. Podobnie, firmy farmaceutyczne opracowały kilka szczepionek/Produktów leczniczych dla dobra publicznego. Jednak rejestracja produktów okazała się dość trudna. Aby uprościć rejestrację przy jednoczesnym zachowaniu ich bezpieczeństwa, jakości i skuteczności, HA udzieliły zezwoleń na użycie w nagłych wypadkach (EUA) na kilka szczepionek i odpowiednich produktów.
Może pojawić się pytanie, w jaki sposób organy ds. zdrowia były w stanie zapewnić, że korzyści z wymienionych produktów przewyższały ryzyko. Odpowiedzią jest przyjęcie najlepszych praktyk w zakresie monitorowania bezpieczeństwa stosowania produktów leczniczych (PV).
Czym jest monitorowanie bezpieczeństwa stosowania produktów leczniczych?
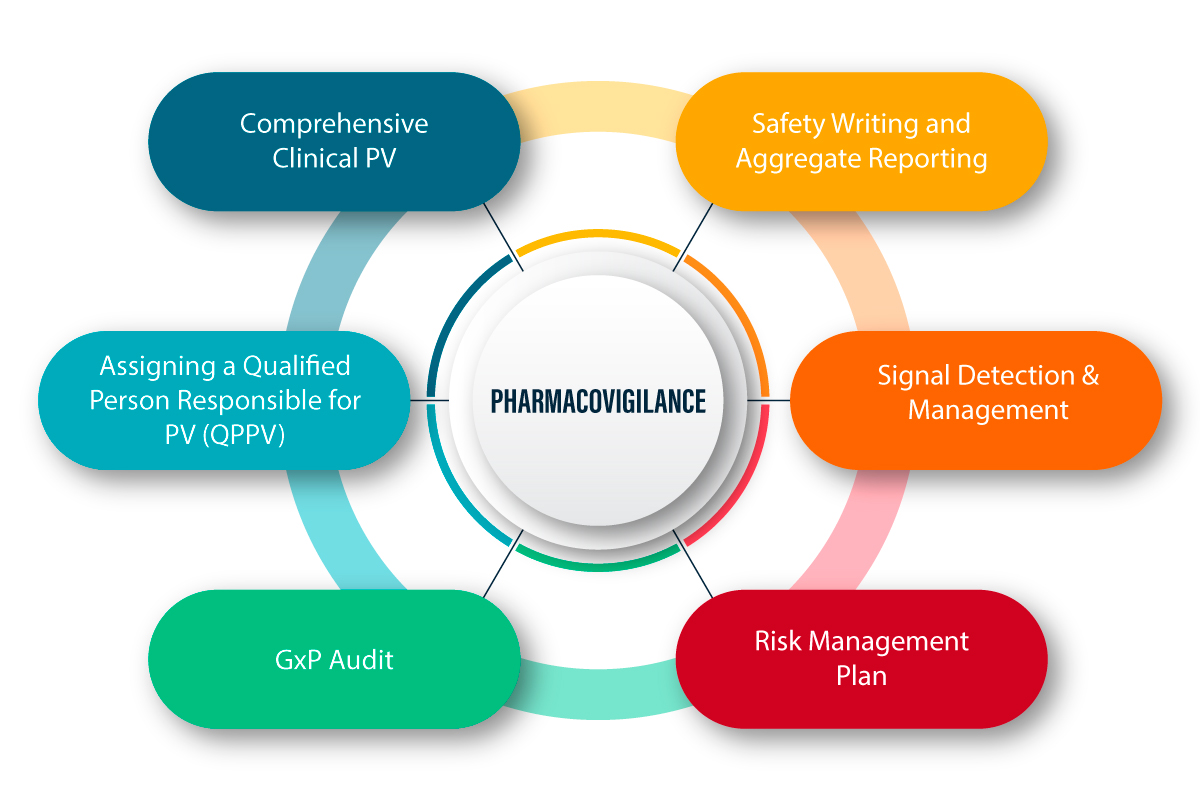
PV jest definiowane jako zbiór działań naukowych związanych z wykrywaniem, oceną, zrozumieniem i zapobieganiem niepożądanym skutkom oraz wszelkim innym problemom związanym z lekami. Poniżej przedstawiono obrazowe wyjaśnienie działania PV i związanego z nim procesu.
PV w pandemii COVID-19
Gdy pandemia COVID-19 zaczęła rozprzestrzeniać się na całym świecie, szczepionki i odpowiednie Produkty lecznicze musiały zostać wprowadzone na rynek w ograniczonym czasie, przy jednoczesnym zachowaniu wymaganych standardów jakości. W takich scenariuszach dostępnych było mniej uczestników do badań klinicznych na etapie rozwoju leków/szczepionek, a proces musiał zostać ukończony szybciej niż zwykle. Mogło to prowadzić do pojawienia się pewnych działań niepożądanych w fazie po zatwierdzeniu.
Dlatego też, bilans korzyści i ryzyka szczepionek/produktów leczniczych był uważany za najważniejszy. Dzięki terminowej komunikacji o niepożądanych reakcjach i szkodliwych skutkach ubocznych, skuteczność produktów była utrzymywana w czasie rzeczywistym.
Niektóre z kluczowych działań w zakresie PV, które pomogły w utrzymaniu bezpieczeństwa, jakości i skuteczności wspomnianych produktów w czasie pandemii, są następujące:
- Wdrożenie dobrego planu zarządzania ryzykiem
- Ocena ryzyka przy pomocy Okresowych Raportów o Bezpieczeństwie (PSUR)
- Gromadzenie danych dotyczących narażenia
- Badania bezpieczeństwa po uzyskaniu pozwolenia (PASS)
- Spontaniczne zgłaszanie podejrzewanych działań niepożądanych
- Skuteczne zarządzanie sygnałami
Monitorowanie bezpieczeństwa stosowania produktów leczniczych w Sprawach regulacyjnych (RA)
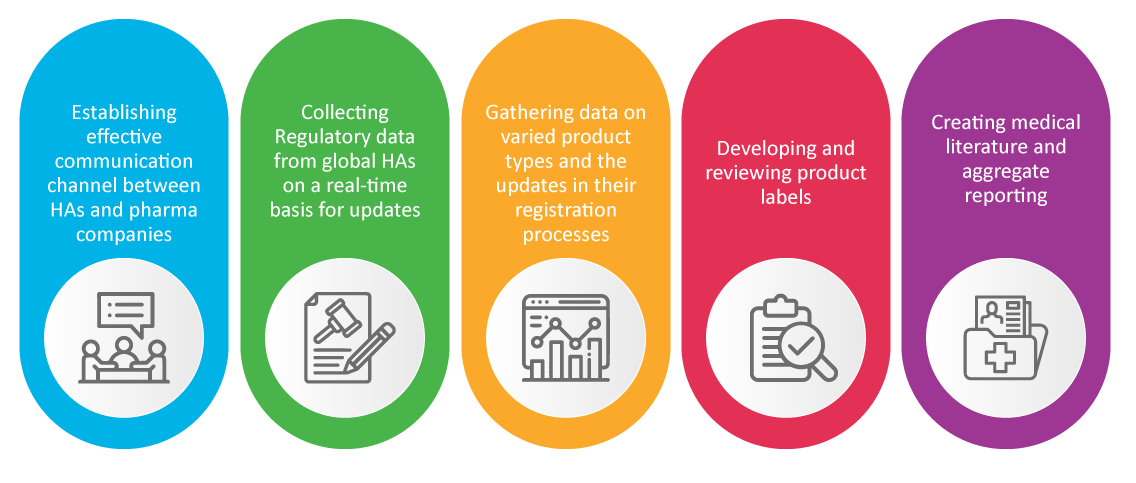
Powszechnie wiadomo, że zespół Spraw regulacyjnych firmy farmaceutycznej jest odpowiedzialny za bezpieczeństwo i zatwierdzanie nowych produktów. Specjaliści ds. RA zajmują się działaniami w zakresie monitorowania bezpieczeństwa stosowania produktów leczniczych, które okazały się kluczowe podczas pandemii, takimi jak:
Podsumowanie
Podsumowując, PV pomaga monitorować i raportować bezpieczeństwo produktu leczniczego. Dzięki spersonalizowanym Indywidualnym Raportom Przypadków (ICSR) producentom/sponsorom łatwiej jest przestrzegać odpowiednich przepisów globalnych organów ds. zdrowia (HA). Szukasz wsparcia regulacyjnego w przygotowaniu ICSR? Skonsultuj się ze sprawdzonym ekspertem regulacyjnym w celu zapewnienia zgodności. Skontaktuj się z Freyr.










