
Większość organizacji z branży nauk przyrodniczych ma trudności z usprawnieniem procesu składania dokumentów regulacyjnych z powodu częstych zmian w wytycznych dotyczących składania. Według niedawnej analizy przeprowadzonej przez United States Food and Drug Administration (USFDA), 32% zgłoszeń z danymi badawczymi miało krytyczne problemy ze zgodnością danych. Proces wymaga szerokiego zrozumienia współpracy między wewnętrznymi i zewnętrznymi interesariuszami. W ramach organizacji, działy produkcji, badań i rozwoju, badań klinicznych/nieklinicznych, QA/QC, marketingu i sprzedaży muszą harmonijnie współpracować, aby przyspieszyć proces zatwierdzania od początkowego etapu rozwoju do momentu wprowadzenia leku na rynek. Dział Spraw regulacyjnych i organy ds. zdrowia (HA) są w stałej korespondencji, aby zapewnić i ocenić bezpieczeństwo i skuteczność leków do stosowania u ludzi. Zobaczmy, jakie wstępne środki muszą podjąć organizacje farmaceutyczne, aby osiągnąć doskonałość w składaniu dokumentów regulacyjnych:
Przydzielanie i wdrażanie zasobów w celu usprawnienia, standaryzacji i przyspieszenia niezorganizowanych prac związanych ze zgłoszeniami
Specjalista ds. zgłoszeń uczestniczy na zasadzie umowy i może rozumieć więcej niż jeden (01) rodzaj zgłoszenia, będąc jednocześnie związanym z programami rozwojowymi przez lata, pomagając w tworzeniu przekonujących narracji do dossier. Dzięki temu organizacjom łatwiej jest:
- Zapobiegać błędom, równoważąc współpracę wewnętrznych i zewnętrznych interesariuszy.
- Skrócenie cyklu przeglądu przez HA procesu tworzenia i zatwierdzania dokumentów
- Przygotować kompletne i zgodne zgłoszenia, aby sprostać zmieniającym się wymaganiom regulacyjnym dla różnych rynków
- Potwierdzenie zgłoszeń objętych przez organ regulacyjny
- Monitoruj status tworzenia, przeglądu i zatwierdzania zgłoszeń
- Ulepszenie obecnego protokołu zgłoszeń
Uprość metodykę składania dossier
Przygotowywanie dokumentacji jest kluczowe w procesie tworzenia zgłoszeń. Zauważa się, że wnioski o pozwolenie na dopuszczenie produktów biologicznych (BLA) oraz wnioski o dopuszczenie nowych leków (NDA) obejmują wiele stron, co utrudnia organom regulacyjnym zrozumienie treści dokumentacji. Posiadanie ustrukturyzowanej prezentacji ogólnej koncepcji może znacznie zwiększyć zdolność zespołu do przygotowywania zgłoszeń oraz ułatwić ich przeglądanie przez agencje.
Wykorzystanie modułów do usprawnienia składania dokumentów umożliwia ekspertom analizę tego, co należy uwzględnić w każdej sekcji lub module dossier. Taka praktyka ułatwia:
- Wczesne rozpoczęcie tworzenia dokumentacji poprzez przyspieszenie przygotowania zgłoszenia przez organizację
- Wykorzystanie odpowiednich danych wymaganych do przygotowania zgłoszeń
- Wykorzystanie odpowiednich zasobów bez konieczności pisania obszernych dokumentów od podstaw dla każdego zgłoszenia
Współpracować z organami regulacyjnymi
Każda organizacja powinna regularnie spotykać się z organami regulacyjnymi (HA) we wczesnej fazie rozwoju produktu. Zapewnia to terminowy przegląd i informacje zwrotne, co skutkuje przyspieszonym rozpatrzeniem uwag przez HA, a w konsekwencji procesem zatwierdzania. To nie tylko buduje dobre relacje między organizacjami a HA, ale także pomaga uzyskać jasność na wczesnym etapie planowania zgłoszenia.
Usprawnij zarządzanie treścią i danymi w systemie zarządzania dokumentami (DMS)
Oczekuje się, że solidne repozytorium treści będzie zarządzać wszystkimi danymi z różnych obszarów funkcjonalnych, w tym wcześniej utworzoną dokumentacją i informacjami. Strukturyzowane repozytorium treści i danych zapewnia płynny dostęp do dokumentów z różnych obszarów funkcjonalnych bez dodatkowego wysiłku i potrzeby duplikowania. Dokumenty przechowywane w DMS stają się jedynym źródłem kontaktu dla wszystkich wewnętrznych interesariuszy (nauki kliniczne, CMC, badania niekliniczne, farmakokinetyka, farmakodynamika, pisanie medyczne i operacje kliniczne). Takie treści i dane mogą być wykorzystane do tworzenia lokalnych treści w oparciu o regionalne wymagania. Optymalizacja zgłoszeń regulacyjnych poprzez zarządzanie ustrukturyzowanymi treściami i danymi
Wdrażanie technologii i automatyzacji w celu ograniczenia powtarzalnych zadań i błędów
Organizacje mogą wykorzystać technologię, korzystając z funkcji automatycznej aktualizacji i kontroli jakości tabel, wykazów i rysunków (TLF) w tekście w odniesieniu do danych źródłowych, aby przyspieszyć proces dokumentacji. W ten sposób, za każdym razem, gdy wprowadzane są zmiany w istniejących tabelach źródłowych, odpowiednia aktualizacja następuje w TLF w tekście. Pomaga to wyeliminować ogólne godziny pracy, zaoszczędzić czas na ścieżce krytycznej i zwiększyć dokładność danych.
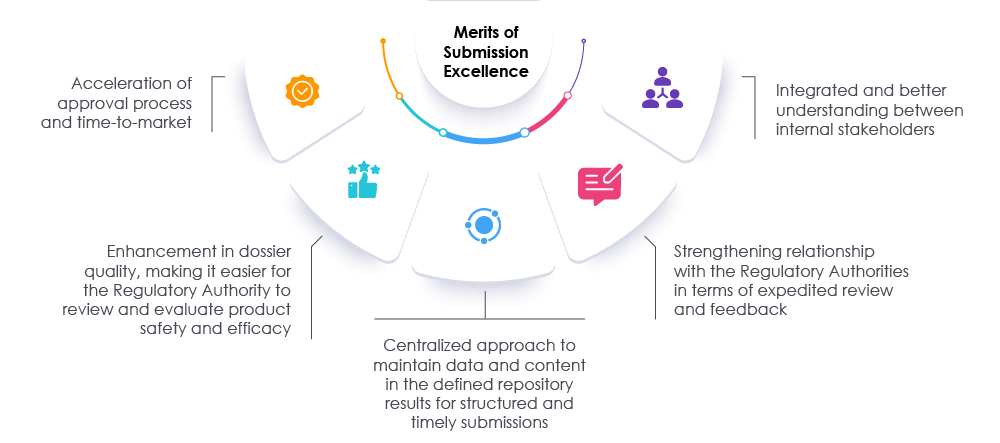
Przyjęcie odpowiednich środków wraz z terminowymi przeglądami dokumentacji i danych może pomóc zarówno organom regulacyjnym, jak i organizacjom przyspieszyć proces składania wniosków. Takie podejście przyspiesza wprowadzanie produktów na rynek, aby sprostać potrzebom zarówno pacjentów, jak i branży. Sprawdzony partner regulacyjny może pomóc organizacjom w ponownym przemyśleniu, ponownej ocenie i modyfikacji obecnych podejść do przygotowywania zgłoszeń. Nasi eksperci z Freyr mogą ułatwić drogę do osiągnięcia doskonałości w zakresie zgłoszeń regulacyjnych poprzez zwiększenie widoczności w całej organizacji i promowanie ogólnej zgodności, co pozwoli organizacji odnieść sukces na dzisiejszym rynku nauk przyrodniczych. Skonsultuj się z Freyr.










