Co to jest QMSR?
Wytyczne FDA stanowią uproszczone podejście dostosowane do wymagań ISO 13485:2016, które stanowi aktualizację poprzedniej struktury QSR. To dostosowanie ma kluczowe znaczenie, ponieważ ułatwia producentom, zwłaszcza tym prowadzącym działalność na skalę globalną, zapewnienie zgodności z przepisami na całym świecie. Dzięki tej harmonizacji przedsiębiorstwa będą mogły spełniać wymogi regulacyjne zarówno w US na innych rynkach w znacznie bardziej ujednolicony sposób.
QMSR nakłada obowiązek wprowadzenia usprawnień w zakresie zarządzania ryzykiem, projektowania wyrobów medycznych oraz nadzoru po wprowadzeniu do obrotu. Niniejsza aktualizacja może wprawdzie zwiększyć stopień złożoności, ale jednocześnie umożliwia producentom ujednolicenie procedur jakościowych, co z kolei podnosi poziom bezpieczeństwa wyrobów medycznych oraz zapewnia lepszą dokumentację, która może okazać się kluczowa podczas USFDA .
Dlaczego przejście z modelu QSR na model QMSR ma kluczowe znaczenie?

Zgodność z międzynarodowymi standardami
Pomoże to producentom w dostosowaniu się do globalnych wymagań dotyczących systemów zarządzania jakością (QMS) dla wyrobów medycznych poprzez przejście na standard QMSR, co ograniczy powielanie wymogów regulacyjnych dla producentów wyrobów medycznych działających na skalę globalną.
Wyższa jakość, bezpieczeństwo i skuteczność
Dzięki tej integracji urządzenia są produkowane zgodnie z globalnymi wymogami systemu zarządzania jakością. Pomaga to producentowi w poprawie jakości i bezpieczeństwa urządzeń.
Zgodność regulacyjna
Pomaga to producentom dostosować się do nowych wymogów, co zmniejsza ryzyko niezgodności z przepisami po wejściu rozporządzenia w życie 2 lutego 2026 r.
Najważniejsze zmiany związane z przejściem z QSR na QMSR:
Dostosowanie do terminologii normy ISO 13485:2016
Dzięki temu producenci stosują się do standardów uznanych na całym świecie.
Zarządzanie ryzykiem:
Kładzie nacisk na zarządzanie ryzykiem w całym cyklu życia wyrobu medycznego.
Konstrukcja urządzenia i elementy sterujące
Zgodnie z wytycznymi FDA zakres kontroli projektowych został rozszerzony, aby zapewnić, że producenci w pełni uwzględniają potrzeby użytkowników, bezpieczeństwo wyrobu oraz kryteria działania, co stanowi jeden z głównych obszarów zainteresowania podczas USFDA
Nadzór pozarynkowy
Firmy muszą usprawnić system nadzoru po wprowadzeniu produktu do obrotu. Będzie to wymagało od producentów gromadzenia informacji dotyczących bezpieczeństwa i skuteczności wyrobów, co pomoże w szybkim wykrywaniu i rozwiązywaniu problemów.
Dokumentacja i prowadzenie ewidencji
W ostatecznej wersji przepisów kładzie się nacisk na dokumentację; podczas kontroli kluczowe znaczenie ma prowadzenie dokładnej ewidencji.
Ważne terminy
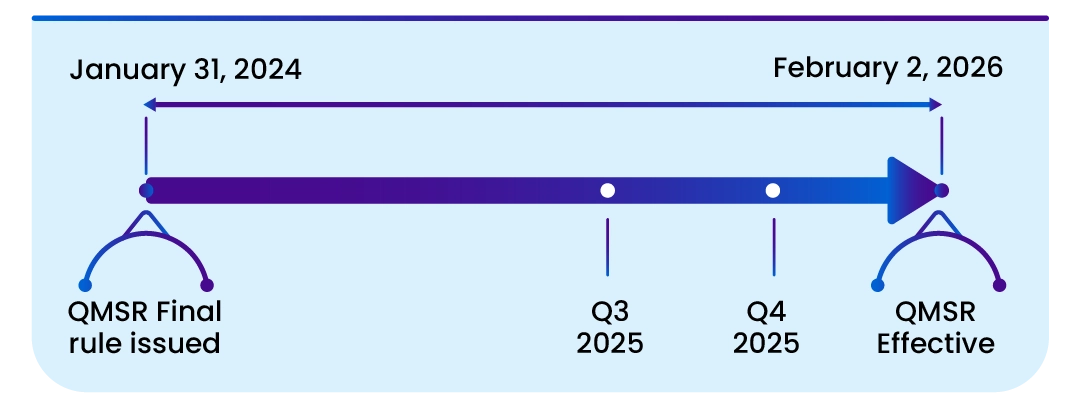
Niniejszy przepis wchodzi w życie z dniem 2 lutego 2026 r. Odwołanie do niektórych dokumentów wymienionych w niniejszym przepisie zostało zatwierdzone przez dyrektora Federalnego Rejestru w dniu 2 lutego 2024 r.
Skorzystaj z fachowego doradztwa w zakresie zgodności z normą QMSR
QMSR
- Klasyfikacja wyroby medyczne z wytycznymiFDA.
- Tworzenie dokumentów zgodnie z przepisami 21 CFR 820.
- Analiza luk w istniejących dokumentach systemu zarządzania jakością (QMS) zgodnie z 21 CFR 820.
- Plan naprawczy dla zgodności z 21 CFR 820.
- Symulacje audytów.
- Dedykowany zespół ekspertów ds. zapewnienia jakości (QA) w zakresie wyrobów medycznych.
- Sprawdzone doświadczenie w zakresie zgodności z 21 CFR 820.
- Elastyczne modele realizacji projektów.




 System QMSR wejdzie w życie 2 lutego 2026 r., co oznacza, że producenci będą mieli obowiązek dostosować swoje systemy zarządzania jakością.
System QMSR wejdzie w życie 2 lutego 2026 r., co oznacza, że producenci będą mieli obowiązek dostosować swoje systemy zarządzania jakością. Terminowe wdrożenie i skuteczne działania konserwacyjne mogą zmniejszyć prawdopodobieństwo wycofania produktu z rynku oraz liczby reklamacji.
Terminowe wdrożenie i skuteczne działania konserwacyjne mogą zmniejszyć prawdopodobieństwo wycofania produktu z rynku oraz liczby reklamacji. Zgodność z wytycznymi QMSR może ograniczyć liczbę uwag zgłaszanych przez US FDA nie wpłynie na status produktu na rynku regulowanym.
Zgodność z wytycznymi QMSR może ograniczyć liczbę uwag zgłaszanych przez US FDA nie wpłynie na status produktu na rynku regulowanym.