
Arzneimittel für neuartige Therapien (ATMPs) stellen einen hochmodernen Ansatz in der Medizin dar, der die Kraft von Zellen, Geweben oder Genen nutzt, um eine Vielzahl von Krankheiten zu behandeln. Aufgrund ihrer Komplexität und Neuartigkeit sind die regulatorischen Anforderungen für Arzneimittel für neuartige Therapien (ATMPs) verständlicherweise streng. Dies erstreckt sich auch auf das Artwork, das in den regulatorischen Einreichungen enthalten ist und eine entscheidende Rolle bei der klaren und prägnanten Vermittlung kritischer Informationen spielt.
Bei der Anpassung von Regulatory Artwork für Arzneimittel für neuartige Therapien (ATMPs) sollten die folgenden Punkte berücksichtigt werden:
Wenden Sie sich an unsere Experten für regulatorisches Artwork
Beratung anfordern
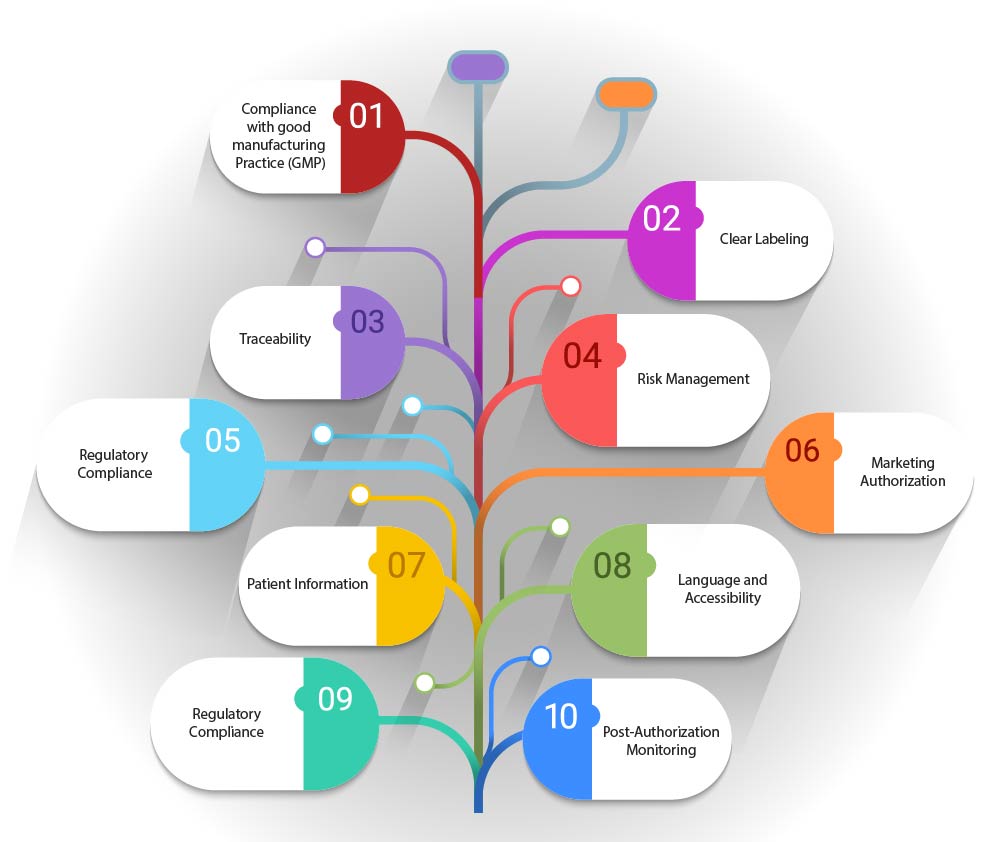
- Einhaltung der Guten Herstellungspraxis (GMP): Das Artwork muss den GMP-Richtlinien speziell für ATMPs entsprechen, die Details zum Herstellungsprozess, zur Qualitätskontrolle und zur Rückverfolgbarkeit umfassen können.
- Eindeutige Kennzeichnung: Das Artwork sollte die Art des Produkts angeben, einschließlich der Frage, ob es sich um eine Gentherapie, eine somatische Zelltherapie oder ein gewebetechnisches Produkt handelt. Es sollte auch spezifische Lager- oder Handhabungsanforderungen enthalten.
- Rückverfolgbarkeit: Angesichts des personalisierten Charakters vieler Arzneimittel für neuartige Therapien (ATMPs) sollte das Artwork die Rückverfolgbarkeit erleichtern. Dies kann eindeutige Identifikatoren oder Barcodes umfassen, die eine Verfolgung des Produkts von der Herstellung über die Verabreichung bis zum Patienten ermöglichen.
- Risikomanagement: Artwork sollte Informationen zum Risikomanagement enthalten, wie potenzielle Nebenwirkungen oder Gegenanzeigen, um sicherzustellen, dass Patienten und medizinisches Fachpersonal umfassend informiert sind.
- Einhaltung regulatorischer Vorschriften: Das Artwork muss dem regulatorischen Rahmen entsprechen, der durch Gesetzgebung wie die Verordnung (EG) Nr. 1394/2007 festgelegt ist. Diese Verordnung legt die Anforderungen für die Marktzulassung, Überwachung und Pharmakovigilanz von ATMPs fest.
- Marktzulassung: Das Artwork sollte den Status der Marktzulassung des Produkts widerspiegeln, ob es vollständig zugelassen, in klinischer Prüfung oder einer Krankenhausausnahme unterliegend ist.
- Patienteninformationen: Das Artwork sollte Patienteninformationsbroschüren umfassen, die umfassende Informationen über das ATMP, dessen Anwendung und die möglicherweise nach der Verabreichung erforderliche Überwachung enthalten.
- Sprache und Zugänglichkeit: Das Artwork sollte so gestaltet sein, dass es zugänglich und verständlich ist, wobei die Sprache und Lesbarkeit der bereitgestellten Informationen berücksichtigt werden müssen.
- Informationen der Regulierungsbehörde: Das Artwork sollte Informationen über die relevanten Regulierungsbehörden enthalten, wie die EMA (European Medicines Agency) und das CAT (Committee for Advanced Therapies), die für die Bewertung und Zulassung von Arzneimitteln für neuartige Therapien (ATMPs) zuständig sind.
- Überwachung nach der Zulassung: Falls zutreffend, sollte das Artwork jegliche Überwachung nach der Zulassung oder zusätzliche Studien erwähnen, die erforderlich sind, um die langfristige Sicherheit und Wirksamkeit des ATMP weiter zu bewerten.
Die Anpassung von regulatorischem Artwork für ATMPs erfordert einen sorgfältigen Ansatz, der wissenschaftliche Genauigkeit, klare Kommunikation und die Einhaltung sich entwickelnder regulatorischer Anforderungen in Einklang bringt. Obwohl internes Fachwissen wertvoll ist, kann die Navigation in dieser komplexen Landschaft äußerst vorteilhaft sein.
Hier kommt die Partnerschaft mit einem Spezialisten wie Freyr Solutions ins Spiel. Freyr Solutions bietet ein Team von Spezialisten für regulatorisches Artwork mit umfassender Erfahrung im Bereich ATMPs. Sie verstehen die spezifischen Herausforderungen, die mit ATMP-Artwork verbunden sind, und verfügen über die technischen Fähigkeiten, um klare, konforme und wirkungsvolle Visualisierungen zu erstellen.
Im heutigen Wettbewerbsumfeld kann eine starke regulatorische Einreichung den Unterschied zwischen Erfolg und Misserfolg ausmachen. Durch die Partnerschaft mit Freyr Solutions stellen Sie sicher, dass Ihr ATMP Artwork das Potenzial Ihrer Therapie effektiv präsentiert und den Weg für einen reibungsloseren regulatorischen Prozess ebnet. Mit ihrem spezialisierten Wissen und ihrem kollaborativen Ansatz wird Freyr zu einem unschätzbaren Vorteil, um Ihr bahnbrechendes ATMP auf den Markt zu bringen. Kontaktieren Sie uns noch heute!










