
Verblindete Studien sind der Grundpfeiler für die Integrität klinischer Studien, da sie Verzerrungen ausschließen und eine objektive Bewertung der Prüfpräparate gewährleisten. Hinter dieser wissenschaftlichen Strenge verbirgt sich jedoch eine entscheidende kreative Komponente: die Verpackungsetiketten für klinische Studien. Für artwork behördliche artwork , ist die Gestaltung für verblindete Studien ein Balanceakt zwischen Compliance, Vertraulichkeit und Klarheit.
Bei Freyr Solutionssind wir auf regelkonforme, auditfähige artwork globale klinische Studien spezialisiert. In diesem Blogbeitrag untersuchen wir, wie artwork für klinische Studien angepasst werden artwork , um den besonderen Anforderungen von Blindstudien gerecht zu werden.
Warum Artwork in Blindstudien Artwork
Die Gestaltung von Verpackungsetiketten für verblindete Studien (typischerweise in klinischen Studien) erfordert spezielle Verfahren, um die Verblindung aufrechtzuerhalten und die Einhaltung behördlicher sowie studienspezifischer Anforderungen sicherzustellen.
Im Gegensatz zu kommerziellen Produkten muss das artwork verblindeten Studien die Produktidentität verbergen und dennoch klare, behördlich genehmigte Informationen für die Endnutzer wie Prüfer, Apotheker und Patienten bereitstellen. Jede Abweichung – sei es in Farbe, Form, Schriftgestaltung oder beim Inhalt der Kennzeichnung – kann unbeabsichtigt zur Aufhebung der Verblindung der Studie führen.
Artwork verblindeten Artwork müssen daher folgende Hauptziele verfolgen:
- Gewährleistung der Verblindung: Auf dem Etikett dürfen keine Informationen enthalten sein, die Aufschluss über die Art der Behandlung geben könnten. Die optische Einheitlichkeit muss in allen Studienarmen gewahrt bleiben.
- Benutzerfreundlichkeit: Gewährleistung einer sicheren und korrekten Nutzung (z. B. ordnungsgemäße Anwendung durch das Personal vor Ort). Vermeidung einer Produktunterscheidung durch Designelemente.
- Umgang mit variablen Daten: Wichtige variable Datenelemente – wie Randomisierungscodes, Verfallsdaten, Kit-Nummern, Patienten-IDs und besuchsbezogene Informationen – müssen verfügbar sein.
- Einhaltung gesetzlicher Vorschriften: Halten Sie die globalen/regionalen Vorschriften für klinische Studien ein
- Rückverfolgbarkeit: Stellen Sie eine eindeutige Verknüpfung zur Studie und zum Patienten sicher, ohne dabei den Produkttyp preiszugeben. Das System sollte versionsverwaltet sein und die Nachvollziehbarkeit gewährleisten.
Verfahren zur Erstellung von Verpackungsetiketten für verblindete klinische Studien
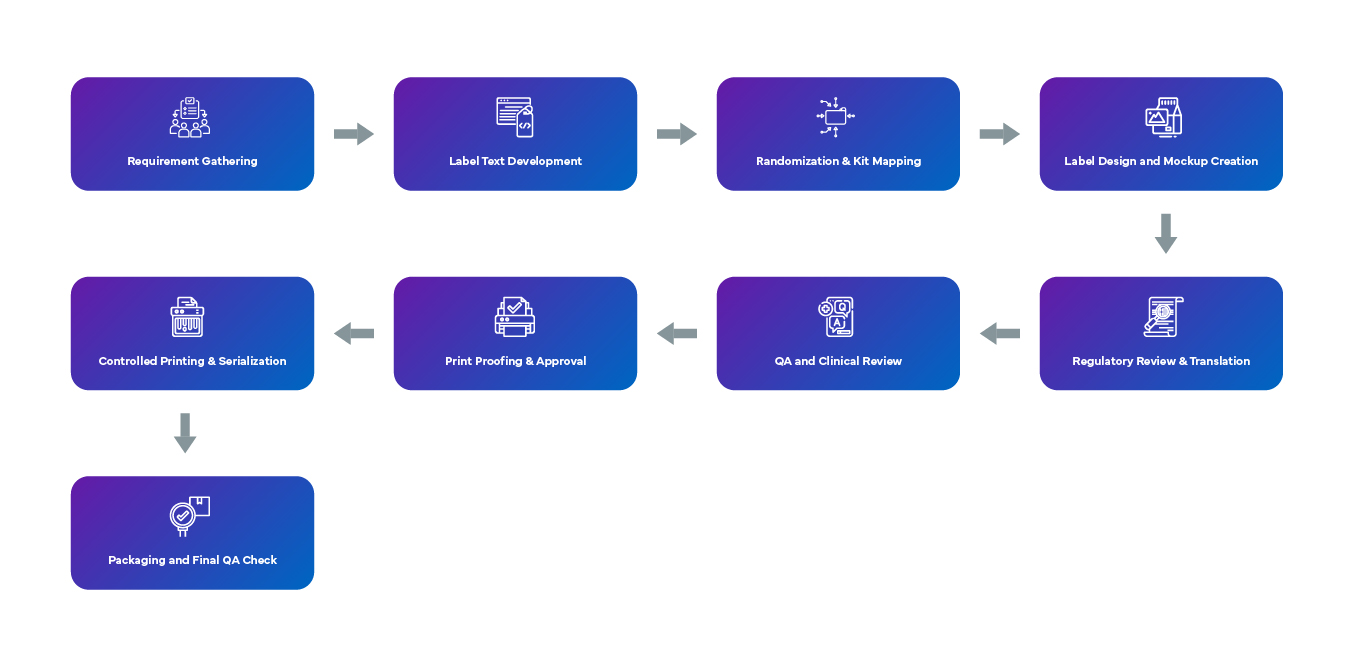
Der Prozess zur Gestaltung der verblindeten Etikettierung beginnt mit der Erfassung der Anforderungen durch die Überprüfung des Protokolls und die Einbeziehung der Interessengruppen, um die Übereinstimmung mit den länderspezifischen Vorschriften sicherzustellen. Der neutrale Etikettentext wird unter Verwendung von Begriffen wie „Prüfpräparat“ erstellt und enthält wichtige Informationen wie Studiennummern, Verfallsdaten und Warnhinweise, wobei Kennzeichnungen vermieden werden, die Aufschluss über die Behandlung geben könnten. Die Randomisierung und die Zuordnung der Kits werden sicher abgewickelt, wobei die Etiketten so gestaltet sind, dass die Verblindung gewahrt bleibt, häufig unter Verwendung von Barcodes. Entwürfe werden unter Berücksichtigung der Behältergröße, mehrsprachiger Anforderungen und Überlagerungsanforderungen erstellt. Regulatorische und Übersetzungsprüfungen gewährleisten die weltweite Compliance. QA klinische Teams überprüfen die Übereinstimmung mit dem Protokoll, während Etikettenproofs elektronischen Kontrollen und formellen Genehmigungen unterzogen werden. Die Strategie zur Etikettenanbringung – ob primär, sekundär oder Overlabeling – berücksichtigt umgebungsbedingte Einschränkungen. Der kontrollierte Druck, oft just-in-time, gewährleistet die serialisierte Rückverfolgbarkeit, und die Endverpackung wird unter QA fertiggestellt, um die Genauigkeit der Etiketten, die Haftung und die Integrität der Verblindung zu bestätigen.
Wichtige Artwork von Etiketten für verblindete Studien
| Artwork | Anforderungen an das Studiendesign bei verblindeten Studien | Freyrs Artwork |
| Farbschema | Vermeidet eine farbliche Unterscheidung, die auf Behandlungsgruppen hindeuten könnte | Einheitliche Farbpaletten für alle Bereiche; Graustufen oder neutrale Farbtöne werden bevorzugt |
| Schriftarten und Typografie | Einheitlicher Schriftstil und einheitliche Schriftgröße bei allen Varianten, um sichtbare Hinweise zu vermeiden | Vordefinierte typografische Richtlinien werden einheitlich auf alle Etikettenentwürfe angewendet |
| Layout und Hierarchie der Etiketten | Platzierung von Text und Grafiken gemäß den technischen Richtlinien | Vorlagenbasierte Designlayouts zur Gewährleistung einer einheitlichen Gestaltung |
| Placebo- vs. Wirkstoff-Kennzeichnung | Es dürfen keine optischen Unterschiede bestehen | Verwenden Sie identische Etikettenvorlagen; nur die variablen Felder unterscheiden sich durch die eingegebenen Daten. |
| Randomisierungs-/Tracking-Codes | Muss vorhanden sein, darf aber vom Endbenutzer nicht interpretiert werden | Möglichkeit, beliebige Barcodes zu erstellen. |
| Sprachmanagement | Mehrsprachige Inhalte sollten keine Layoutverzerrungen verursachen | Sprachblöcke sind symmetrisch angeordnet. |
| Dynamische Datenfelder | Angaben wie Chargennummer, Verfallsdatum und Komponenten-ID variieren je nach Packung | Platzhalterfelder oder gemäß den Vorgaben der Verpackung |
| Material und Format der Etiketten | Muss je nach Studienanforderungen eine Verblindung und Aufhebung der Verblindung ermöglichen | Verwendung von Heftetiketten, Abziehetiketten oder Überklebeetiketten nach Bedarf |
| Versionskontrolle und Freigabe | Die Etiketten werden aufgrund von Protokolländerungen häufig aktualisiert | Zentrale artwork mit Versionskontrolle für Etiketten und Genehmigungsmanagement |
Verweise auf Aufsichtsbehörden für die Kennzeichnung klinischer Studien
Region | Regulierungsbehörde | Verweis auf die Richtlinie |
| EU | EMA | Anhang VI der Verordnung (EU) Nr. 536/2014 |
| US | FDA | 21 CFR § 312.6 |
| UK | MHRA | Leitfaden zur guten klinischen Praxis |
| Kanada | Health Canada | Leitfaden für Sponsoren klinischer Studien |
Häufige Fehler bei Artwork von Blindstudien Artwork und wie man sie vermeidet)
✗ Verwendung unterschiedlicher Etikettengrößen für die aktive/Placebo-
✓ Einheitliche Größe und Form für alle Gruppen
✗ Die Anordnung der Sprachen variiert von Land zu Land
✓ Verwenden Sie gespiegelte Sprachblöcke mit einheitlicher Formatierung
✗ Sichtbare Chargen-/Produkt-IDs auf artwork
✓ Verwendung von verschlüsselten Daten und Barcodes, um sichtbare Identifikationsmerkmale zu verbergen
Warum sollten Sie bei der Erstellung von Artwork für Blindstudien mit Freyr zusammenarbeiten?
- Kompetenz im Bereich der Gestaltung von Blindetiketten für weltweite Studien
- Verfügbarkeit von regulatorischen Informationen in den US, der EU, Großbritannien, Kanada und der APAC-Region
- Bei Bedarf Einsatz eines Tools Artwork . Das Tool kann an die Anforderungen klinischer Studien angepasst werden.
- Versionsverwaltete, konforme und prüfungsfähige Dateien
- Mehrsprachigkeit und technisches Korrekturlesen von Etiketten für jedes beliebige Land oder jede beliebige Region










