
Die US FDA hat einen Leitfaden veröffentlicht, der der Branche und den Mitarbeitern der Gesundheitsbehörde (HA) helfen soll, zu bestimmen, wann eine Softwareänderung an einem Medizinprodukt von einem Hersteller die Einreichung und den Erhalt der FDA-Zulassung einer neuen Vorabmeldung (510(k)) erfordert. Dieser Leitfaden soll die Vorhersehbarkeit, Konsistenz und Transparenz des Entscheidungsprozesses „Wann einzureichen?“ verbessern, indem er einen am wenigsten belastenden Ansatz bietet und den regulatorischen Rahmen, die Richtlinien und Praktiken beschreibt, die einer solchen Entscheidung zugrunde liegen, insbesondere im Zusammenhang mit Softwareänderungen. Lassen Sie uns den FDA-Leitfaden im Detail beleuchten.
Leitprinzipien und Flussdiagramm der FDA
Mit der Absicht, Medizinproduktehersteller bei der Anwendung der Hauptprinzipien zu unterstützen, bietet das Dokument ein Flussdiagramm, zusätzliche Erläuterungen und Beispiele, die für Entscheidungen bezüglich einer neuen Prämarkt-Benachrichtigung 510(k) für eine Softwareänderung an einem bereits zugelassenen Gerät in den US erforderlich sind. Zusätzlich sollte man mehrere Leitprinzipien befolgen, wenn man diese Leitlinie verwendet, um zu bestimmen, ob eine neue 510(k)-Einreichung für die Änderung eines bestehenden Geräts erforderlich ist. Einige davon sind weithin bekannt und leiten sich aus der aktuellen FDA 510(k)-Politik ab, und andere sind notwendig, um das in dieser Leitlinie erwähnte Logikschema zu verwenden. Gemäß der Leitlinie kann das bereitgestellte Schema nicht alle möglichen Feinheiten im Zusammenhang mit solchen Änderungen und deren Auswirkungen auf die Entscheidung abdecken. Um daher die Notwendigkeit einer neuen Prämarkt-Benachrichtigung 510(k) zu bestimmen, sollten Medizinproduktehersteller die unten zusammengefassten allgemeinen Prinzipien und das Flussdiagramm berücksichtigen.
- Änderungen, die die Sicherheit oder Wirksamkeit eines Medizinprodukts beeinflussen
- Erstmalige risikobasierte Bewertung
- Unbeabsichtigte Folgen von Änderungen
- Einsatz von Risikomanagement
- Die Rolle von Tests (Verifizierungs- und Validierungsaktivitäten) bei der Bewertung, ob eine Änderung die Sicherheit und Wirksamkeit erheblich beeinträchtigen könnte
- Gleichzeitige Änderungen bewerten, um festzustellen, ob die Einreichung eines neuen 510(k) erforderlich ist
- Geeignetes Vergleichsprodukt und die kumulative Wirkung von Änderungen
- Dokumentationsanforderung (21 CFR Part 820)
- 510(k)-Einreichungen für modifizierte Medizinprodukte
- Feststellungen zur wesentlichen Gleichwertigkeit
- Die Einreichung eines neuen 510(k) ist wahrscheinlich erforderlich, wenn ein Hersteller sein Produkt so modifiziert, dass die Sicherheit oder Wirksamkeit des Produkts beeinflusst wird. Änderungen, die nicht dazu bestimmt sind, die Sicherheit oder Wirksamkeit eines Produkts zu beeinflussen, sollten jedoch dennoch bewertet werden.
- Um festzustellen, ob eine Änderung oder Modifikation die Sicherheit oder Wirksamkeit erheblich beeinflussen könnte, sollte der Hersteller zunächst eine risikobasierte Bewertung durchführen, um zu ermitteln, ob die Änderung die Sicherheit oder Wirksamkeit des Produkts positiv oder negativ beeinflussen könnte. Diese risikobasierte Bewertung sollte alle neuen Risiken und Änderungen bestehender Risiken, die sich aus der Produktänderung ergeben, identifizieren und analysieren und zu einer ersten Entscheidung führen, ob die Einreichung eines neuen 510(k) erforderlich ist.
- Manchmal gibt es zusätzliche unbeabsichtigte oder ungeplante Folgen, die bei Software-Einreichungen ausgelöst werden können. Das Flussdiagramm sollte diese Folgen bewerten, um festzustellen, ob die Einreichung eines neuen 510(k) erforderlich ist.
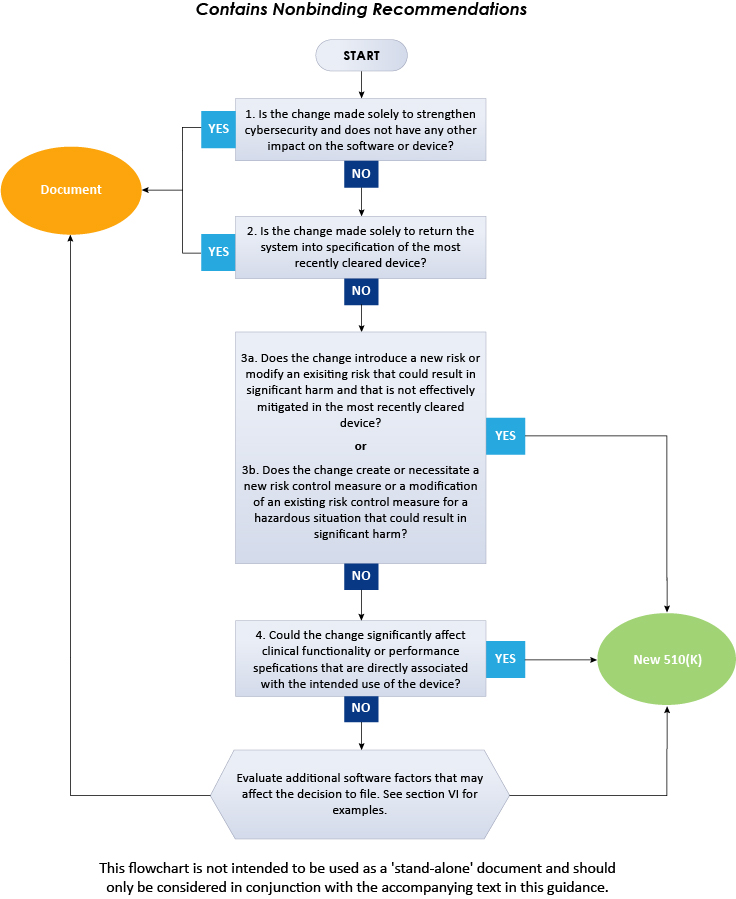
Das obige Flussdiagramm veranschaulicht ein Schritt-für-Schritt-Verfahren, das befolgt werden muss, um über die 510(k)-Einreichung für Softwareänderungen in bestehenden Geräten zu entscheiden. Zusammenfassend beschreibt der vorliegende FDA-Leitfaden detailliert den Ansatz, den Hersteller von Medizinprodukten verfolgen müssen, wenn sie entscheiden, ob Softwareänderungen an einem bestehenden Medizinprodukt die Einreichung einer neuen 510(k) erfordern. Um weitere Einblicke in den FDA-Leitfaden zu erhalten, konsultieren Sie Freyr – einen bewährten Regulierungsexperten. Bleiben Sie informiert. Bleiben Sie konform.









