
Die Idee elektronischer regulatorischer Einreichungen für Arzneimittel ist älter als das eCTD-Tool selbst. In den späten 1980er Jahren wurden Initiativen wie CANDA (Computer-Aided New Drug Application) von der US FDA (Food and Drug Administration) und europäischen Behörden untersucht. Diese frühen Bemühungen zielten darauf ab, die Effizienz und den Datenzugang für Prüfer zu verbessern.
Einführung des eCTD-Standards (2003):
Die Internationale Konferenz zur Harmonisierung (ICH) führte 2003 eine bahnbrechende Neuerung ein: den eCTD-Standard (Electronic Common Technical Document). Dieses standardisierte Format wurde entwickelt, um eine universelle Sprache für elektronische Einreichungen weltweit zu etablieren.
Das Aufkommen von eCTD-Tools:
Mit der Einführung des eCTD-Standards stieg die Nachfrage nach spezialisierten eCTD-Tools stark an. Diese Tools boten mehrere entscheidende Vorteile:
- Optimierte Inhaltserstellung: Benutzer konnten Dokumente mühelos gemäß der eCTD-Struktur erstellen und organisieren.
- Robuste Validierung: eCTD-Tools stellten sicher, dass Einreichungen den technischen Spezifikationen entsprachen, wodurch Verzögerungen durch Formatierungsfehler vermieden wurden.
- Effizientes Lebenszyklusmanagement: Die Verwaltung von Überarbeitungen, die Verfolgung von Versionen und die Aufrechterhaltung der Einhaltung regulatorischer Vorschriften wird einfacher.
Diese Innovationen revolutionierten den Prozess der regulatorischen Einreichung und machten ihn effizienter und zuverlässiger.
Wie die Software von Freyr Digital die eCTD-Erstellung automatisiert
Die fortschrittliche Softwarelösung von Freyr Digital, Freyr SUBMIT PRO, löst diese Herausforderungen, indem sie wichtige Aspekte der eCTD-Erstellung automatisiert und so die Effizienz steigert sowie menschliche Fehler reduziert.
Ressourcenoptimierung: Durch die Automatisierung wiederkehrender Aufgaben setzt unsere Software wertvolle Personalressourcen frei. Fachkräfte können sich auf strategischere und höherwertige Aktivitäten konzentrieren, wie Datenanalyse, Entwicklung regulatorischer Strategien und Einbindung von Stakeholdern. Diese Verlagerung steigert nicht nur die Produktivität, sondern senkt auch die Betriebskosten und bietet einen erheblichen Return on Investment.
Minimiertes Risiko menschlicher Fehler: Automatisierung minimiert das Risiko menschlicher Fehler, indem sichergestellt wird, dass Daten präzise übertragen und Dokumente korrekt formatiert werden. Die integrierten Validierungsprüfungen und Fehlererkennungsmechanismen der Software verbessern zusätzlich die Qualität und Konformität regulatorischer Einreichungen. Dies reduziert den Überarbeitungsaufwand und trägt dazu bei, zeitnahe Genehmigungen zu gewährleisten.
Einreichungs-Tracker für einen umfassenden Überblick über eCTD-Einreichungen
Ein benutzerfreundliches, automatisiertes System zur Planung und Verfolgung komplexer globaler eCTD-Einreichungsaktivitäten, zur Verwaltung von Arbeitsabläufen sowie zur Speicherung und Verwaltung von Zulassungsanträgen und Einreichungsinformationen ist unerlässlich. Es stellt sicher, dass Antragsteller die damit verbundenen Herausforderungen rechtzeitig bewältigen. Ein detaillierter Einblick in die Einreichungs- und Veröffentlichungsprozesse macht den gesamten Einreichungsprozess reibungsloser und schneller.
Einreichungsverfolgung
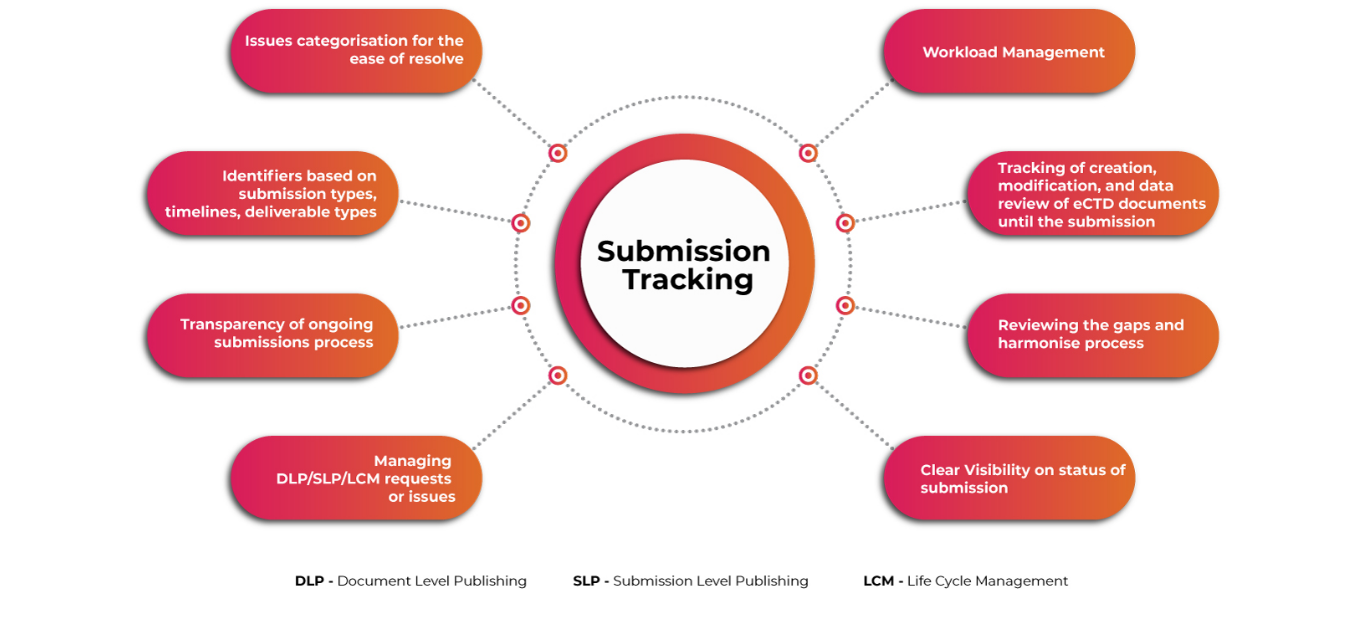
Das jüngste Upgrade des eCTD
Der Übergang zu eCTD 4.0 verspricht eine höhere Effizienz und globale Standardisierung im pharmazeutischen Arzneimittelzulassungsprozess. Indem sich Ihr Unternehmen auf diesen Übergang vorbereitet, kann es die Veränderungen nahtlos bewältigen und die zahlreichen Möglichkeiten dieser neuen Ära nutzen. Obwohl der Wechsel zu eCTD 4.0 Herausforderungen mit sich bringen kann, sind diese mit dem Engagement und der Entschlossenheit aller beteiligten Länder überwindbar. Auch wenn erhebliche Investitionen und Anstrengungen erforderlich sein werden, machen die wesentlichen Vorteile von eCTD 4.0 das Vorhaben wirklich lohnenswert.
Überarbeitung des Einreichungsprozesses: eCTD 4.0 verspricht, die Art und Weise zu revolutionieren, wie Pharmaunternehmen Arzneimittelentwicklungsdaten bei Gesundheitsbehörden einreichen. Ziel ist es, den Einreichungsprozess zu optimieren.
Zeitplan für die Implementierung: Die FDA plant, ab 2024 neue Anträge im eCTD 4.0-Format anzunehmen. Zukünftige Phasen werden bestehende v3.2.2-Anträge und die bidirektionale Kommunikation behandeln.
Vorwärtskompatibilität: eCTD 4.0 bietet Vorwärtskompatibilität, was die Wiederverwendung von Lebenszyklus- und Dokumenteninhalten aus Version 3.2.2 ermöglicht. Dies vereinfacht die Umstellung von 3.2.2-Anwendungen auf eCTD 4.0.
Validierungskriterien: Spezifikationen für die Validierungskriterien von eCTD 4.0 sind verfügbar. Diese Kriterien gewährleisten die Qualität und Genauigkeit der Einreichungen.
Globale Konformität: Bis 2026 könnten Aufsichtsbehörden weltweit die Einhaltung der eCTD 4.0-Standards vorschreiben. Obwohl derzeit freiwillig, wird die Durchsetzung zwischen 2026 und 2029 beginnen.
Die Zukunft des eCTD:
Sie sollten KI willkommen heißen und Ihre Regulierungsfunktion dynamisch gestalten, da sie Ihrem Unternehmen einen Mehrwert bietet. Freya Fusion ist eine hochmoderne, KI-gesteuerte, Cloud-native Plattform für regulatorisches Informationsmanagement (RIM), die außergewöhnliche Leistung, Sicherheit und Skalierbarkeit bietet, und das alles unter Einhaltung strenger GxP-Vorschriften. Ausgestattet mit fortschrittlichen KI/ML- und Automatisierungsfunktionen, zeichnet sich Freya Fusion im digitalen Bereich aus und bietet überragende Funktionalität sowie ein herausragendes Benutzererlebnis. Die KI-Fortschritte von Freyr Digital versprechen Module zur Erstellung und Verfolgung von Einreichungen, die Funktionen für die nahtlose Zusammenstellung, Veröffentlichung und Validierung regulatorischer Einreichungen umfassen und eine sorgfältige Einhaltung der eCTD-Richtlinien gewährleisten. Im Bereich der regulatorischen Compliance mit KI-gestütztem SaaS die Nase vorn zu haben, wird Ihrem Unternehmen sicherlich zugutekommen. Ob mit einem Frühwarnsystem für regulatorische Änderungen, einer optimierten Überprüfung und Analyse regulatorischer Dokumente oder prädiktiver Analytik für das Risikomanagement – Freyr Digital deckt all diese Bereiche für Sie ab. Kontaktieren Sie uns unter hello@freyrdigital.com, um unsere KI/ML-gesteuerten Innovationen kennenzulernen, die regulatorische Abläufe in der Medizinbranche optimieren.
Bleiben Sie mit regelmäßigen Updates und technologischen Fortschritten immer einen Schritt voraus. Arbeiten Sie mit uns zusammen, um Ihre regulatorischen Abläufe zu optimieren, die Produktivität zu steigern und die Qualität der Einreichungen zu verbessern. Fordern Sie noch heute eine Demo an und erleben Sie die perfekte Mischung aus Fachwissen und Tools. Bringen Sie Ihr Unternehmen von gut zu exzellent. Kontaktieren Sie uns noch heute.









