Ninsho (Zertifizierung von Medizinprodukten) ist ein Zertifizierungssystem durch Dritte in Japan, bei dem eine registrierte Zertifizierungsstelle (RCB), die vom Ministerium für Gesundheit, Arbeit und Soziales (MHLW) akkreditiert ist, bestimmte stark kontrollierte Medizinprodukte zertifiziert. Es gilt für Produkte der Klasse II und eine begrenzte Anzahl von Produkten der Klasse III, die einen zugehörigen japanischen Industriestandard (JIS) haben. Einige Medizinprodukte der Klasse II ohne festgelegte Zertifizierungskriterien erfordern eine Zulassung im Rahmen des Shonin-Programms.
Welche anderen Zulassungswege für Medizinprodukte gibt es in Japan?
In Japan werden neben Ninsho auch die Todokede- und Shonin-Verfahren für die Zulassung von Medizinprodukten genutzt. Je nach Risikokategorie des Produkts und der Verfügbarkeit von Vergleichsprodukten in Japan muss der Hersteller die Einreichung seines Produkts sorgfältig planen.
Welche Voraussetzungen gibt es für die Ninsho-Zertifizierung?
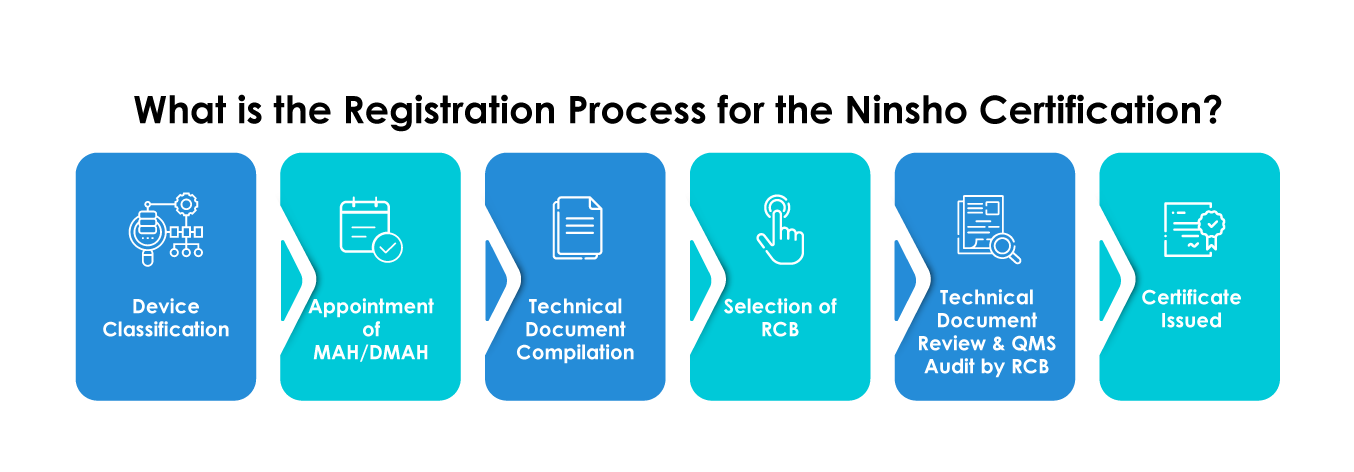
Hersteller, die ihre Produkte über das Ninsho-Verfahren registrieren, müssen die Einreichungen hinsichtlich der folgenden Punkte sorgfältig planen:
- Auswahl einer RCB
- Einreichung allgemeiner Produktdaten wie Medizinproduktkategorie, Verwendungszweck, Daten zur Wirksamkeits-Risikoanalyse, klinische Daten usw.
- Bereitstellung der Zusammenfassung der technischen Dokumentation (STED)
- Die Bereitstellung von Dokumenten sollte ausschließlich in japanischer Sprache erfolgen
- Ausländische Hersteller müssen zwingend einen Marketing Authorization Holder (MAH) oder einen Designated Marketing Authorization Holder (DMAH) ernennen.
- Ausländische Hersteller müssen sich beim MHLW registrieren und ein Foreign Manufacturer Registration (FMR)-Zertifikat für ihre Produktionsstätten erhalten.
Was sind RCBs?
Die Registered Certification Bodies (RCBs) sind von der MHLW akkreditierte Drittanbieter-Zertifizierungsstellen. RCBs sind für die Prüfung und Zertifizierung von Medizinprodukten zuständig, die für den Ninsho-Pathway in Frage kommen und unter diesem beantragt werden. RCBs sind auch für die Durchführung des QMS-Audits der Herstelleranlage verantwortlich.
Was sind die QMS-Anforderungen für die Produktregistrierung im Rahmen des Ninsho-Verfahrens?
Hersteller müssen alle QMS-Anforderungen gemäß Verordnung 169 erfüllen. Der MAH oder DMAH muss den Antrag bei den RCBs einreichen. Die RCBs führen eine detaillierte QMS-Inspektion der Herstelleranlage durch und stellen bei zufriedenstellender Umsetzung des QMS das Zertifikat aus.
Wie lange dauert die Ninsho-Zertifizierung im Durchschnitt?
Die RCB benötigt in der Regel drei (03) bis fünf (05) Monate, um die technische Bewertung abzuschließen, das QMS-Audit durchzuführen und das Ninsho-Zertifikat auszustellen.
Gibt es eine Ablaufzeit für die Ninsho-Zertifizierung?
Die Registrierung von Medizinprodukten läuft nicht ab, aber der Sponsor sollte die QMS-Zertifikate alle fünf (05) Jahre erneuern.
Japan ist nach den US und China der drittgrößte Markt für Medizinprodukte und bietet weltweit große Chancen für Hersteller von Medizinprodukten. Hersteller, die ihre Produkte in Japan vermarkten möchten, müssen die Zertifizierung und Zulassung von Medizinprodukten sorgfältig planen, da die PMDA spezifische regulatorische Anforderungen hat. Hersteller können sich für einen zuverlässigen regulatorischen Partner entscheiden, um einen problemlosen Zugang zum japanischen Markt zu erhalten.
Um mehr über die Zertifizierung von Medizinprodukten in Japan oder andere PMDA-Japan-Vorschriften zu erfahren, kontaktieren Sie Freyr noch heute!
