
Sprawy regulacyjne (RA) odgrywają kluczową rolę w zapewnieniu bezpieczeństwa, skuteczności i jakości produktów leczniczych w dynamicznym środowisku farmaceutycznym. Sprawy regulacyjne w zakresie chemii, wytwarzania i kontroli (CMC RA) są kluczowe dla zachowania zgodności. Ich celem jest ochrona zdrowia pacjentów i budowanie zaufania publicznego do produktów farmaceutycznych poprzez zapewnienie spójności i jakości w całym procesie wytwarzania leków.
CMC RA obejmuje wymagania dotyczące dokumentacji i zgodności związane z produkcją, kontrolą jakości i stabilnością produktów farmaceutycznych. Wymaga to dbałości o szczegóły i przestrzegania wytycznych regulacyjnych przez cały cykl życia rozwoju leku. Aby dowiedzieć się więcej o znaczeniu CMC RA, skonsultuj się z naszymi ekspertami.
W tym blogu zagłębimy się w podstawy CMC RA i zbadamy ich znaczenie w osiąganiu zgodności i utrzymywaniu wysokich standardów jakości.
Rola CMC w rozwoju leków
Kwestie CMC rozpoczynają się wcześnie w procesie rozwoju leku i kontynuowane są przez wszystkie etapy, od badań przedklinicznych po komercjalizację. Dane i dokumentacja CMC są kluczowymi elementami zgłoszeń regulacyjnych, takich jak wnioski o dopuszczenie nowego leku do badań klinicznych (IND), wnioski o dopuszczenie nowego leku (NDA) i wnioski o Pozwolenie na dopuszczenie do obrotu produktu leczniczego (MAA). Organy regulacyjne przeglądają dane CMC w celu oceny bezpieczeństwa, tożsamości, mocy i jakości produktu leczniczego, a także niezawodności i spójności procesu produkcyjnego.
Zapewnienie zgodności z CMC RA
Zgodność z wymogami regulacyjnymi CMC jest kluczowa dla pomyślnego wejścia na rynek. Organy regulacyjne, takie jak USFDA, EMA i inne regionalne organy ds. zdrowia (HA), są odpowiedzialne za ustanawianie wytycznych i standardów, których należy przestrzegać. Wytyczne te obejmują różne aspekty, w tym praktyki produkcyjne, systemy jakości, metody analityczne, badania stabilności i walidację. Zgodność wymaga skrupulatnej dokumentacji, przestrzegania Dobrych Praktyk Wytwarzania (GMP) oraz wdrażania skutecznych Systemów Zarządzania Jakością (QMS).
Rola zgodności CMC w sukcesie firmy farmaceutycznej
Utrzymywanie wysokich standardów zgodności CMC oferuje firmom farmaceutycznym wiele korzyści. Niektóre z kluczowych korzyści to:
- Łagodzenie ryzyka regulacyjnego.
- Wspieranie pomyślnych zatwierdzeń regulacyjnych.
- Zmniejszanie prawdopodobieństwa wycofań produktów z rynku.
- Budowanie pozytywnej reputacji w zakresie jakości i niezawodności.
Kwestie do rozważenia dla skutecznego funkcjonowania RA CMC:
- Bycie na bieżąco z wiedzą regulacyjną: Zmieniające się wymogi regulacyjne od władz zdrowotnych (HAs) wymagają bycia na bieżąco z najnowszymi wytycznymi. Ciągłe monitorowanie aktualizacji regulacyjnych i włączanie ich do praktyk CMC jest kluczowe dla zachowania zgodności.
- Ustanawianie Systemów Jakości: Obejmuje to opracowywanie i utrzymywanie kompleksowych Standardowych Procedur Operacyjnych (SOP), procedur kontroli dokumentów, procesów kontroli zmian oraz programów szkoleniowych, aby zapewnić, że pracownicy rozumieją i przestrzegają ustalonych protokołów.
- Ocena i łagodzenie ryzyka: Firmy powinny identyfikować potencjalne ryzyka na wszystkich etapach procesów rozwoju leku i produkcji oraz wdrażać odpowiednie strategie łagodzenia ryzyka. Obejmuje to ocenę krytycznych parametrów procesu, zmienności surowców, potencjalnych zanieczyszczeń i ryzyka w łańcuchu dostaw, co zapewnia zgodność z przepisami.
- Dokumentacja i integralność danych: Utrzymywanie dokładnej i kompletnej dokumentacji jest niezbędne do wykazania zgodności. Firmy muszą ustanowić solidne praktyki dokumentacyjne, w tym prowadzenie zapisów partii, danych analitycznych, badań stabilności i raportów walidacyjnych. Zapewnienie integralności, identyfikowalności i bezpieczeństwa danych jest kluczowe, aby uniknąć problemów z zgodnością.
- Skuteczne zarządzanie zmianami: Firmy muszą posiadać dobrze zdefiniowane procedury kontroli zmian w celu oceny i dokumentowania zmian, oceny ich wpływu na jakość produktu i zgodność z przepisami regulacyjnymi oraz uzyskania niezbędnych zatwierdzeń przed wdrożeniem zmian.
- Silne partnerstwa i zarządzanie dostawcami: Obejmuje to wybór kwalifikowanych dostawców, przeprowadzanie audytów oraz ustanawianie umów jakościowych, które określają obowiązki i oczekiwania. Kluczowe jest przeprowadzanie regularnych ocen zgodności dostawców z wymogami Current GMP (cGMP).
- Gotowość do Audytów i Inspekcji: Firmy powinny przeprowadzać samooceny, aby zidentyfikować obszary wymagające poprawy i zapewnić gotowość do audytów regulacyjnych. W rzeczywistości, szybkie reagowanie na ustalenia audytu i wdrażanie działań korygujących są kluczowe dla utrzymania zgodności.
- Ciągłe doskonalenie: Można to osiągnąć poprzez zachęcanie do zaangażowania pracowników, zapewnianie szkoleń i edukacji w zakresie wymogów regulacyjnych oraz wspieranie nastawienia na jakość na wszystkich poziomach organizacji.
- Zajmowanie się działaniami korygującymi i zapobiegawczymi (CAPA): Systematycznie zajmując się niezgodnościami za pomocą metodologii CAPA, firmy farmaceutyczne mogą wykazać swoje zaangażowanie w ciągłe doskonalenie i zgodność.
- Znajomość zmian regulacyjnych po zatwierdzeniu: Zrozumienie wymagań regulacyjnych dotyczących zmian po zatwierdzeniu jest kluczowe dla zapewnienia zgodności. Wdrażanie odpowiednich procesów zarządzania zmianami i skuteczna komunikacja z Urzędami (HAs) może pomóc w zarządzaniu tymi zmianami przy jednoczesnym zapewnieniu zgodności.
Rola dostawcy usług regulacyjnych w procesie zgodności CMC
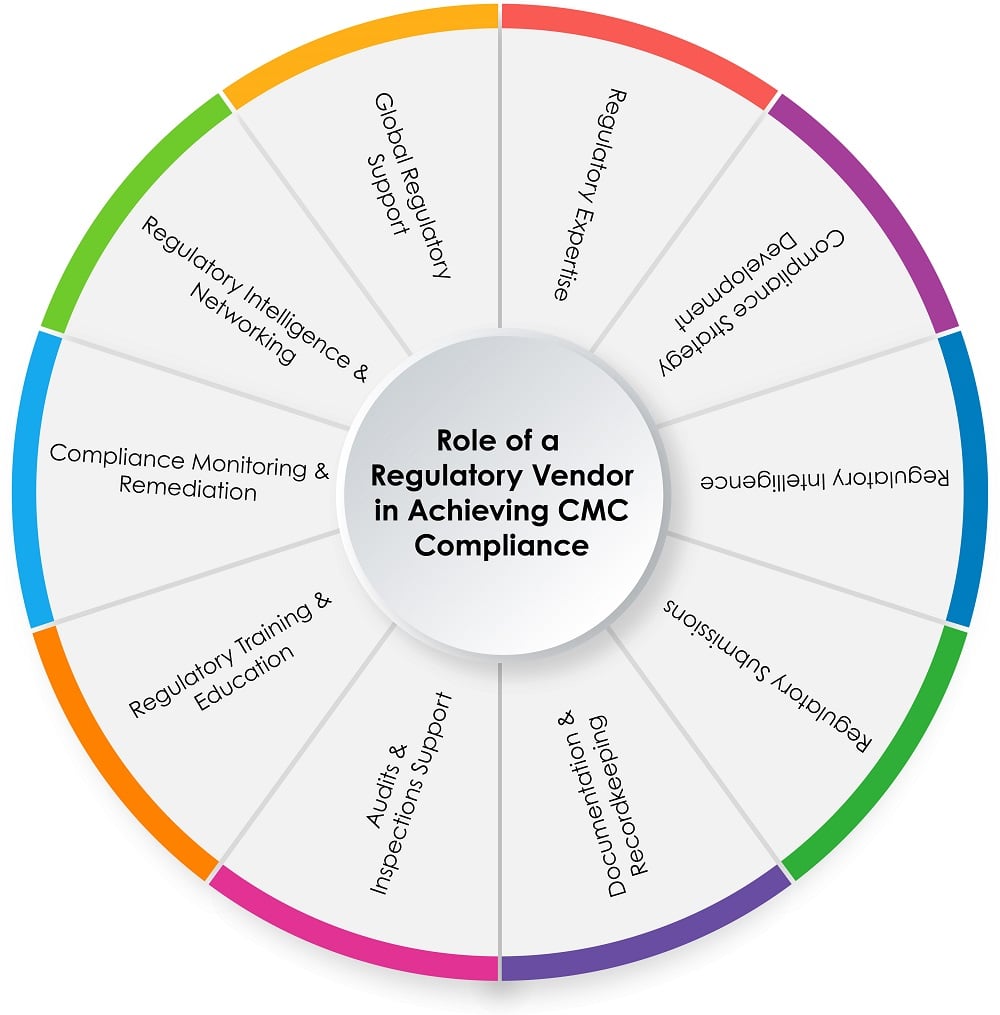
Poniższy wykres kołowy (Rysunek 1) przedstawia rolę dostawcy usług regulacyjnych w procesie zgodności CMC:
Rysunek 1: Rola dostawcy usług regulacyjnych w osiągnięciu zgodności z CMC
Podsumowanie
Osiągnięcie i utrzymanie zgodności z wymogami CMC wymaga strategicznego podejścia, które obejmuje współpracę międzyfunkcyjną, solidne systemy jakości oraz bieżącą analizę danych regulacyjnych (RI). Jest to również kluczowe dla skutecznego dostępu do rynku i ciągłej dostępności produktów. Dogłębne zrozumienie podstaw CMC RA oraz wdrożenie skutecznych strategii zgodności może pomóc firmom farmaceutycznym w poruszaniu się po środowisku regulacyjnym, uzyskiwaniu zezwoleń i utrzymywaniu najwyższych standardów jakości oraz bezpieczeństwa pacjentów. Strategiczne partnerstwa regulacyjne mogą usprawnić te kluczowe kroki, oferując najlepszą w swojej klasie wiedzę specjalistyczną w zakresie utrzymania zgodności. Skontaktuj się z nami, aby dowiedzieć się więcej o naszych usługach!









