
Administracja Produktów Leczniczych (TGA) w Australii ma rygorystyczne zasady rejestracji nowych leków na receptę z nowymi substancjami czynnymi. Niedawno TGA opracowała zmieniony proces, aby poprawić skuteczność ratujących życie leków na receptę i szybciej udostępnić je pacjentom. Zmiany te dotyczą wniosków, które muszą być poparte danymi nieklinicznymi, klinicznymi i/lub biorównoważności (kategoria 1 i kategoria 2). TGA opublikowała w sierpniu dokument zawierający szczegóły wymagań regulacyjnych w tym zakresie.
Istotne cechy w nowym procesie rejestracji leków na receptę
- TGA opracowała etapowy proces rejestracji i nazwała te etapy kamieniami milowymi. Każdy z nich podąża oddzielną ścieżką.
- Nowy proces ma na celu poprawę jakości dokumentacji. Dokumentacja jest przygotowywana w formacie wspólnego dokumentu technicznego (CTD) i jest zgodna ze wszystkimi wymogami regulacyjnymi.
- Faza planowania przed złożeniem wniosku jest istotna, ponieważ wnioskodawcy przedstawiają szczegóły dotyczące przyszłego zgłoszenia. Odbywa się to co najmniej dwa i ćwierć (02 ¼) miesiąca przed złożeniem kompletnego dossier. Celem tego etapu jest wsparcie TGA w ustaleniu dat kolejnych kamieni milowych oraz przygotowanie zasobów do zarządzania CTD.
- Kolejnym etapem jest złożenie wniosku. Po jego złożeniu TGA nie zezwala wnioskodawcy na dostarczanie żadnych dodatkowych danych ani informacji po dacie złożenia. Obowiązkowe jest złożenie kompletnego dossier, które jest poprawne i wysokiej jakości.
- Zgodnie z sekcją 31 Ustawy o Produktach Leczniczych z 1989 roku, TGA żąda dodatkowych informacji na etapie oceny. Po wstępnej ocenie wszystkie wnioski są zbierane i wysyłane do wnioskodawcy.
Aby poznać kluczowe etapy odnowionego procesu, prosimy zapoznać się z poniższymi schematami.
Etap 1
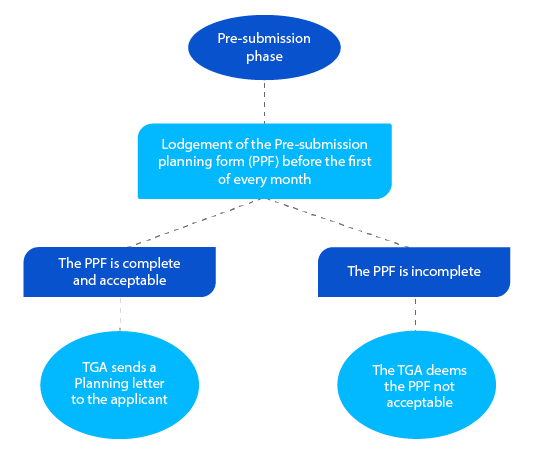
Pismo planistyczne zawiera oczekiwaną datę, w której TGA spodziewa się złożenia dossier, oraz inne docelowe daty kamieni milowych dla wniosku o lek na receptę.
Etap 2
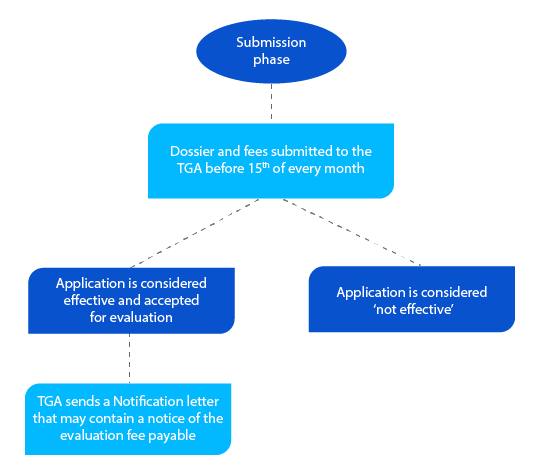
Dossier zawiera informacje, które pomagają TGA ocenić wniosek, a jeśli wszystko jest w porządku, pismo powiadamiające jest wysyłane przed końcem miesiąca, w którym wnioskodawca złożył dossier.
Etap 3
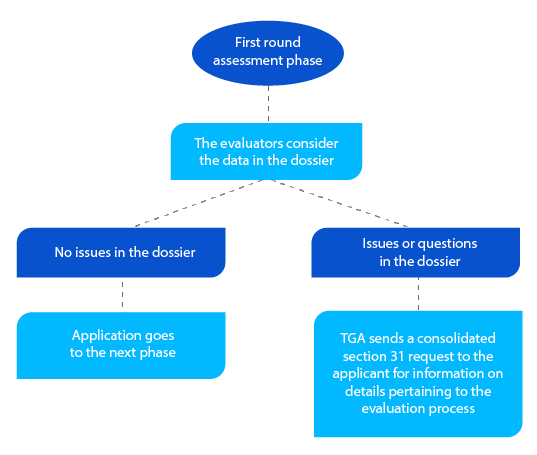
Oprócz skonsolidowanego wniosku z sekcji 31, gdy ma to zastosowanie, TGA wysyła kopie raportów z oceny przygotowanych przez oceniających jakość, badania niekliniczne, kliniczne oraz plany zarządzania ryzykiem (RMP).
Etap 4
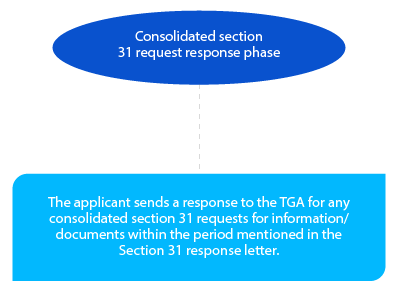
Wnioskodawca może wskazać czas na odpowiedź zgodnie z sekcją 31. Może to być trzydzieści (30) lub sześćdziesiąt (60) dni i powinno być zaznaczone w PPF. Okres ten musi zostać potwierdzony przez TGA w piśmie planistycznym (Planning Letter). Akceptowalny format odpowiedzi to CTD i musi być przesłany w formie kopii papierowej i elektronicznej.
Ponieważ jest to ostatnia szansa dla wnioskodawcy na dostarczenie TGA wszelkich brakujących informacji, musi to zostać wykonane w sposób zgodny z przepisami.
Etap 5
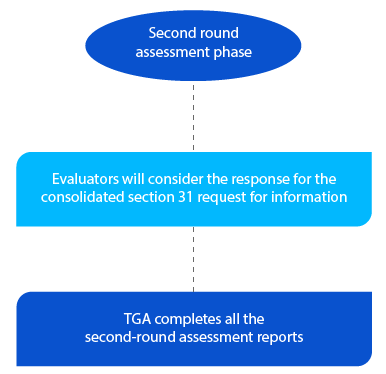
TGA ma dwa (02) miesiące na wnioski dotyczące nowych leków generycznych w drugiej rundzie raportów oceny oraz jeden (01) miesiąc na wszystkie inne typy wniosków. Raporty są wysyłane do odpowiednich wnioskodawców po zakończeniu drugiej oceny.
Etap 6
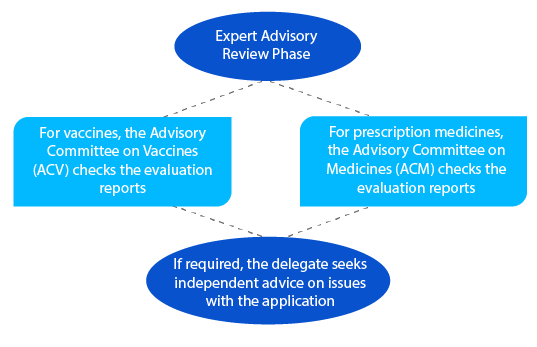
Po przeglądzie doradczym TGA wysyła powiadomienie zawierające szczegóły porady otrzymanej od ACV lub ACM.
Etap 7
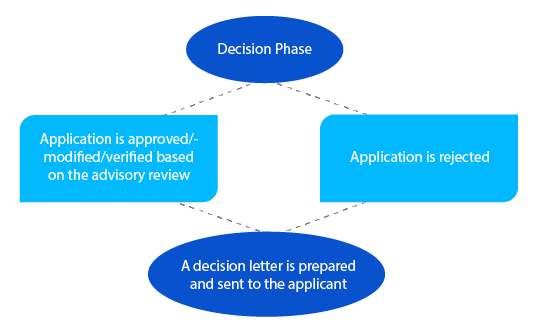
W przypadku nierozstrzygniętych kwestii, delegat może skontaktować się z wnioskodawcą na tym etapie przed podjęciem decyzji. W przypadku wniosków złożonych na podstawie sekcji 23 ustawy o produktach leczniczych z 1989 roku (nowo ocenione leki umieszczone w Australijskim Rejestrze Produktów Leczniczych (ARTG)), powiadomienie jest wysyłane do wnioskodawcy w ciągu dwudziestu ośmiu (28) dni od podjęcia decyzji.
Etap 8
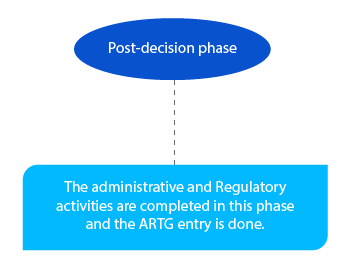
Zaległe płatności są regulowane na tym etapie. Musi to zostać zakończone do końca miesiąca następującego po decyzji delegata.
Ponieważ TGA podejmuje wszelkie środki ostrożności w celu zapewnienia bezpieczeństwa, skuteczności i jakości leków na receptę, jednocześnie skracając czas ich wprowadzania na rynek, obowiązek złożenia odpowiednich zgłoszeń w celu sprawnego procesu rejestracji spoczywa na wnioskodawcy. Na każdym etapie idealną sytuacją jest współpraca z kompleksowym dostawcą usług regulacyjnych, który jest ekspertem w rejestracji leków na receptę. Skontaktuj się z doświadczonym podmiotem regulacyjnym, aby uzyskać ścieżkę zgodności; bądź na bieżąco i zachowaj zgodność.










