
Niezaspokojona potrzeba medyczna (UMN) to jeden z najpilniejszych priorytetów systemów opieki zdrowotnej. Stale rozwijająca się nauka i technologia w dziedzinie opieki zdrowotnej stworzyły potencjał do badania różnych opcji terapeutycznych. Organy ds. zdrowia zachęcają do innowacyjnych terapii, które obiecują znaczące korzyści dla jakości życia pacjentów. Opierając się na priorytetowym traktowaniu innowacji i ukierunkowaniu na niezaspokojone potrzeby pacjentów w rozwoju leków, Europejska Agencja Leków (EMA) wprowadziła w 2016 roku ścieżkę PRIority MEdicines (PRIME). Od tego czasu ścieżka PRIME stała się metodą udzielania pozwoleń na innowacyjne terapie w przyspieszonym tempie. Ten rodzaj ułatwionej ścieżki może być rozważany przez każdą firmę, od start-upów, przez średnie firmy biotechnologiczne, po duże międzynarodowe organizacje. Jednakże kwalifikacja do tej ścieżki jest ograniczona do produktów w fazie rozwoju, które jeszcze nie ubiegały się o Pozwolenie na dopuszczenie do obrotu produktu leczniczego w ramach procedury scentralizowanej. Kryteria kwalifikacyjne są stosowane rygorystycznie. Między marcem 2016 a kwietniem 2022 roku, tylko 24% wniosków otrzymało pozytywną opinię, podczas gdy 72% wniosków PRIME zostało odrzuconych. Spośród 24% wybranych do ścieżki PRIME, większość należała do obszaru terapeutycznego onkologii.
Innowatorzy ubiegający się o pozwolenia na dopuszczenie do obrotu leków na rzadkie choroby lub leków sierocych często mogą dysponować ograniczonymi zbiorami danych jako dowodami na poparcie swoich wniosków o nowe leki, zgodnie z wymogami organów regulacyjnych. Wnioski o dopuszczenie do obrotu zaawansowanych terapii leczniczych (ATMP) i leków sierocych zazwyczaj napotykają takie wyzwania. Ze względu na ograniczone dane dotyczące populacji pacjentów, zachęca się do stałej interakcji z organami regulacyjnymi, aby uzyskać lepszy wgląd w wymagania dotyczące przeglądu naukowego i zatwierdzenia. Ścieżka PRIME może być przydatna w przypadku takich terapii ze względu na wczesne zaangażowanie organów regulacyjnych w zapewnianie proaktywnego wsparcia i wskazówek w zakresie gromadzenia danych oraz oceny korzyści i ryzyka.
Zalety podążania ścieżką PRIME
- Pomaga innowatorom w opracowaniu dobrze przygotowanego planu rozwoju.
- Przynosi korzyści innowatorom poprzez angażowanie organów ds. zdrowia na wczesnym etapie rozwoju; przyczynia się to do opracowywania wysokiej jakości wniosków o dopuszczenie do obrotu.
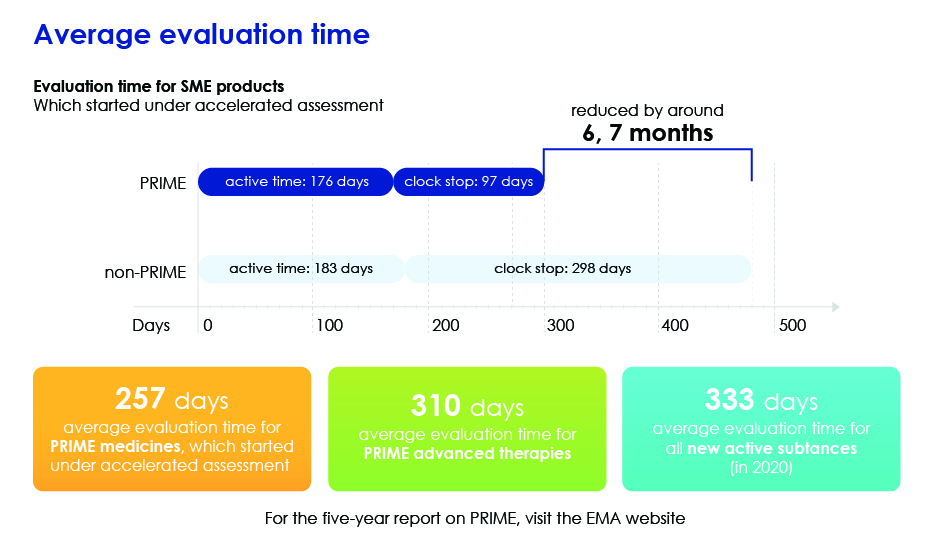
- Przyspiesza ogólną ocenę poprzez skrócenie średniego czasu oceny, dzięki czemu leki mogą szybciej dotrzeć do pacjentów.
- Wspieramy innowatorów, aby skupili się na rozwoju leków w celu poprawy wyników leczenia pacjentów i zaspokojenia niezaspokojonych potrzeb pacjentów.
Czas oceny szczegółowo
Wnioski dla ścieżki PRIME
Ścieżka PRIME priorytetowo traktuje niezaspokojone potrzeby medyczne. Spośród 384 wniosków PRIME otrzymanych od marca 2016 r., tylko 18 uzyskało Pozwolenie na dopuszczenie do obrotu produktu leczniczego do czerwca 2021 r.

Czy jesteś gotowy na PRIME?
Istnienie ścieżki PRIME wynika ze znaczących niezaspokojonych potrzeb medycznych oraz z dążenia do wypełnienia luk przez Europejską Sieć Regulacji Leków (EMRN). Aby ocenić przydatność produktu do ścieżki PRIME, należy wziąć pod uwagę następujące kwestie:
- Ustalenia: Wnioskodawcy muszą wskazać niezaspokojoną potrzebę medyczną i przedstawić przekonujący argument, jak ich produkt rozwiąże ten problem.
- Potencjał: Wnioskodawcy muszą wykazać korzystny potencjał terapii w kryteriach niezaspokojonej potrzeby medycznej.
- Dane przedkliniczne: Wnioskodawcy muszą przedstawić dane dotyczące skuteczności lub działania terapii w ludzkim układzie biologicznym. Modele niekliniczne, niezależnie od ich dokładności, nie zapewniają dokładnego obrazu jej zachowania w ludzkim układzie biologicznym.
- Etap rozwoju: Wnioskodawca musi określić właściwy etap, aby wejść na ścieżkę PRIME w celu uzyskania optymalnych wskazówek od organów regulacyjnych i kontynuować proces składania wniosku.
Po przyznaniu grantu PRIME.
Gdy wnioskodawca otrzyma możliwość skorzystania z uproszczonej ścieżki, EMA będzie:
- Wyznaczenie sprawozdawcy z Komitetu ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) lub Komitetu Terapii Zaawansowanych (CAT) w przypadku terapii zaawansowanych.
- Zorganizuj spotkanie inauguracyjne z referentem CHMP/CAT oraz multidyscyplinarną grupą ekspertów, aby uzyskać wskazówki dotyczące ogólnego planu rozwoju i strategii regulacyjnej.
- Należy wyznaczyć jedną osobę kontaktową dla wnioskodawcy.
- Udzielanie porad naukowych na każdym kluczowym etapie rozwoju, angażując dodatkowych interesariuszy, takich jak organy oceny technologii medycznych – w celu przyspieszenia dostępu pacjentów do nowego leku.
- Potwierdź możliwość przyspieszonej oceny w momencie składania wniosku, przy jednoczesnym rozważeniu Pozwolenia na dopuszczenie do obrotu produktu leczniczego.
Czy Twoja aplikacja do ścieżki PRIority MEdicine (PRIME-ready) jest gotowa? Skontaktuj się z Freyr już dziś i dokonaj oceny. Dowiedz się więcej o tym, jak możemy pomóc w Twojej strategii regulacyjnej i uzyskaniu statusu PRIME. Bądź na bieżąco. Zachowaj zgodność.









