
Innowacje w połączeniach leków z wyrobami medycznymi doprowadziły do znaczących postępów w opiece nad pacjentem. Produkty lecznicze w połączeniu z wyrobami medycznymi oferują ukierunkowane dostarczanie leków, lepsze wyniki terapeutyczne i zwiększoną zgodność pacjenta z leczeniem. Jednak poruszanie się w otoczeniu regulacyjnym dla połączeń leków z wyrobami medycznymi może być skomplikowane.
Ten blog omówi kwestie do rozważenia i wyzwania związane z działaniami regulacyjnymi dla produktów złożonych z leku i wyrobu medycznego, oferując wgląd w usprawnienie tych procesów.
Przegląd i ramy regulacyjne dla produktów złożonych lek-wyrób medyczny
Produkty złożone z leku i wyrobu medycznego łączą efekty terapeutyczne leków farmaceutycznych z możliwościami dostarczania wyrobów medycznych. Kombinacje leków i wyrobów medycznych obejmują stenty uwalniające leki, inhalatory i urządzenia oddechowe, plastry transdermalne, systemy dostarczania insuliny, systemy infuzyjne leków oraz balony pokryte lekiem. Ukierunkowane dostarczanie, zwiększona skuteczność, poprawa przestrzegania zaleceń przez pacjenta oraz precyzyjna kontrola nad leczeniem to niektóre z godnych uwagi cech tych produktów.
Organy regulacyjne, takie jak amerykańska Agencja Żywności i Leków (US FDA), Europejska Agencja Leków (EMA) i inne, ustanowiły wytyczne dotyczące połączeń leków i wyrobów medycznych. W ostatnich latach nastąpiły znaczące zmiany w obszarze regulacyjnym, ze zwiększonym naciskiem na harmonizację, oceny oparte na ryzyku oraz nadzór po wprowadzeniu do obrotu.
Kluczowe kwestie dotyczące operacji regulacyjnych
Poniżej szczegółowo opisano niektóre kwestie, które należy wziąć pod uwagę podczas zarządzania operacjami regulacyjnymi dotyczącymi produktów złożonych lek-wyrób medyczny:
Zrozumienie klasyfikacji produktów i ścieżek regulacyjnych.
Zrozumienie klasyfikacji produktów złożonych z leku i wyrobu medycznego oraz wybór odpowiedniej ścieżki regulacyjnej jest kluczowe. Producenci muszą określić, czy jest to produkt złożony z leku i wyrobu medycznego, kategoria wyrobów medycznych pokrytych lekiem, czy kategoria produktów pakowanych razem. Wybór właściwej ścieżki dla konkretnego typu produktu jest niezbędny do skutecznego wprowadzenia go na rynek.
Spełnianie wymagań naukowych i technicznych
Obejmuje to zapewnienie zgodności między składnikami leku a wyrobu, przeprowadzanie badań stabilności w celu oceny okresu przydatności produktu do użycia, walidację procesów produkcyjnych oraz wdrażanie ocen ryzyka w celu identyfikacji i łagodzenia potencjalnych zagrożeń.
Opieka nad pacjentem i testy użyteczności
Opieka nad pacjentem i inżynieria użyteczności odgrywają znaczącą rolę w rozwoju takich produktów złożonych. Uwzględnienie czynników takich jak interfejs użytkownika, ergonomia, obsługa urządzenia i przestrzeganie zaleceń przez pacjenta podczas opracowywania produktu pomaga zapewnić jego bezpieczne i skuteczne stosowanie przez pacjentów i pracowników służby zdrowia z minimalną liczbą błędów.
Kwestie do rozważenia po wprowadzeniu na rynek
Obowiązki pomarketingowe są kluczowym aspektem zgodności regulacyjnej dla produktów złożonych (lek-wyrób medyczny). Producenci muszą ustanowić procesy zgłaszania zdarzeń niepożądanych, nadzoru po wprowadzeniu do obrotu oraz zgłaszania działań w ramach nadzoru nad bezpieczeństwem, aby monitorować bezpieczeństwo i działanie swoich produktów.
Bądź na bieżąco z najnowszymi wytycznymi i aktualizacjami regulacyjnymi
Śledzenie najnowszych wytycznych i aktualizacji jest kluczowe dla zapewnienia zgodności i dostosowania strategii regulacyjnych do obecnych oczekiwań. Środowisko regulacyjne dla produktów złożonych (lek-wyrób medyczny) stale ewoluuje. Dostosowanie się do wytycznych FDA, rozporządzenia UE w sprawie wyrobów medycznych (MDR) oraz Międzynarodowej Rady ds. Harmonizacji Wymagań Technicznych dla Produktów Farmaceutycznych do Stosowania u Ludzi (ICH) może pomóc producentom w utrzymaniu zgodności.
Najlepsze praktyki usprawniania działań regulacyjnych
Aby zoptymalizować działania regulacyjne dla produktów złożonych lek-wyrób medyczny, firmy farmaceutyczne mogą stosować najlepsze praktyki przedstawione na poniższym wykresie kołowym:
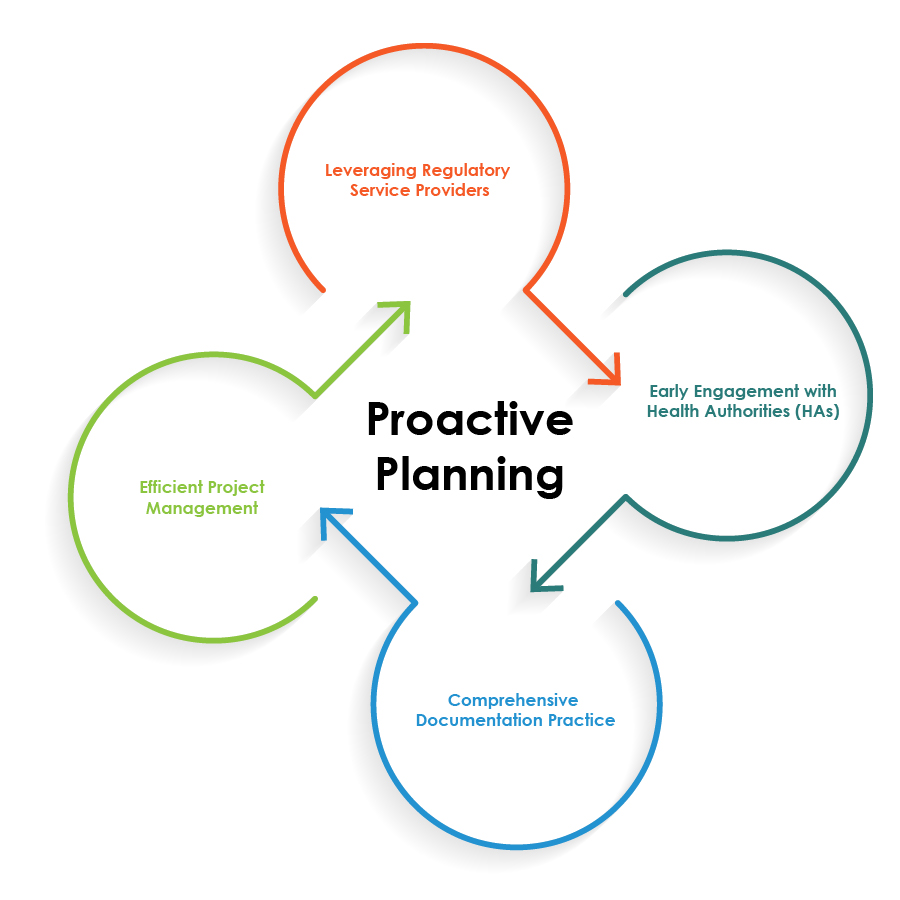
Proaktywne planowanie jest kamieniem węgielnym dla płynnych operacji regulacyjnych dotyczących produktów złożonych leków i wyrobów medycznych.
Przyszłe trendy i wyzwania
Śledzenie przyszłych trendów i niedociągnięć jest kluczowe dla firm farmaceutycznych i specjalistów ds. regulacji zaangażowanych w operacje regulacyjne dotyczące tych produktów. Poniżej przedstawiono kilka trendów i wyzwań, na które należy zwrócić uwagę:
- Nowe technologie: Nanotechnologia, druk 3D i powiązane zastosowania wpływają na rozwój innowacyjnych kombinacji leków i wyrobów medycznych. Te trendy technologiczne oferują ukierunkowane dostarczanie leków, medycynę spersonalizowaną i ulepszone monitorowanie pacjentów. Jednakże stwarzają one również unikalne wyzwania regulacyjne związane z bezpieczeństwem, skutecznością i kontrolą jakości.
- Cyberbezpieczeństwo: Wraz ze wzrostem łączności wyrobów medycznych, zapewnienie bezpieczeństwa danych i ochrona przed zagrożeniami cybernetycznymi staje się sprawą najwyższej wagi. Wdrożenie solidnych środków cyberbezpieczeństwa i bycie na bieżąco z najlepszymi praktykami w zakresie bezpieczeństwa urządzeń to kluczowe kwestie dla działań regulacyjnych.
- Różnorodne wyzwania: Obejmują one złożoności globalnego łańcucha dostaw, takie jak pozyskiwanie surowców, dostępność komponentów i procesy produkcyjne, co stwarza wyzwania w utrzymaniu zgodności regulacyjnej i zapewnieniu jakości produktu. Solidne praktyki zarządzania łańcuchem dostaw, oceny ryzyka i nadzór nad dostawcami są kluczowe dla sprostania tym wyzwaniom i ograniczenia związanego z nimi ryzyka.
Poruszanie się w krajobrazie regulacyjnym produktów złożonych lekowo-urządzeniowych wymaga kompleksowego zrozumienia ram regulacyjnych, najnowszych wytycznych i najlepszych praktyk. Rozważenie kluczowych kwestii, bycie na bieżąco ze zmianami i wdrażanie najlepszych praktyk pomoże firmom farmaceutycznym w usprawnieniu ich działań regulacyjnych. Współpraca z dostawcami usług regulacyjnych pozwala firmom wykorzystać specjalistyczną wiedzę i doświadczenie oraz zoptymalizować ich szanse na sukces regulacyjny w tej ewoluującej i wymagającej dziedzinie. Dzięki naszemu sprawdzonemu doświadczeniu w przestrzeganiu globalnych norm regulacyjnych, Freyr może pomóc w zapewnieniu zgodności produktu na każdym etapie. Aby dowiedzieć się więcej, skontaktuj się z nami.









