
Aby zwiększyć dostępność innowacyjnych leków dla pacjentów w Wielkiej Brytanii po Brexicie, w styczniu 2021 roku uruchomiono nową i przyspieszoną ścieżkę zatwierdzania, znaną jako Innowacyjna Ścieżka Licencjonowania i Dostępu (ILAP). Jej głównym celem było zapewnienie zintegrowanej mapy drogowej dla wszystkich zainteresowanych stron, która usprawnia proces rozwoju produktu. ILAP dodatkowo wspiera deweloperów komercyjnych i niekomercyjnych, ułatwiając dostęp do innowacyjnych leków dla populacji pacjentów poprzez skrócenie czasu wprowadzenia na rynek. Firmy farmaceutyczne mogą rozważyć ILAP jako drogę, gdy dane niekliniczne zostaną skonsolidowane. Ma zastosowanie do Nowych Jednostek Chemicznych (NCE), leków biologicznych, nowych wskazań i leków zmienionych przeznaczeniem.
ILAP to inicjatywa opracowana wspólnie przez Agencję Regulacji Leków i Produktów Opieki Zdrowotnej (MHRA) we współpracy z All-Wales Therapeutics and Toxicology Centre (AWTTC), National Institute of Health and Care Excellence (NICE) oraz Scottish Medicines Consortium (SMC) jako stałymi partnerami. Partnerzy wspierający ILAP to National Health Service England (NHS), Health Research Authority (HRA) i National Institute for Health Research (NIHR). Wspólnie, interesariusze zapewniają wzmocnione wkłady regulacyjne, naukowe, etyczne i komercyjne na wczesnym etapie rozwoju leków podczas badań klinicznych.
Zdaniem Freyr, ILAP oferuje wspaniałe możliwości dla twórców innowacyjnych terapii, zwłaszcza tych, którzy odpowiadają na niezaspokojone potrzeby pacjentów. Za stosunkowo niewielką opłatą (około 8000 GBP) firma mogłaby uzyskać porady na wczesnym etapie, uzyskać oznaczenie dla swojego produktu i uzgodnić docelowy profil rozwoju. Ma to potencjał, aby zaoszczędzić znaczną ilość czasu w całym cyklu życia produktu. Istnieją również korzyści w wybieganiu poza Pozwolenie na dopuszczenie do obrotu produktu leczniczego i wczesnym przygotowaniu się do negocjacji dotyczących refundacji.
ILAP wypada korzystnie w porównaniu z podobnymi programami oferowanymi w ramach europejskiej sieci leków (takimi jak PRIME). Chociaż różni się koncepcją i realizacją, ILAP ma szersze kryteria akceptacji i wyższy wskaźnik akceptacji. ILAP zapewnia również ścieżkę integracji z projektem Project Orbis amerykańskiej Agencji ds. Żywności i Leków (USFDA) dla nowo powstających produktów onkologicznych.
Jak złożyć wniosek o ILAP?
Aby uzyskać dostęp do ILAP, wnioskodawcy muszą ubiegać się o Paszport Innowacji (IP). Uzyskanie statusu IP umożliwia producentom leków dostęp do ścieżki w oparciu o dowody wymagane, aby produkt spełniał kryteria kwalifikacyjne określone przez NICE, SMC, AWTTC i MHRA.
To oznaczenie działa jako katalizator dla innowacyjnych produktów od etapu przedklinicznego do środkowego etapu rozwoju. IP może prowadzić do zdefiniowania dokumentu Profilu Rozwoju Docelowego (TDP). TDP to mapa drogowa, która ułatwia dostęp do partnerów ILAP na wczesnych etapach cyklu życia rozwoju leku, aby przyspieszyć i usprawnić dostęp pacjentów do nowych i innowacyjnych terapii. Pacjenci są częścią całego tego procesu. Kilka narzędzi dostarczanych przez ILAP wspiera wnioskodawców na wszystkich etapach procesu projektowania, rozwoju i zatwierdzania.
Kryteria wyznaczenia paszportu innowacyjnego
Wytyczne MHRA wyjaśniają kryteria dla oznaczenia IP. Jest to szczególnie istotne dla innowacyjnych produktów i korzystnie wypada w porównaniu z równoważnymi programami oferowanymi w Europie.
W przyszłości, specyficzne zastosowanie IP dla wyrobów medycznych i produktów złożonych, obszarów, w których zawsze występuje znacząca innowacja, może okazać się korzystne.
Oznaczenie IP jest oceniane przez stałych i wspierających partnerów na podstawie następujących kryteriów:
- Kryterium 1: Szczegóły dotyczące stanu, pacjenta lub obszaru zdrowia publicznego
- W przypadku stanów zagrażających życiu i poważnych schorzeń
- W sytuacji, gdy potrzeba jest kluczowa dla pacjentów
- Kryterium 2: Produkt leczniczy spełnia jeden lub więcej określonych obszarów, które obejmują
- Innowacyjna medycyna
- Lek związany z nowym wskazaniem
- Lek na rzadką chorobę
- Lek w fazie rozwoju w celu ochrony zdrowia publicznego w Wielkiej Brytanii.
- Kryterium 3: Lek ma potencjał, aby oferować
- Krótki opis korzyści, jakie proponowany lek lub wskazanie przyniesie pacjentom.
- Opinie pacjentów lub organizacji pacjentów są mile widziane.
Po złożeniu wniosku IP odbywa się spotkanie między wnioskodawcami a MHRA w celu ustalenia, czy produkt spełnia trzy (03) kryteria.
Zgodnie z najnowszymi informacjami ze stycznia 2022 roku, MHRA otrzymała siedemdziesiąt jeden (71) wniosków, z czego czterdzieści jeden (41) zakończyło się nadaniem statusu IP, dwadzieścia dwa (22) są w trakcie przetwarzania, a siedem (07) wniosków zostało odrzuconych.
Poniżej wskazano odpowiedni czas na przystąpienie do ILAP.
- Na wczesnym do średniego etapu rozwoju produktu
- Gdy dostępne są odpowiednie dane
- Gdy wnioskodawcy czują potrzebę uzyskania opinii od interesariuszy
- Wnioskodawcy dążą do przyjęcia nowych, innowacyjnych podejść
- Nie wtedy, gdy produkt jest pod koniec etapu rozwoju
Przegląd rozwoju leków
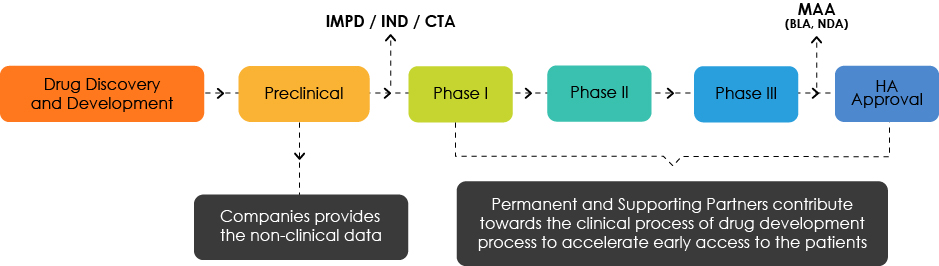
Zrozumienie Docelowego Profilu Rozwoju (TDP)
Eksperci TDP analizują cechy produktu i wskazują niedociągnięcia z punktu widzenia regulacyjnego. Odpowiadają za wskazywanie producentom leków ścieżki, która zapewnia wczesny dostęp pacjentów do ich produktów.
TDP to dokument aktualizowany w czasie rzeczywistym zgodnie z wymaganiami związanymi z rozwojem produktu. Dlatego produkt podlega wielu zmianom TDP w miarę generowania nowych danych.
Dostęp pacjentów do niezbędnych leków może być zagrożony przez opóźnienia rynkowe. Aby uniknąć takich scenariuszy, przyspieszone ścieżki działają jako katalizator. ILAP jest przykładem elastycznej ścieżki autoryzacji, która jest dobrze akceptowana w całej branży i może przyspieszyć harmonogram rozwoju innowacyjnych leków. Szczegółowe kryteria określone przez brytyjski system opieki zdrowotnej pozwalają wnioskodawcom zbadać ich kwalifikowalność do ubiegania się o oznaczenie IP. Zachęcanie do zaspokajania niezaspokojonych potrzeb klinicznych i pacjentów za pomocą przyspieszonych ścieżek, takich jak ILAP, ułatwia wejście na rynek i może przynieść ulgę zagrożonym populacjom pacjentów. Aby chronić interesy pacjentów, organy ds. zdrowia nie idą na kompromis w kwestii bezpieczeństwa, skuteczności ani jakości produktu, jednocześnie zapewniając przyspieszony proces zatwierdzania. End-to-End usługi regulacyjne Freyr ułatwiają proces dokumentacji w celu wsparcia oznaczenia Innovative Passport w przyspieszonym czasie, pomagając Twoim produktom dotrzeć do pacjentów wcześniej. Skontaktuj się z Freyr.










