
OSIĄGNIĘCIE TERMINU ZGODNOŚCI Z IDMP DO LIPCA 2016: NIEBANALNE PRZEDSIĘWZIĘCIE
Istnieje wiele pytań dotyczących IDMP, np.: gdzie w organizacji znajdują się dane? Czy wymagane jest czyszczenie i ujednolicenie obecnych danych? Jak firmy organizują te dane w celu łatwego wyszukiwania i przesyłania? Czy organizacja posiada procesy, które mogą skorzystać z centralnego repozytorium?
Osiągnięcie zgodności z Identyfikacją Produktów Leczniczych (IDMP) nie jest zadaniem trywialnym; działanie to musi uwzględniać różne presje regulacyjne i operacyjne. Organizacje muszą poczekać, aż władze wydadzą ostateczne wytyczne i zatwierdzą specyfikacje. Jednocześnie, czekanie na te wytyczne może nie pozostawić im wystarczająco dużo czasu na uporządkowanie swoich spraw.
IDMP to złożony standard mający szerokie implikacje dla danych, wymagający współpracy i kooperacji między wieloma jednostkami międzyfunkcyjnymi. Przejście to daje możliwość kompleksowego (End-to-End) spojrzenia na procesy biznesowe organizacji i możliwości IT w wielu jednostkach funkcjonalnych. Pomaga również w ustanowieniu solidnego systemu zarządzania zmianami.
Organizacje muszą zrozumieć, że dobra architektura informacji wymaga wysiłku i czasu, a także muszą uznać, że IDMP to nie tylko większy XEVMPD. Ważne jest również, aby pamiętać, że wytyczne ICH to tylko część historii, a dostępność regionalnych wytycznych jest kluczowa. Należy również wziąć pod uwagę, że równoległe wdrożenia regionalne będą miały różne zakresy i różne ramy czasowe, z szerokim zakresem podmiotów dostarczających dane.
Ponadto, firmy farmaceutyczne zamierzające wprowadzać produkty na rynki w regionach regulowanych muszą spełnić wymogi IDMP począwszy od 2016 roku. Niedawno EMA zorganizowała Dzień Informacyjny IDMP i przedstawiła swój status wdrożenia IDMP na wysokim poziomie oraz harmonogramy. Po dyskusjach z branżą farmaceutyczną, dostawcami oprogramowania oraz analizie własnych systemów i dostępności zasobów, EMA zaplanowała podzielenie całego wdrożenia EU-IDMP na wiele iteracji. Plan ten zostanie przedstawiony Komisji Europejskiej (KE) do zatwierdzenia, a jeśli uda im się przekonać KE, wdrożenie IDMP w UE zostanie rozłożone na lata 2016-2018. W najgorszym przypadku, jeśli KE się nie zgodzi, nie ma planu B. Kary za niezgodność wynoszą do 5% przychodów organizacji; brak dobrego rozwiązania dla początkowej i bieżącej zgodności z IDMP to ryzyko, na które żadna firma farmaceutyczna nie może sobie pozwolić.
IDMP: OPRACOWANE JAKO GLOBALNY ZBIÓR STANDARDÓW ZGODNIE Z ISO
W przypadku konieczności wprowadzenia jakichkolwiek przepisów dotyczących identyfikacji Produktów leczniczych w którymkolwiek z krajów ISO, zostanie to dokonane w oparciu o standardy ISO IDMP. Gdy różne regiony przyjmą standardy IDMP, wprowadzanie danych będzie spójne, a globalne firmy i organy regulacyjne będą miały dostęp do danych w celu weryfikacji spójności w różnych regionach. Ponadto, wspólne, kontrolowane słowniki znacznie ułatwią ten proces.
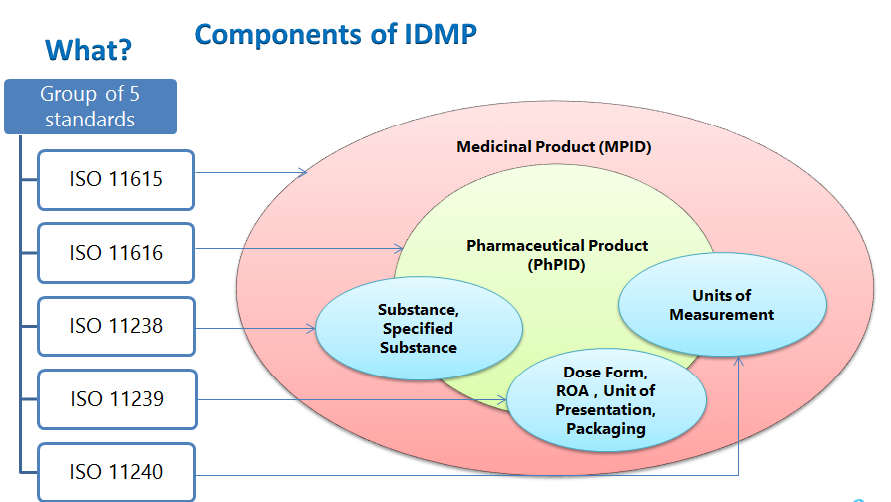
Elementy strukturalne IDMP obejmują identyfikator produktu leczniczego, identyfikator produktu farmaceutycznego, identyfikator substancji, kontrolowane słownictwo – postać dawkowania, drogę podania, składniki opakowania, jednostki prezentacji, jednostki miary oraz opis procesu produkcyjnego, który należy złożyć.
STANDARDY IDMP
- ISO 11615 – Informacje o produkcie leczniczym
- ISO 11616 – Informacje o produkcie farmaceutycznym
- ISO 11238 – Substancje
- ISO 11239 – Farmaceutyczne postacie dawkowania, Jednostki prezentacji, Drogi podania i Opakowania
- ISO 11240 – Jednostki miary
OBECNY STATUS
ICH przygotowuje przewodniki wdrożeniowe i dokonuje rewizji norm ISO.
Regulatorzy UE przygotowują się na IDMP
- EMA rozpoczęła prace w celu nawiązania współpracy z europejską siecią regulacyjną, aby zdefiniować uzasadnienia biznesowe dla danych IDMP
- EMA tworzy “Grupa zadaniowa UE ds. ISO IDMP” rekrutowanie ekspertów z Komitetów EMA oraz z Rady ds. Danych Sieci UE w celu osiągnięcia tego. W szczególności będzie to:
- Zdefiniuj obowiązkowe i opcjonalne elementy danych ISO IDMP
- Zdefiniuj zasady biznesowe dla opcjonalnych elementów danych
- Zdefiniuj zgodność i typy danych
- Zdefiniuj modele zarządzania w UE
Stanowisko US organów regulacyjnych
- Aktywne przywództwo w rozwijaniu IDMP we współpracy z globalnymi (byłymi ICH) organami regulacyjnymi i z ISO
INNE ORGANY REGULACYJNE
- Szwajcaria – Zamierza wdrożyć po UE (szybki naśladowca)
- Japonia i Kanada nominowały organy regulacyjne na ekspertów do grupy ds. Substancji IG
OSI CZASOWE
EUROPEJSKIE WYTYCZNE WDROŻENIOWE
- Rozpoczęto prace nad projektem przewodników wdrożeniowych, a przewodniki będą dostępne od I kwartału 2016 r.
INNE
- FDA nie podała jeszcze daty, ale zamierza rozwijać SPL w miarę potrzeb
- Japonia – Niepewna w ICH, ale obecnie współpracuje w ramach grupy Regulatora i ISO
- Kanada – Oczekuje się wdrożenia, ale brak jeszcze szczegółów
- Szwajcaria – Brak aktualizacji
ZROZUMIENIE WYMOGÓW ZGODNOŚCI Z IDMP
IDMP wymaga informacji o produktach leczniczych w postaci zestawu standardowych identyfikatorów, które są zbudowane na hierarchii identyfikacji stworzonej podczas budowania słownika produktów leczniczych EudraVigilance (EVMPD) lub w jego rozszerzonej formie (xEVMPD). Nastąpi nakładanie się informacji z tymi złożonymi w zgłoszeniach Structured Product Labeling (SPL) w US i innych globalnych rejestrach produktów.
Jednakże IDMP wprowadza nowe identyfikatory, nowe kategorie i nowe sposoby wyrażania relacji między elementami w modelu danych. IDMP musi być zintegrowane z DNA organizacji, ponieważ musi napędzać tworzenie modeli danych w całym przedsiębiorstwie. Infrastruktura IT organizacji może następnie rozpoznawać je w wielu systemach, procesach biznesowych i jednostkach funkcjonalnych, takich jak RA, bezpieczeństwo, R&D, dokumentacja i procesy produkcyjne.
WYZWANIA ZWIĄZANE Z ZGODNOŚCIĄ Z IDMP
Organizacyjne
- Dane rozproszone między wieloma działami
- Wymagane jest wsparcie ze strony kadry kierowniczej w celu zachęcenia do udziału
Techniczny
- Odkrywanie, gromadzenie i konsolidacja, czyszczenie danych
- 250 do 300 pól na produkt
Koordynacja
- Zarządzanie ciągłymi zmianami
- Koordynacja między wieloma zespołami
- Zapewnienie zgodności danych z przepisami za pomocą wewnętrznego procesu
PODSUMOWUJĄC:
IDMP: WPŁYW NA PRZEMYSŁ FARMACEUTYCZNY
Oczekuje się, że wdrożenie standardów IDMP wpłynie na przygotowanie i planowanie zgłoszeń oraz utrzymanie danych w całej firmie, w tym danych produkcyjnych i ustrukturyzowanych informacji o substancjach do informacji rejestracyjnych.
STANDARD IDMP: ZYSKI Z EFEKTYWNOŚCI ZAPEWNIONE PO WDROŻENIU
Zapewnienie gotowości organizacji na wyzwanie IDMP będzie wymagało ścisłej współpracy między wieloma działami w organizacji. Kompetentny dostawca usług z wyłącznym portfolio kompetencji regulacyjnych może pomóc w osiągnięciu zgodności z IDMP, co z kolei może pomóc organizacji reagować na nowe, pojawiające się możliwości na rynku.










