
Rynek farmaceutyczny w Malezji stanowi rozwijające się centrum w Azji Południowo-Wschodniej, oferujące ogromne możliwości dla międzynarodowych przedsiębiorstw. Wraz z rosnącym zapotrzebowaniem na wysokiej jakości opiekę zdrowotną oraz coraz bardziej usystematyzowanymi ramami prawnymi rynek farmaceutyczny w Malezji staje się atrakcyjnym miejscem zarówno dla producentów leków generycznych, jak i leków innowacyjnych.
Przegląd rynku malezyjskiego: obiecujące perspektywy na malezyjskim rynku farmaceutycznym
Zarówno leki generyczne, jak i nowe substancje chemiczne (NCE) mają przed sobą świetlaną przyszłość na malezyjskim rynku farmaceutycznym, który stanowi szybko rozwijającą się branżę w Azji Południowo-Wschodniej. Kraj ten oferuje dynamiczne warunki dla firm farmaceutycznych dzięki rosnącej liczbie ludności i zwiększającym się zapotrzebowaniu na opiekę zdrowotną. Branża opieki zdrowotnej stanowi lukratywny rynek dla farmaceutyków, ponieważ jest dobrze ugruntowana i dysponuje placówkami medycznymi na najwyższym poziomie.
Rynek farmaceutyczny w Malezji charakteryzuje się rosnącym popytem na nowe leki, zwłaszcza w takich obszarach terapeutycznych jak cukrzyca, choroby układu krążenia i onkologia. Otoczenie regulacyjne stało się bardziej uporządkowane, z precyzyjnymi zasadami zatwierdzania produktów i wprowadzania ich na rynek, podczas gdy rząd nadal koncentruje się na poprawie publicznej opieki zdrowotnej i dostępu do leków.
Proces rejestracji w Malezji:
Proces rejestracji produktów farmaceutycznych w Malezji podlega nadzorowi Krajowej Agencji Regulacyjnej ds. Produktów Farmaceutycznych ( NPRA), która odpowiada za zapewnienie bezpieczeństwa, skuteczności i jakości produktów farmaceutycznych.
NPRA dotyczące rejestracji produktów farmaceutycznych są zgodne z wytycznymi i zaleceniami Światowej Organizacji Zdrowia (WHO) w zakresie jakości, bezpieczeństwa i skuteczności oraz z innymi uznanymi na arenie międzynarodowej standardami, takimi jak Międzynarodowa Konferencja ds. Harmonizacji (ICH). Główne etapy procesu rejestracji są następujące:
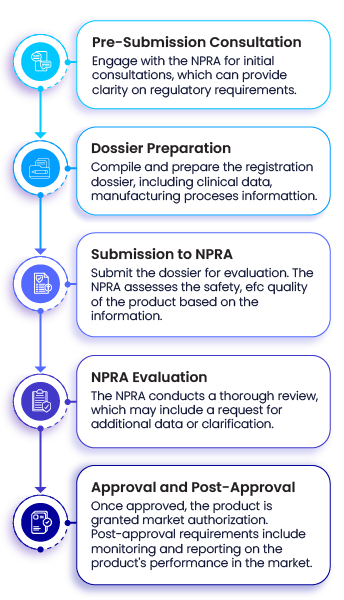
Podstawowe wymogi regulacyjne:
Aby produkt farmaceutyczny mógł zostać zarejestrowany w Malezji, musi spełniać kilka istotnych wymogów regulacyjnych:
- Dobra praktyka wytwarzania (GMP): Aby zagwarantować, że produkt spełnia wymagania jakościowe, zakłady produkcyjne muszą posiadać akredytację organów PIC/S w PIC/S .
- Dane kliniczne: Aby wykazać bezpieczeństwo i skuteczność, nowe substancje czynne (NCE) wymagają danych z badań klinicznych. W przypadku produktów generycznych należy wykazać ich biorównoważność.
- Etykietowanie i pakowanie: Podczas etykietowania produktów należy przestrzegać lokalnych przepisów, zwłaszcza tych dotyczących języka i informacji dotyczących bezpieczeństwa.
- Charakterystyka produktu: Konieczne jest przedstawienie wyczerpującego opisu składników produktu, dawkowania oraz wytycznych dotyczących stosowania.
- Przedstawicielstwo lokalne: Zazwyczaj rolę punktu kontaktowego NPRA musi pełnić lokalny agent lub przedstawiciel. Wnioskodawca ubiegający się o rejestrację produktu, zwany posiadaczem rejestracji produktu (PRH), musi być spółką zarejestrowaną lokalnie, osobą prawną lub podmiotem prawnym posiadającym stałą siedzibę oraz zarejestrowanym w Komisji ds. Spółek Malezji (SSM) (o przedmiocie działalności związanym z produktami zdrowotnymi/farmaceutycznymi).
Studium przypadku firmy Freyr: wsparcie tajwańskiej firmy farmaceutycznej w wejściu na rynek:
Informacje o kliencie: Wiodąca tajwańska firma farmaceutyczna zwróciła się do firmy Freyr o end-to-end wsparcie end-to-end w celu wprowadzeniaProdukty lecznicze malezyjski rynek farmaceutyczny zarównoProdukty lecznicze generycznych, jak iProdukty lecznicze NCE . Celem firmy było zapewnienie terminowego wejścia na rynek przy jednoczesnym pokonaniu złożonych wyzwań regulacyjnych.
Szczegóły projektu: Zakres usług świadczonych przez firmę Freyr obejmuje pełen zakres usług w zakresie zgodności z przepisami:
- Strategia i podejście regulacyjne: Na potrzeby wprowadzenia produktu na rynek malezyjski opracowano strategię zgodną z NPRA i dostosowaną do potrzeb klienta.
- Przegląd techniczny i analiza luk: Przeprowadzono szczegółową analizę dokumentów rejestracyjnych w celu wykrycia ewentualnych luk oraz upewnienia się, że są one zgodne z wymogami NPRA.
- Przygotowanie i złożenie dokumentacji: Przed sporządzeniem i złożeniem dokumentacji rejestracyjnej do NPRA upewniłem się, że wszystkie wymagane dokumenty są kompletne i zgodne z przepisami.
- Kontrola działań z NPRA: Nadzorowałem bieżącą korespondencję z NPRA wyjaśnienia wszelkich wątpliwości i rozpatrzenia dodatkowych wniosków, co przyspieszyło procedurę zatwierdzania.
Wynik: Dzięki wsparciu firmy Freyr klientowi udało się pomyślnie zakończyć proces rejestracji w Malezji. Produkty zostały szybko zatwierdzone, co umożliwiło płynne wejście na rynek, wypełniło wszelkie luki techniczne i zapewniło złożenie odpowiednich dokumentów. Przypadek ten podkreślił mocne strony firmy Freyr w Sprawy regulacyjne jej rolę w skutecznym poruszaniu się po rynku farmaceutycznym w Malezji.
Dzięki end-to-end firmy Freyr klient mógł skupić się na swojej podstawowej działalności, a firma zadbała o sprawny przebieg całego procesu regulacyjnego – od przygotowania dokumentacji po uzyskanie ostatecznego zezwolenia.
Chcesz wejść na dynamicznie rozwijający się rynek farmaceutyczny w Malezji?
Malajski rynek farmaceutyczny oferuje ogromny potencjał wzrostu. Jednak poruszanie się po systemie regulacyjnym wymaga dobrze opracowanej strategii, precyzyjnej dokumentacji oraz znajomości lokalnych realiów.
Dzięki współpracy z doświadczonymi dostawcami usług regulacyjnych, takimi jak Freyr, firmy farmaceutyczne mogą usprawnić proces wejścia na malezyjski rynek farmaceutyczny, wyeliminować niedociągnięcia techniczne i szybciej uzyskać niezbędne zezwolenia, otwierając sobie tym samym nowe możliwości w tym dynamicznie rozwijającym się regionie.










