
W związku z wdrożeniem przez Amerykańską Agencję ds. Żywności i Leków (USFDA) ostatecznej zasady dotyczącej przepisów systemu zarządzania jakością (QMSR) w 2024 roku, producenci wyrobów medycznych muszą przyjąć zmiany, aby wprowadzać i dystrybuować swoje wyroby na rynku USA.
Ta zasada aktualizuje przepisy USFDA dotyczące systemów jakości (QSR) poprzez dostosowanie do ISO 13485:2016, międzynarodowego standardu dla systemów zarządzania jakością wyrobów medycznych (QMS). Producenci wyrobów medycznych mają dwuletni okres przejściowy na dostosowanie się, co sprawia, że organizacje muszą dostosować się do nowych wymagań, aby uniknąć niezgodności podczas kontroli.
Co to jest QMSR?
FDA QMSR to uproszczone podejście do wymogów QMS, które stanowi aktualizację poprzedniej struktury QSR. To dostosowanie jest kluczowe, ponieważ upraszcza globalne przestrzeganie przepisów dla producentów, zwłaszcza tych działających globalnie. Ta harmonizacja pozwoli firmom spełniać wymogi regulacyjne zarówno w US, jak i na innych rynkach w znacznie bardziej ujednolicony sposób.
QMSR nakłada obowiązek usprawnień w zakresie zarządzania ryzykiem, projektowania wyrobów i nadzoru po wprowadzeniu do obrotu. Ta rola może zwiększyć złożoność, ale jednocześnie umożliwia producentom standaryzację ich procedur jakościowych, co z kolei zwiększa bezpieczeństwo wyrobów, a także poprawia dokumentację, co może być kluczowe podczas inspekcji USFDA.
Kluczowe zmiany w QMSR
- Harmonizacja z ISO 13485: Jest to kluczowy krok, który umożliwia producentom wyrobów medycznych przyjęcie międzynarodowych standardów. USFDA uznała, że wiele firm produkujących wyroby medyczne już spełnia normę ISO 13485, co zmniejsza powielanie wysiłków.
- Zarządzanie ryzykiem kładzie nacisk na zarządzanie ryzykiem przez cały cykl życia wyrobu medycznego. Producenci wyrobów medycznych muszą wykazać się skutecznym zarządzaniem ryzykiem, kontrolą ryzyka i zarządzaniem ryzykiem.
- Projektowanie i kontrola wyrobów: Zgodnie z QMSR, kontrole projektowe zostały rozszerzone, aby zapewnić, że producenci wyrobów medycznych w pełni uwzględniają potrzeby użytkowników, bezpieczeństwo wyrobu i kryteria wydajności, co jest obszarem zainteresowania podczas inspekcji USFDA.
- Nadzór po wprowadzeniu do obrotu: Firmy muszą usprawnić system monitorowania po wprowadzeniu do obrotu. Oczekuje się, że producenci będą gromadzić informacje na temat bezpieczeństwa i skuteczności wyrobu, co pomoże w szybkim wykrywaniu i identyfikowaniu problemów.
- Dokumentacja i prowadzenie rejestrów: Jest to ostateczna zasada, która kładzie nacisk na dokumentację. Dokładne i właściwe prowadzenie rejestrów jest kluczowe podczas inspekcji.
Kroki przygotowawcze do inspekcji US Food and Drug Administration:
Ponieważ inspekcja trwa do 2026 roku, firmy mają dwa lata na dostosowanie swoich systemów jakości, co jest zgodne z QMSR. Jednak czekanie na ostatnią chwilę może być ryzykowne.
Kroki do inspekcji USFDA w ramach QMSR dla branż, w których obecny QMS opiera się na QSR:
- Przeprowadź analizę luk: To pierwszy krok, w którym obecny system jakości odbiega od nowych wymagań QMSR. Dokładna analiza luk pomoże zidentyfikować obszary wymagające aktualizacji, takie jak zarządzanie ryzykiem, nadzór po wprowadzeniu do obrotu i kontrola projektowania.
- Zaktualizuj procedurę zarządzania ryzykiem: Upewnij się, że działania związane z zarządzaniem ryzykiem są zintegrowane z całym cyklem życia produktu, od projektu po nadzór po wprowadzeniu na rynek.
- Ponownie przeanalizuj kontrolę projektu: Producenci powinni zapewnić, że proces projektowania jest solidny i dobrze udokumentowany. Zweryfikuj, czy proces projektowania jest solidny i dobrze udokumentowany oraz w pełni zintegrowany z systemem zarządzania jakością.
- Usprawnienie nadzoru po wprowadzeniu do obrotu: Wdrożenie systemów monitorowania działania wyrobu po jego wprowadzeniu na rynek. Może to obejmować ustanowienie mechanizmów zbierania opinii klientów, gromadzenie danych klinicznych i ich ścisłe śledzenie.
- Szkolenia i dokumentacja: Szkolenie personelu w zakresie nowych wymagań, zwłaszcza tych zaangażowanych w zarządzanie jakością i zgodność regulacyjną. Zapewnia to, że cały proces dokumentacji jest zgodny z oczekiwaniami QMSR.
- Certyfikacja przez stronę trzecią: Jeśli Twoja firma nie posiada certyfikatu ISO 13485, teraz może być dobry moment, aby to rozważyć. Uzyskanie certyfikatu ISO 13485 może dać Ci przewagę w spełnianiu wymagań USFDA, aby zwiększyć wiarygodność na rynkach globalnych.
Poruszanie się po dwuletnim okresie przejściowym
Aby skutecznie wykorzystać okres przejściowy i zapewnić zgodność z rozporządzeniem USFDA dotyczącym Systemu Zarządzania Jakością (QMSR), producenci powinni przyjąć proaktywne podejście. Oto sugerowany plan działania:
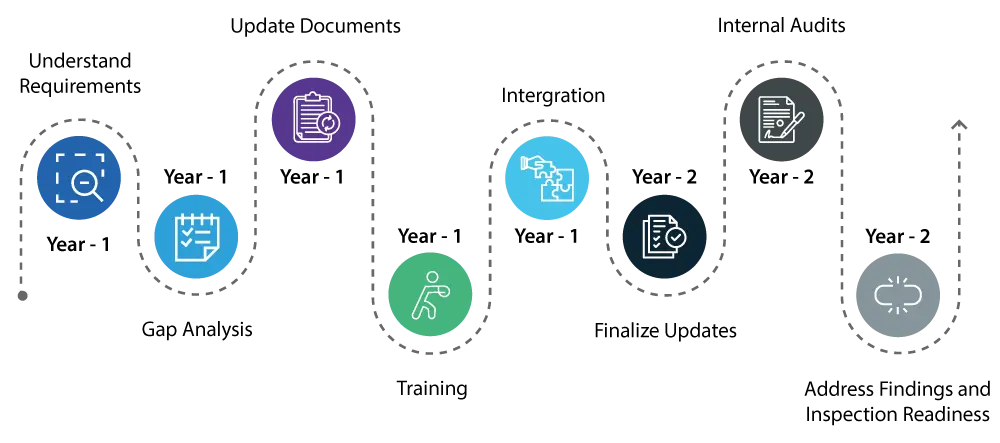
Rok 1:
- Zrozumienie wymagań: Zacznij od dokładnego zrozumienia zmian wprowadzonych przez QMSR. Obejmuje to szczegółowy przegląd nowych wymagań i tego, jak różnią się one od istniejących przepisów dotyczących Systemu Jakości (QS).
- Poznaj luki: Przeprowadź kompleksową analizę luk, aby zidentyfikować obszary w obecnym systemie jakości, które wymagają aktualizacji, aby spełnić nowe standardy QMSR.
- Aktualizacja / naprawa dokumentacji: Zainicjuj niezbędne aktualizacje swojego systemu jakości, koncentrując się na obszarach takich jak zarządzanie ryzykiem i kontrola projektu, które są kluczowymi elementami QMSR.
- Szkolenie: Rozpocznij szkolenie personelu w zakresie nowych przepisów, aby upewnić się, że wszyscy zaangażowani są świadomi zmian i rozumieją swoje role w utrzymaniu zgodności.
- Integracja : Rozpocznij integrowanie nowych wymagań QMSR z codziennymi operacjami, aby ułatwić przejście.
Rok 2:
- Kontynuuj wdrażanie zmian w swoim systemie jakości, zapewniając pełną integrację i funkcjonalność wszystkich aktualizacji.
- Przeprowadzaj dokładne audyty wewnętrzne, aby zweryfikować skuteczność aktualizacji i pełną zgodność systemu jakości z wymaganiami QMSR.
- Niezwłocznie zajmij się wszelkimi ustaleniami z audytów wewnętrznych, aby zapewnić zgodność wszystkich aspektów Twojego systemu jakości.
- Do końca drugiego roku Twój system jakości powinien być w pełni zgodny z QMSR, a Ty powinieneś być przygotowany na inspekcje USFDA z pewnością, że nie będzie żadnych poważnych problemów.
Postępując zgodnie z tą mapą drogową, producenci mogą nie tylko spełnić wymagania USFDA, ale także ustanowić solidny system jakości, który jest wydajny, ustandaryzowany i uznawany globalnie. To proaktywne podejście pomoże zapewnić płynne przejście do nowych przepisów i utrzymać najwyższe standardy jakości i bezpieczeństwa dla wyrobów medycznych.
Podsumowanie: Podejmowanie proaktywnych działań
Przygotowanie do inspekcji USFDA zgodnie z nowymi przepisami QMSR to nie tylko unikanie kar – to także poprawa bezpieczeństwa i skuteczności wyrobów. Poprzez harmonizację z ISO 13485, USFDA podnosi poprzeczkę, ale jednocześnie oferuje drogę do bardziej usprawnionej globalnej zgodności. Producenci, którzy zaczną się dostosowywać wcześnie, powinni skupić się na kluczowych obszarach, takich jak zarządzanie ryzykiem i nadzór po wprowadzeniu do obrotu, oraz zapewnić, że ich systemy jakości są aktualne i solidne, co nie tylko spełni oczekiwania regulacyjne, ale także zwiększy ich przewagę konkurencyjną na rynku.

