
W silnie regulowanym środowisku branży Life Sciences przestrzeganie Wytycznych Specyficznych dla Produktu (PSG) jest kluczowe dla pomyślnego rozwoju i zatwierdzania leków. PSG to kompleksowe dokumenty wydawane przez globalne Organy ds. Zdrowia (HA) w celu zapewnienia wytycznych dotyczących zatwierdzania produktów farmaceutycznych w określonych kategoriach terapeutycznych.
Ten blog szczegółowo opisuje cel, znaczenie oraz perspektywę HA w kwestii wydawania PSG. Zrozumienie uzasadnienia i oczekiwań przedstawionych w PSG, które umożliwiają strategiczny sukces firm z branży nauk przyrodniczych, jest szczegółowo opisane w tym artykule.
Zrozumienie wytycznych specyficznych dla produktu i ich rodzajów
PSGs odgrywają kluczową rolę w kształtowaniu ścieżki regulacyjnej dla produktów farmaceutycznych. Dostarczając ukierunkowane wytyczne, władze zdrowotne (HAs) zapewniają spójność i rzetelne oceny wniosków o dopuszczenie produktów w określonych kategoriach terapeutycznych. Przestrzegając PSGs, firmy farmaceutyczne mogą poruszać się po złożonym otoczeniu regulacyjnym, zapewniając, że ich produkty spełniają wymagane standardy bezpieczeństwa i skuteczności.
PSGs nie ograniczają się do rozwoju leków generycznych. Obejmują również szeroki zakres produktów farmaceutycznych, takich jak następujące:
- Dla leków innowacyjnych: PSGs dostarczają szczegółowych wytycznych dotyczących badań przedklinicznych, projektowania badań klinicznych, oceny bezpieczeństwa, farmakokinetyki i punktów końcowych skuteczności. Prowadzą firmy w zakresie rodzaju i ilości danych wymaganych do wykazania bezpieczeństwa i skuteczności ich innowacyjnych leków.
- Dla leków biopodobnych: PSGs (wytyczne dotyczące konkretnych produktów) określają wymagania dotyczące danych, metody analityczne i kwestie projektowania badań klinicznych dla produktów biopodobnych. Przestrzegając ich, firmy produkujące leki biopodobne mogą wykazać podobieństwo swoich produktów do referencyjnego produktu biologicznego, torując drogę do zatwierdzenia i dostępu do rynku.
- Dla produktów biologicznych: Te wytyczne dotyczą kluczowych aspektów, takich jak produkcja, charakterystyka i badania porównawcze, zapewniając, że produkty biologiczne spełniają zatwierdzone normy.
Opracowywanie Wytycznych i Procesów Specyficznych dla Produktu
Opracowywanie PSG to wspólny wysiłek z udziałem HAs, ekspertów naukowych i interesariuszy z branży. Poniżej przedstawiono etapy opracowywania PSG:
Etap 1 – Kompleksowa ocena obszaru terapeutycznego: Organy ds. zdrowia (HAs) identyfikują luki w istniejących wytycznych i inicjują rozwój PSGs w celu ich uzupełnienia. Następnie angażowani są eksperci naukowi i przedstawiciele branży, aby wnieść swoją wiedzę, co zapewnia, że projekty wytycznych są oparte na dowodach i praktyczne we wdrożeniu.
Etap 2 – Konsultacje publiczne: Projekty PSGs są teraz dostępne do publicznego wglądu i zgłaszania uwag. To otwarte i przejrzyste podejście umożliwia zainteresowanym stronom, w tym pracownikom służby zdrowia (HCPs), grupom pacjentów i przedstawicielom branży, wniesienie cennego wkładu oraz poprawę ogólnej jakości i trafności wytycznych.
Etap 3: Etap przeglądu wewnętrznego: Podczas gdy projekty PSG są poddawane konsultacjom publicznym, zespół ds. rozwoju PSG w ramach organów regulacyjnych przeprowadza rygorystyczny przegląd wewnętrzny, zapewniając, że wytyczne spełniają niezbędne wymogi regulacyjne i są zgodne z szerszymi ramami regulacyjnymi.
Etap 4 – Finalizacja: Po sfinalizowaniu, PSG są publikowane i udostępniane branży, dostarczając jasnych i praktycznych wskazówek dotyczących rozwoju produktu i składania wniosków.
Elementy PSG
Firmy z branży nauk przyrodniczych muszą mieć jasne zrozumienie komponentów PSG. Poniższy wykres kołowy przedstawia je szczegółowo:
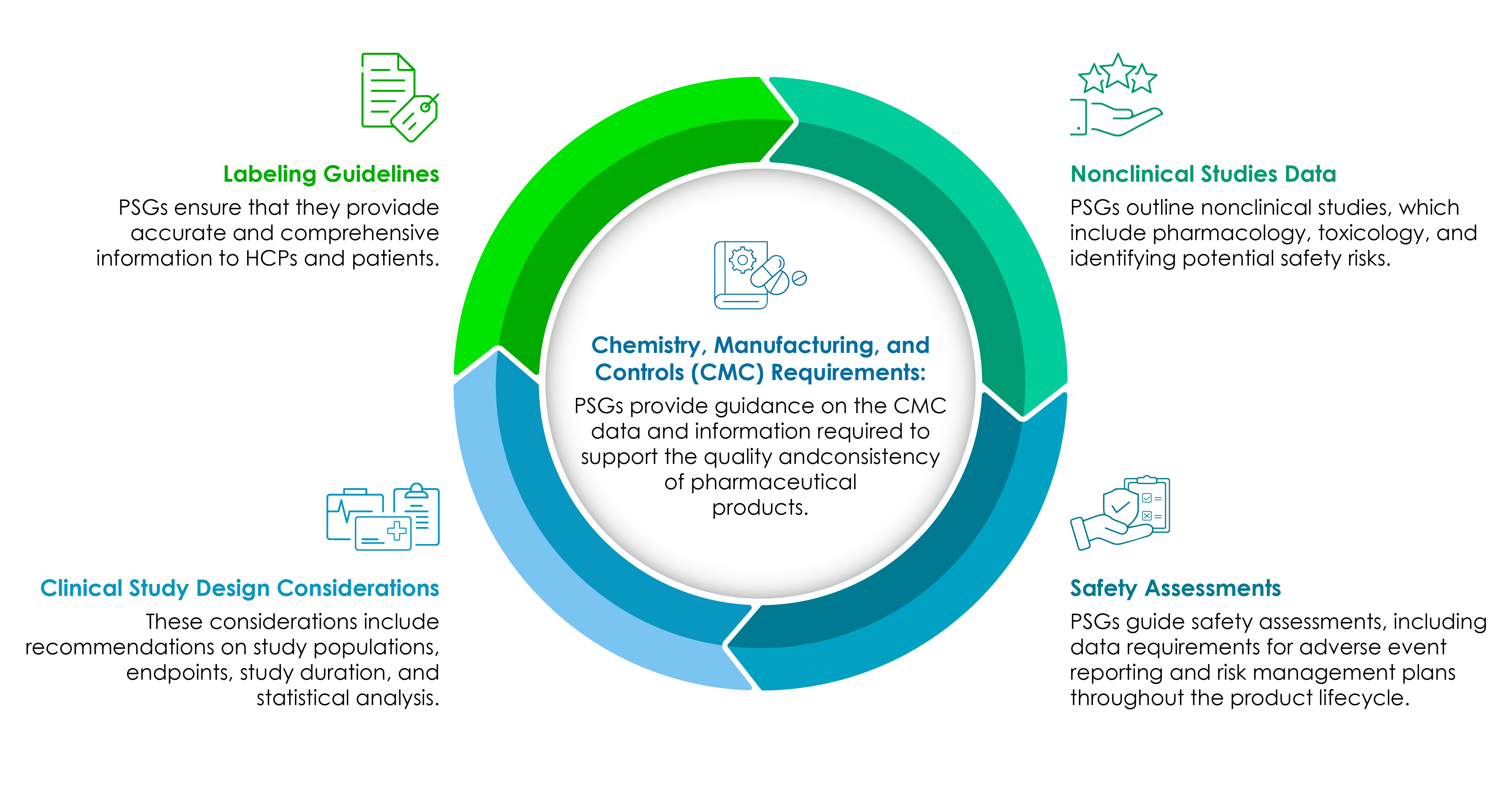
CMC pozostaje podstawą każdego rozwoju produktu farmaceutycznego ukierunkowanego na regulacje.
Poruszanie się po PSGs
Poruszanie się po PSGs w sposób zgodny z przepisami regulacyjnymi można osiągnąć poprzez następujące wymienione punkty/strategie:
- Wczesne zaangażowanie w współpracę z organami ds. zdrowia: Takie zaangażowanie sprzyja podejściu opartemu na współpracy i pomaga proaktywnie rozwiązywać potencjalne wyzwania.
- Ekspertyza naukowa: Wykorzystanie opinii ekspertów zapewnia, że projekty badań, metody analityczne i oceny bezpieczeństwa są zgodne z najwyższymi standardami naukowymi.
- Konsultanci regulacyjni: Konsultanci zapewniają fachowe doradztwo, zapewniając sukces planów rozwoju i zgłoszeń regulacyjnych.
- Kompleksowy przegląd PSG: Firmy powinny zidentyfikować konkretne sekcje PSG mające zastosowanie do ich produktu i odpowiednio dostosować swoje plany rozwoju.
- Ciągłe monitorowanie: PSG to dynamiczne dokumenty, które mogą być często aktualizowane lub zmieniane. Firmy muszą monitorować zmiany w PSG, aby zapewnić zgodność regulacyjną z najnowszymi wymogami PSG.
Eksperckie doradztwo regulacyjne ułatwia poruszanie się po PSG. Skonsultuj się teraz!
Podsumowanie
Wytyczne specyficzne dla produktu (PSG) stanowią podstawę zgłoszeń regulacyjnych dla produktów farmaceutycznych w określonych kategoriach terapeutycznych. Zrozumienie perspektyw organów regulacyjnych (HA) stojących za wydawaniem PSG jest kluczowe dla firm z branży nauk przyrodniczych, które dążą do przyspieszenia zatwierdzeń, zapewnienia jakości produktów i płynnego poruszania się w globalnym środowisku regulacyjnym.
Jako wiodący dostawca usług regulacyjnych, Freyr docenia znaczenie przestrzegania najlepszych praktyk i wykorzystywania wiedzy, która pomoże firmom z branży nauk przyrodniczych dostosować strategie rozwoju produktów do wymagań PSG. Skontaktuj się z nami już dziś, aby dowiedzieć się więcej o naszych usługach i jak możemy pomóc Państwu osiągnąć cele.









