Podczas gdy innowacyjne lub markowe produkty lecznicze wiążą się z dodatkowymi kosztami związanymi z badaniami i rozwojem produktu, od etapu identyfikacji cząsteczki do dopuszczenia do obrotu po wprowadzeniu na rynek, generyczne produkty lecznicze są stosunkowo opłacalne. Terapie te nie tylko zmniejszają ogólny koszt leczenia, ale także znacząco poprawiają dostęp pacjentów do ratujących życie produktów leczniczych. Ponieważ zależność od importu generycznych antybiotyków i terapii lekowych na choroby rzadkie wpłynęła na dostępność tych produktów leczniczych globalnie w czasie pandemii, agencje zdrowia wprowadzają nowe wytyczne w celu wsparcia lokalnych producentów leków.
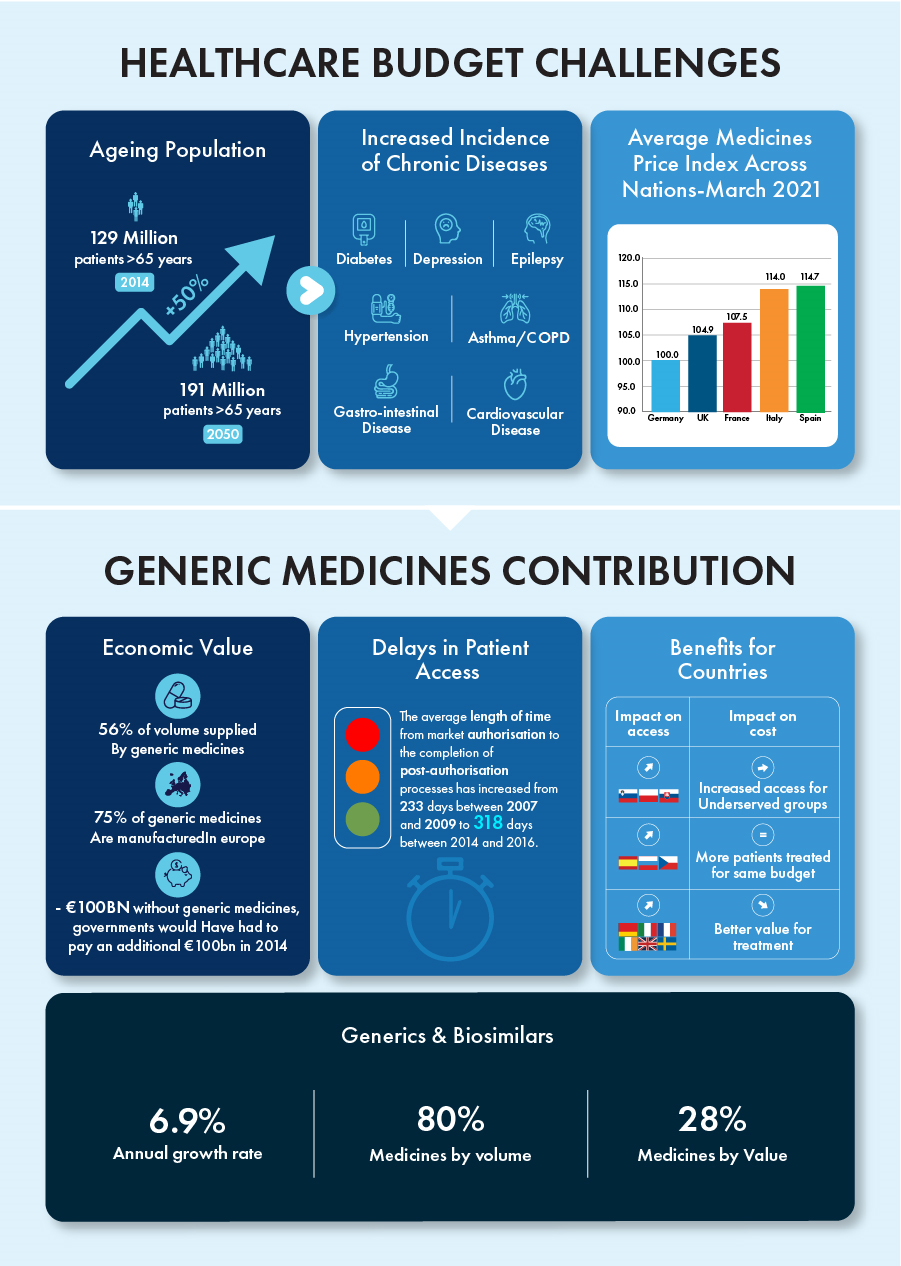
Od 1993 roku organizacja handlowa Medicines for Europe, wcześniej znana jako European Generics Medicine Association (EGA), konsekwentnie realizuje swój cel, jakim jest udostępnianie opłacalnych terapii europejskim pacjentom. W ciągu ostatniej dekady z powodzeniem dostarczyli 67% wszystkich leków do Europy, zwiększając dostęp pacjentów do 100% w siedmiu (07) kluczowych obszarach terapeutycznych. W ramach kompetencji europejskich organów ds. zdrowia, „autonomia strategiczna” po Brexicie zapoczątkowała natychmiastową potrzebę skutecznego zaradzenia niekorzystnej sytuacji konkurencyjnej, z jaką borykają się europejscy producenci leków generycznych i biopodobnych. Wraz z nadejściem pandemii COVID-19, globalne możliwości łańcucha dostaw uległy presji popytu na leki. Leki ratujące życie, które przynosiły ulgę w chorobach przewlekłych, zniknęły z półek lokalnych aptek. Aby pokonać przeszkody związane z produktami leczniczymi chronionymi patentami i zbudować lokalne zdolności produkcyjne leków w celu poprawy dostępu pacjentów, Rada UE przyjęła rozporządzenie, które przewiduje wyjątek dla oryginalnej cząsteczki poprzez wydanie dodatkowego świadectwa ochronnego (SPC). Przepis ten ułatwia produkcję leków generycznych i biopodobnych przed wygaśnięciem patentu w celach magazynowania lub eksportu. Wyjątek będzie jednak miał zastosowanie tylko w następujących okolicznościach.
- Wytwarzane leki generyczne lub biopodobne są przeznaczone wyłącznie na eksport do innego kraju, gdzie patent na cząsteczkę leku nie istnieje lub wygasł, lub do celów gromadzenia zapasów w ramach pozostałego okresu ważności patentu wynoszącego sześć (06) miesięcy.
- Zgodnie z wymogiem producent przekazał informację lokalnemu organowi ds. zdrowia oraz posiadaczowi SPC przed upływem trzech (03) miesięcy.
- Producent poinformował wszystkich zainteresowanych komercjalizacją produktu.
- Producent zapewnił, że wymagania dotyczące etykietowania wskazują, iż produkt leczniczy jest przeznaczony wyłącznie na eksport.
W rzeczywistości
Od czasu udzielenia warunkowego pozwolenia na dopuszczenie do obrotu produktów szczepionkowych przeciwko COVID-19 w UE, Komitet ds. Produktów Leczniczych Stosowanych u Ludzi (CHMP) Europejskiej Agencji Leków zatwierdził cztery (04) miejsca produkcji szczepionek w ciągu roku; dwa (02) w Szwajcarii i dwa (02) w USA. Takie decyzje na rzecz rozszerzenia miejsc produkcji zwiększą możliwości wytwarzania szczepionek, jednocześnie czyniąc je bardziej dostępnymi dla ludności europejskiej.
Leki generyczne i biopodobne samodzielnie przyczyniły się do rocznego wzrostu o 6,9%, stanowiąc w ostatniej dekadzie 80% wszystkich leków pod względem objętości i 28% pod względem wartości. Termin ważności patentów na niektóre leki biologiczne o wartości około 90 miliardów euro wygaśnie do 2023 roku, tworząc konkurencyjne środowisko dla tych produktów o ogromnym potencjale wzrostu.
Wdrożenie zwolnienia z SPC przyniosłoby korzyści Unii Europejskiej poprzez:
- Dodanie dodatkowych około 90,5 mld euro rocznie.
- Stworzenie dwudziestu pięciu tysięcy (25 000) nowych miejsc pracy, w tym dwa tysiące (2000) bezpośrednich miejsc pracy dla przemysłu API w UE. Inicjatywa pomoże Member States UE zaoszczędzić 3,1 mld euro na wydatkach na opiekę zdrowotną.
- Gromadzenie tańszych alternatyw innowacyjnych leków opatentowanych, aby umożliwić im wejście na rynek natychmiast po wygaśnięciu własności intelektualnej (IP), poprawiając dostęp pacjentów.
Dla producenta leków z Unii Europejskiej, wdrożenie zwolnienia z SPC jest jedną z najbardziej korzystnych inicjatyw na rzecz leków generycznych. Ponieważ Organ ds. Zdrowia UE reguluje leki do stosowania u ludzi i zwierząt poprzez procedurę scentralizowaną lub zdecentralizowaną, poruszanie się po specyficznych lokalnych wymaganiach może być przytłaczające. Ekspert, znający lokalne wymagania dotyczące różnych zgłoszeń i dokumentów licencyjnych, może pomóc Państwu skupić się na kluczowych protokołach produkcyjnych, zamiast koncentrować się na złożonych przeszkodach regulacyjnych. Odkryj na nowo potencjał swojej firmy, doświadczając zgodności i jakości. Skontaktuj się z Freyr.









