
Zezwolenia na użycie w nagłych wypadkach (EUA) są istotne dla szybszego udostępniania pacjentom ratujących życie Produktów leczniczych. Okazały się pomocne w walce z pandemiami, takimi jak COVID-19. Inicjatywa USFDA (United States Food and Drug Administration) rozpoczęła się w 2004 roku, a EUA weszły w życie, gdy sekcja 564 Federalnej Ustawy o Żywności, Lekach i Kosmetykach została zmieniona przez ustawę Project BioShield. Program ten jest krokiem podjętym przez FDA w celu ochrony zdrowia publicznego poprzez zapewnienie bezpieczeństwa, skuteczności i jakości produktów medycznych, jednocześnie reagując na nagłe przypadki medyczne i pojawiające się zagrożenia dla zdrowia publicznego.
Zrozummy to lepiej w kolejnych wierszach.
Analiza EUA
Ścieżka EUA jest sposobem na ułatwienie dostępu do medycznych środków zaradczych w czasach ogłoszonych sytuacji nadzwyczajnych. Komisarz FDA może autoryzować poniższe w takich sytuacjach:
- Autoryzowane użycie niezarejestrowanych produktów medycznych.
- Nieuprawnione użycie zatwierdzonych produktów medycznych.
Produkty objęte EUA obejmują szczepionki, płyny dożylne, leki, wyroby medyczne, testy itp. i mogą być stosowane do diagnozowania, leczenia lub zapobiegania stanom zagrażającym życiu. Produkty otrzymują EUA, jeśli spełnione są następujące kryteria:
- Dowód na stan/chorobę zagrażającą życiu.
- Dane naukowe dostarczają wystarczających dowodów na to, że produkt jest skuteczny w swoim zamierzonym zastosowaniu.
- Korzyści płynące z produktu przewyższają ryzyko (czyli dowód bezpieczeństwa).
- Brak produktów alternatywnych.
Sponsorom zaleca się wcześniejsze zapoznanie się z wymaganiami FDA, aby mogli postępować zgodnie z najlepszym procesem regulacyjnym i zapewnić bezbłędne złożenie wniosku EUA. Poniżej przedstawiono obowiązkowe informacje, które sponsor musi udostępnić we wniosku.
Dane do przedłożenia przez sponsora do FDA w celu uzyskania zatwierdzenia EUA.
- Opis produktu i jego przeznaczenie.
- Status zatwierdzenia produktu przez FDA.
- Informacje dotyczące bezpieczeństwa i skuteczności, takie jak dane kliniczne i niekliniczne, itp.
- Raport z analizy ryzyka i korzyści.
- Dane dotyczące Chemii, Wytwarzania i Kontroli (CMC).
- Informacje dotyczące dawkowania, przeciwwskazań, ostrzeżeń i działań niepożądanych w związku z dystrybucją danego produktu medycznego.
Jak EUAs są wydawane przez FDA?
Poniżej przedstawiono schematyczną interpretację cyklu życia EUA w skrócie:
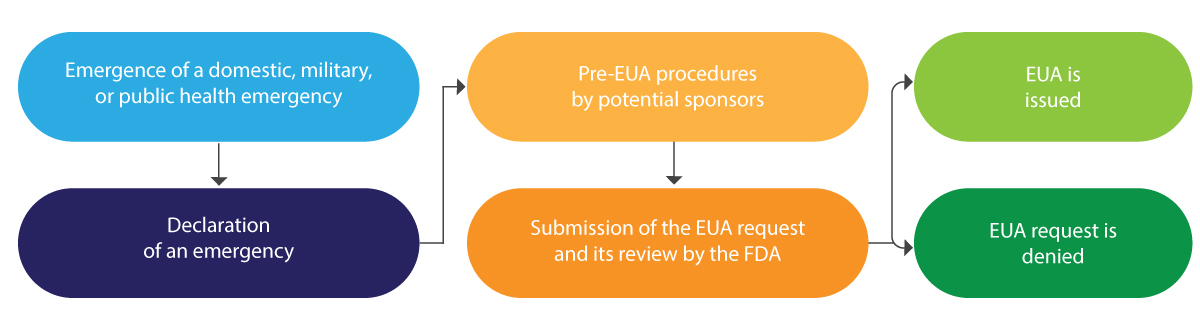
EUA jest zazwyczaj wydawane na ograniczony okres, a po zakończeniu wspomnianej sytuacji nadzwyczajnej, jest ono wycofywane przez FDA.
EUA a COVID-19
Sekretarz Zdrowia i Nauk Humanitarnych (HHS) ogłosił COVID-19 pandemią 31 stycznia 2020 r. Od tego czasu FDA odegrała kluczową rolę w zatwierdzaniu kilku szczepionek i domowych zestawów testowych w ramach ścieżki EUA, aby poradzić sobie z trwającą globalną epidemią.
Wraz z pojawieniem się nowych wariantów COVID-19, cała branża farmaceutyczna ciężko pracuje, aby ograniczyć rozprzestrzenianie się i obniżyć wskaźniki śmiertelności. Istnieje zapotrzebowanie na nowe Produkty lecznicze i szybsze zatwierdzenia przez globalne organy regulacyjne, tak aby ich czas wprowadzenia na rynek był skrócony. Ścieżka EUA (Emergency Use Authorization) rejestracji nowych Produktów leczniczych/leków jest, zdaniem ekspertów, drogą naprzód. Kilka innych organów ds. zdrowia, takich jak Europejska Agencja Leków (EMA), Central Drugs Standard Control Organization (CDSCO), Saudi Food and Drug Authority (SFDA) itp., również wdrożyły ścieżkę EUA w celu szybszych zatwierdzeń.
Jeśli jesteś producentem leków i szukasz EUA dla swojego produktu ratującego życie, będziesz potrzebować doświadczonego dostawcy rozwiązań regulacyjnych. Skontaktuj się z Freyr, aby zapewnić szybsze wprowadzenie produktu na rynek i zgodną z przepisami ścieżkę.










