
List ostrzegawczy to oficjalna wiadomość/pismo wydawane przez organ ds. zdrowia do organizacji, która narusza ustalone zasady i przepisy. W przypadku firm farmaceutycznych, muszą one przestrzegać kilku Dobrych Praktyk Wytwarzania (GMP), GCP, GDP itp., aby uniknąć takich ostrzeżeń. Istnieje wiele przypadków, w których każdy Organ ds. Zdrowia (HA), w szczególności FDA, wydaje takie pisma.
Na przykład, niedawno indyjska firma farmaceutyczna otrzymała list ostrzegawczy od Amerykańskiej Agencji ds. Żywności i Leków (USFDA) z powodu naruszeń w swoim zakładzie produkcyjnym Aktywnych Składników Farmaceutycznych (APIs). Działanie to było wynikiem inspekcji zakładu przeprowadzonej przez FDA kilka miesięcy temu.
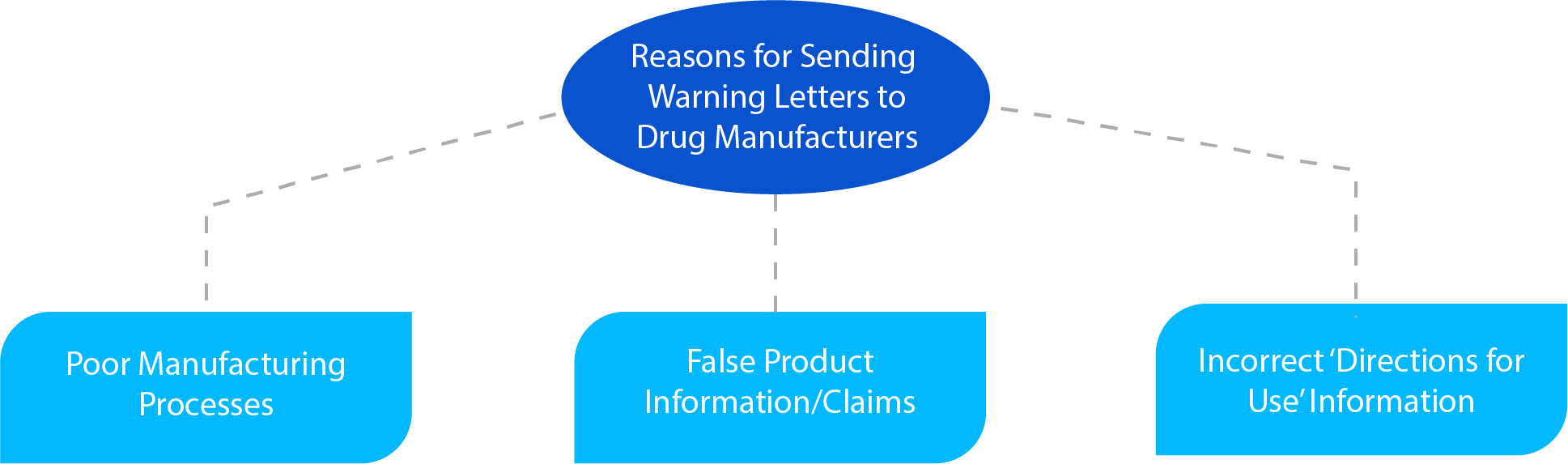
Co może zawierać list ostrzegawczy?
Pismo ostrzegawcze jest dość szczegółowe i może zawierać następujące informacje, w zależności od przypadku:
- Naruszenie zidentyfikowane przez HA podczas przeprowadzania inspekcji, zasadniczo jeden z trzech (03) powodów określonych na powyższym schemacie.
- Lista środków naprawczych, które należy podjąć w związku z zidentyfikowanym problemem.
- Ramy czasowe, w których producent musi poinformować FDA o planie korekty.
Jednakże list ostrzegawczy jest przeszkodą, która może wpłynąć na kilka czynników w działalności biznesowej. Poniżej wymieniono kilka z nich.
Konsekwencje listu ostrzegawczego
- Opóźnienie we wprowadzeniu na rynek.
- Trudności finansowe przy podejmowaniu działań naprawczych.
- Odpowiedzialność w łańcuchu dostaw z powodu wstrzymania procesu produkcyjnego.
Podsumowanie
Unikanie skrótów i naruszeń w cyklu życia produkcji to jedyny sposób na uniknięcie pism ostrzegawczych od odpowiednich organów ds. zdrowia (HA). Kilka firm musiało zamknąć swoją działalność z powodu poważnych naruszeń wytycznych. Wsparcie ze strony kompleksowego eksperta regulacyjnego, takiego jak Freyr, może pomóc producentom farmaceutycznym w przestrzeganiu zgodnej ścieżki. Skontaktuj się z Freyr już teraz i uniknij wszelkich ryzyk.









