Raportowanie zdarzeń dotyczących wyrobów medycznych (MDR) to narzędzie nadzoru po wprowadzeniu do obrotu, które Agencja Żywności i Leków (FDA) wykorzystuje do monitorowania działania wyrobów, wykrywania potencjalnych problemów bezpieczeństwa związanych z wyrobami oraz przyczyniania się do oceny korzyści i ryzyka wyrobów. Celem MDR jest terminowe wykrywanie i rozwiązywanie zdarzeń niepożądanych związanych z wyrobami. Umożliwia to lekarzom, placówkom opieki zdrowotnej, producentom i konsumentom dobrowolne zgłaszanie informacji w celu zrozumienia bezpieczeństwa i skuteczności wyrobu po wprowadzeniu do obrotu.
MDR ma zastosowanie do wszystkich klas wyrobów medycznych, które są produkowane w Stanach Zjednoczonych Ameryki (USA) lub importowane do USA. Producenci wyrobów medycznych, którzy chcą wprowadzić swoje wyroby na rynek w USA, muszą przestrzegać MDR, w przeciwnym razie może to prowadzić do kar finansowych. Ma zastosowanie w USA, w tym w przypadku zdarzeń zagranicznych, tzn. dotyczy legalnie wprowadzonych do obrotu wyrobów medycznych w Stanach Zjednoczonych, zarówno produkowanych w USA, jak i w krajach zagranicznych. Dodatkowo, istnieją różne przypadki zastosowania MDR, takie jak:
- jeśli wyrób jest produkowany w USA, dystrybuowany lokalnie i na inne rynki
- gdy wyrób jest produkowany w USA, ale dystrybuowany na innych rynkach
- gdy wyrób jest produkowany w obcym kraju, dostarczany do USA i na inne rynki
- gdy wyrób jest produkowany w obcym kraju i dystrybuowany lokalnie oraz
- gdy wyrób jest przedmiotem dochodzenia w USA
MDR i przebieg procesu raportowania
Rozporządzenie w sprawie wyrobów medycznych (MDR) zawiera wiele obowiązkowych wymagań dla producentów, importerów i placówek użytkujących wyroby medyczne, aby zgłaszali określone zdarzenia niepożądane związane z wyrobami medycznymi i problemy z produktami do FDA. Poniżej przedstawiony schemat blokowy procesu szczegółowo opisuje proces zgłaszania krok po kroku.
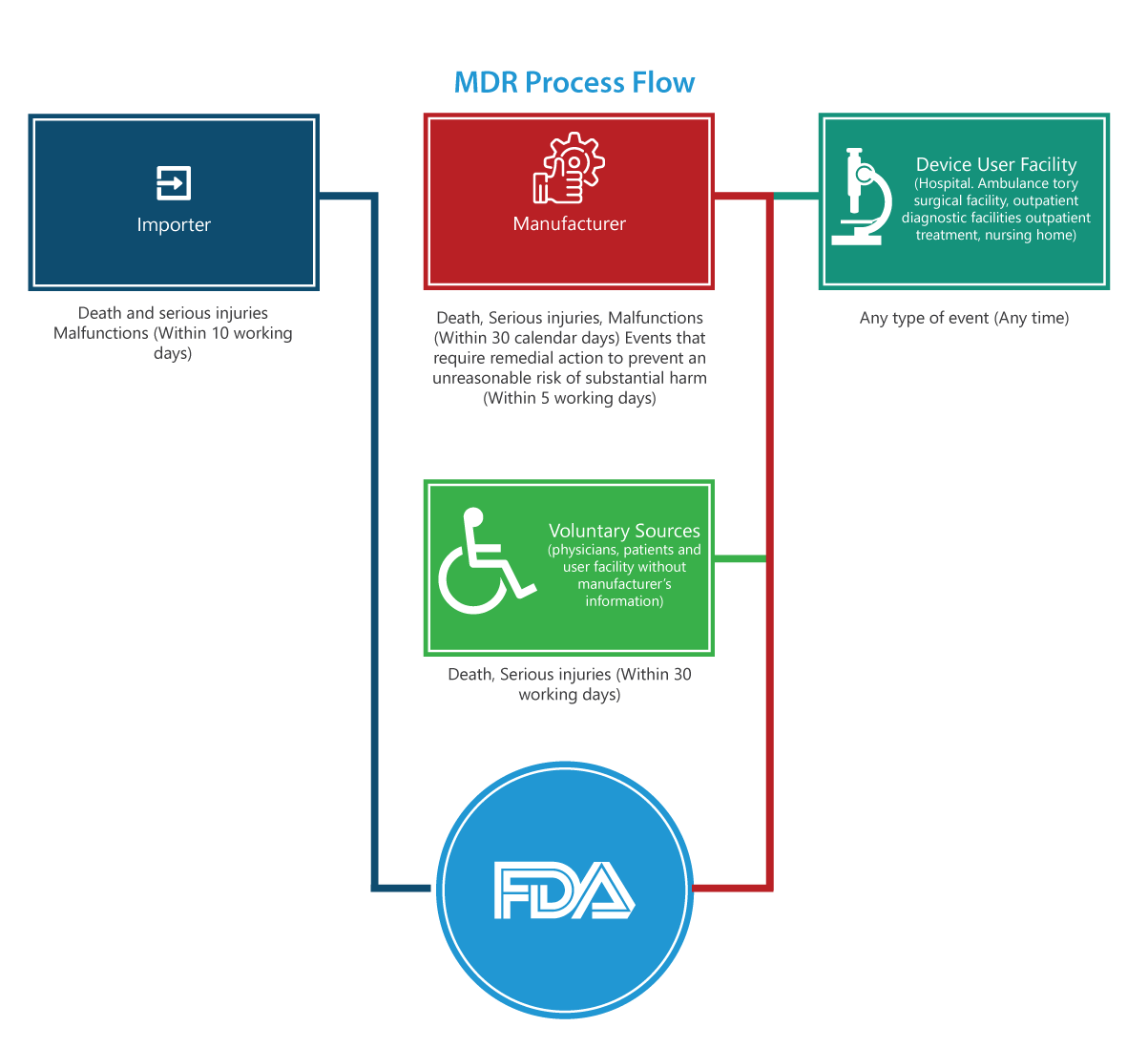
Kogo to dotyczy?
Importerzy
Zgłoszenia zgonów, poważnych obrażeń i nieprawidłowego działania należy przesyłać do FDA i producenta w ciągu 30 dni roboczych. Jeśli nieprawidłowe działanie może spowodować obrażenia lub zgony w innych miejscach, importerzy mają obowiązek zgłosić to producentowi.
Producenci
Zgłoszenia dotyczące zdarzeń (zgonów, poważnych obrażeń i nieprawidłowego działania) wyznaczonych przez FDA lub zdarzenia wymagającego działań naprawczych w celu zapobieżenia nieuzasadnionemu ryzyku znacznej szkody dla zdrowia publicznego muszą zostać przesłane do FDA w ciągu 5 dni roboczych poprzez wypełnienie formularza 3500A.
Placówka użytkownika wyrobu medycznego (Szpital, ambulatoryjna placówka chirurgiczna, dom opieki, ambulatoryjna placówka diagnostyczna lub ambulatoryjna placówka lecznicza)
Zgłoszenia należy przesyłać do producenta wyrobu nie później niż 10 dni roboczych od dnia, w którym placówka uzyska informację, że wyrób spowodował lub mógł spowodować lub przyczynił się do poważnego obrażenia pacjenta placówki. Jeśli producent jest nieznany, placówka musi przesłać zgłoszenie do FDA.
Dobrowolne grupy
Pacjenci, pracownicy służby zdrowia i konsumenci, którzy zauważą problem związany z wyrobem medycznym, mogą zgłosić go do FDA za pośrednictwem MedWatch.
eMDR
FDA nakazało elektroniczne zgłaszanie MDR (eMDR) w 2015 roku w celu identyfikacji krytycznych problemów z jakością i integralnością danych związanych ze zgłaszaniem poważnych obrażeń dotyczących wszystkich klas wyrobów medycznych. eMDR jest preferowanym sposobem zgłaszania.
Producenci mogą składać swoje eMDR za pośrednictwem Elektronicznej Bramy Zgłoszeń (ESG). Od momentu złożenia, elektroniczna brama potrzebuje do 48 godzin na wysłanie potwierdzenia. W przypadku błędu podczas składania raportu, pojawi się komunikat umożliwiający dokonanie korekty/korekt.
eMDR – Jakie są jego korzyści?
eMDR oferuje wiele zalet w porównaniu z ręcznym mechanizmem raportowania (tj. MDR). Poniżej wymieniono kilka znaczących korzyści, na które mogą liczyć producenci / agencje / pacjenci:
- Narzędzie do zgłaszania eMDR usprawnia współpracę między organizacją, agencją zdrowia (FDA) a pacjentami.
- eMDR pozwala oszczędzać koszty. Automatyzacja zmniejsza potrzebę kosztów administracyjnych i tradycyjnej komunikacji; pomaga przyspieszyć proces i sprzyja efektywnemu raportowaniu zdarzeń, co skutkuje natychmiastową interakcją z FDA.
- Procesy ręczne wiążą się z dużą ilością dokumentacji, mogą być czasochłonne oraz trudne do śledzenia i przetwarzania. Zgłoszenia eMDR są zautomatyzowane i scentralizowane. Dokumenty można łatwo odzyskać, co znacznie oszczędza czas podczas przeglądu.
- eMDR umożliwia stronom szybkie oznaczanie błędów w zgłoszeniach, w przeciwieństwie do ręcznej i czasochłonnej korespondencji z FDA.
- eMDR działa jako pojedynczy punkt wejścia do przetwarzania wszystkich zgłoszeń elektronicznych w wysoce zabezpieczonym środowisku i jest to korzystne, ponieważ skargi w organizacji mogą być bezpośrednio powiązane z formularzem MedWatch i zintegrowane z bramą FDA.
eMDR i przepływ procesu raportowania
Rozporządzenie eMDR zawiera obowiązkowe wymagania dla producentów, importerów i placówek użytkujących wyroby medyczne dotyczące zgłaszania do FDA niektórych zdarzeń niepożądanych związanych z wyrobami medycznymi i problemów z produktami. Poniższy schemat przedstawia szczegółowo proces zgłaszania krok po kroku.
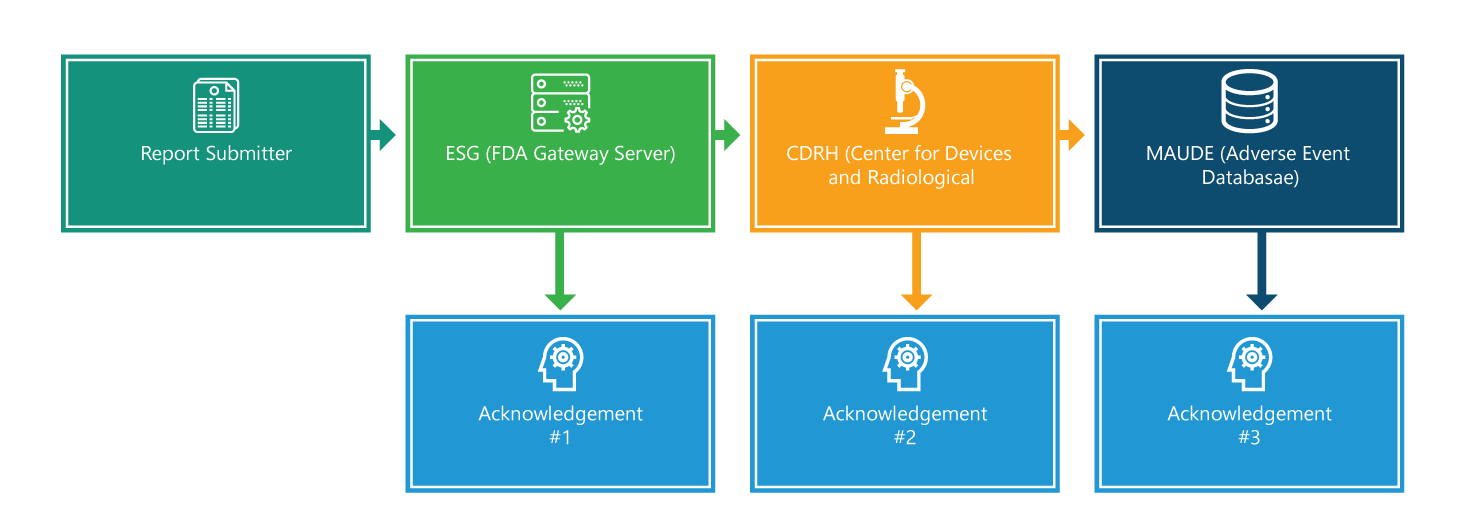
Proces raportowania składa się z czterech etapów. Z wyjątkiem pierwszego etapu, każdy etap jest potwierdzany. Ponadto, każdy etap zawiera dodatkowe informacje, które ułatwią ten proces.
Krok 1: Podmiot składający raport
Składanie eMDR. Na początku, aby złożyć zgłoszenie, należy posiadać podpis elektroniczny i upewnić się, że nazwy plików zgłoszeniowych zawierają tylko jedną kropkę, która służy do wskazania rozszerzenia typu pliku (na przykład 555.xml lub 555.pdf). Jednakże czas dostarczenia i przetwarzania wniosku zależy od całkowitego rozmiaru zgłoszenia; większe zgłoszenia wymagają dłuższego czasu na dostarczenie i przetworzenie.
Krok 2: Brama do elektronicznego składania dokumentów (ESG)
Gdy Twoje zgłoszenie dotrze do ESG, powinieneś szybko otrzymać potwierdzenie #1, chyba że ESG jest niedostępne z powodu konserwacji. Jesteś zobowiązany do sprawdzenia statusu swojego MDR na stronie internetowej ESG.
Krok 3: CRDH
eMDR jest automatycznie przekierowywany z ESG do Centrum Urządzeń i Zdrowia Radiologicznego (CDRH). Po przekierowaniu, podobnie jak w kroku 2, należy otrzymać potwierdzenie, tj. #2.
Krok 4: Doświadczenia producentów i użytkowników urządzeń (MAUDE)
Kiedy CDRH weryfikuje i aktualizuje zgłoszenie w bazie danych zdarzeń niepożądanych (MAUDE), oczekuje się, że zgłaszający otrzyma potwierdzenie nr 3. Należy zauważyć, że wszelkie błędy, które wystąpią podczas weryfikacji i ładowania, są rejestrowane.
Raportowanie zdarzeń dotyczących wyrobów medycznych (MDR) to kluczowy proces, który pomaga ratować życie i chronić pacjentów przed niepotrzebnym ryzykiem. Zapewnia on, że wszystkie strony zaangażowane w opiekę nad pacjentem są odpowiedzialne i czujne w zakresie użytkowania wyrobów.
eMDR ułatwia raportowanie, ale dokumentacja i działania następcze mogą być zasobochłonne. Zrób to dobrze za pierwszym razem; skontaktuj się z nami pod adresem sales@freyrsolutions.com.