24. September 2016; da die Frist für die Einhaltung der Vorschriften zum Unique Device Identifier (UDI) für Medizinprodukte der Klasse II nur noch einen Monat entfernt ist, gehen wir davon aus, wenn nicht sogar sicher, dass alle Hersteller von Medizinprodukten mit einem umfassenden regulatorischen Fahrplan gut aufgestellt sind. Neben einem fundierten Verständnis der Governance-Voraussetzungen wird von den Herstellern erwartet, dass sie für die Einhaltung der Vorschriften auditbereit sind. Von der Validierung der Device Identifier (DI)- und Product Identifier (PI)-Datensätze bis hin zu erfolgreichen GUDID-Einreichungen müssen sie über die einzureichenden Daten und die einzuhaltenden Verfahren Bescheid wissen. Ob vor oder nach der Einreichung – ein besseres Wissen über das verfahrenstechnische Know-how könnte Hersteller vor entsprechenden Herausforderungen schützen, die die Datenaggregation, die Einreichung von DI-Datensätzen, die Verwaltung von Geräteberichten, die Nachverfolgung von HA-Bestätigungen usw. betreffen.
Um Hersteller in solchen Szenarien besser zu unterstützen, stellen wir hier eine leicht verständliche Infografik zu den Herausforderungen und Lösungen der UDI-Konformität bereit. Diese könnte Ihnen dabei helfen, die Komplexität der Compliance zu entschlüsseln, besser vorauszuplanen und den Fahrplan zu strukturieren.
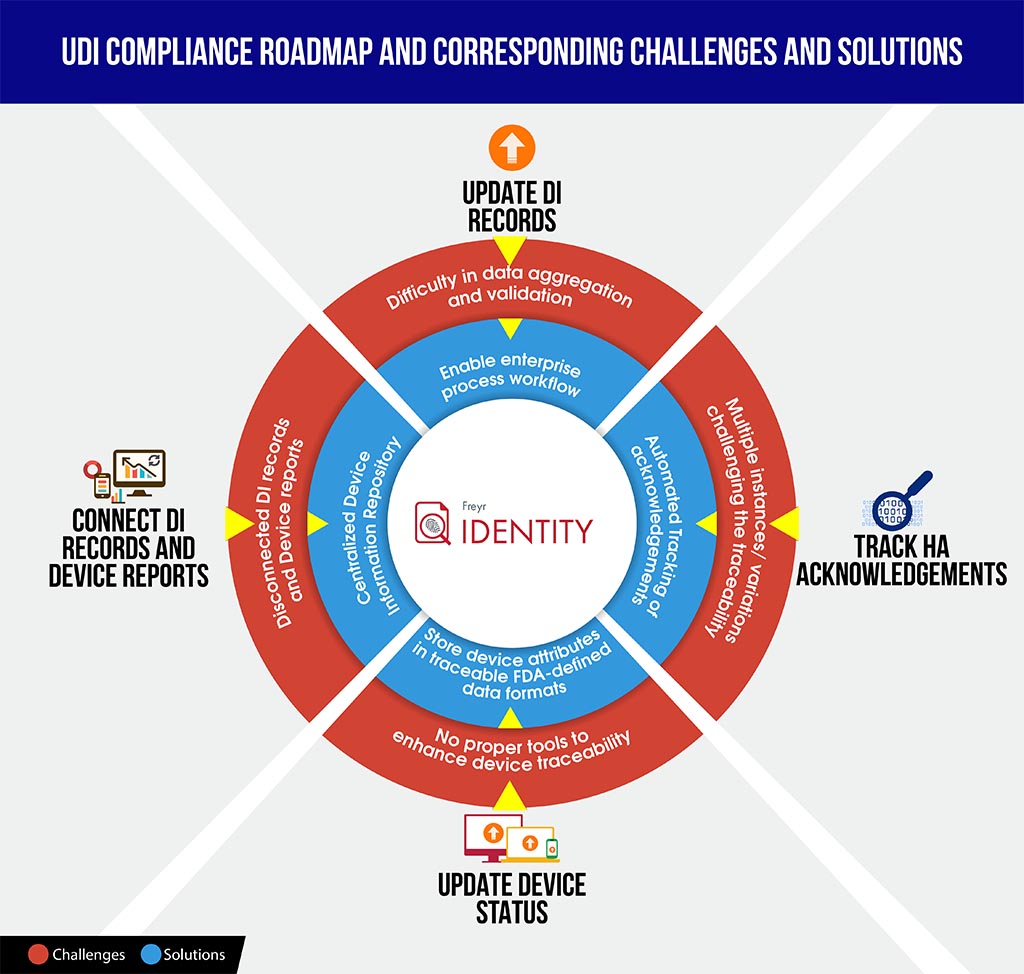
Um Ihre Organisation reibungslos durch diesen komplexen Konformitätsprozess zu führen, bietet Freyr das Beste aus zwei Welten – eine On-Demand, vollständig konfigurierbare UDI-Softwarelösung, Freyr IDENTITY, sowie ein UDI Centre of Excellence (CoE), das erstklassige, kostengünstige und anpassbare UDI-Dienstleistungen bietet, die auf Ihre einzigartigen und anspruchsvollen Anforderungen zugeschnitten sind.









