
Die Kennzeichnung von Arzneimitteln ist einer der am strengsten kontrollierten Aspekte der Einhaltung gesetzlicher Vorschriften. Schon ein kleiner Fehler kann erhebliche Folgen sowohl für die Patientensicherheit als auch für den Ruf eines Unternehmens haben. Betrachten Sie folgende Erkenntnisse:
- 20 % der Pharma- und Medizintechnikunternehmen melden monatlich Probleme bei der Qualitätskontrolle im Bereich der Kennzeichnung.
- Studien haben gezeigt, dass 40 % der Arzneimitteletiketten in bestimmten Märkten die behördlichen Anforderungen nicht erfüllen und häufig wichtige Sicherheitshinweise fehlen.
- Laut Zusammenfassungen vonFDA US FDA sind weltweit 35–40 % der Produktrückrufe auf Fehler bei der Verpackung und Kennzeichnung zurückzuführen.
- Bei behördlichen Prüfungen beziehen sich über 50 % der Beanstandungen auf die Dokumentation zur Kennzeichnung, von der Fachinformation bis hin zu artwork Übersetzungen.
Diese Statistiken unterstreichen eine Tatsache: Entscheidungen zur Indikationszuweisung müssen präzise, evidenzbasiert und umfassend begründet sein. Der Grundstein für diese Begründung liegt in der klinischen Gesamtbetrachtung und in systematischen Literaturrecherchen.
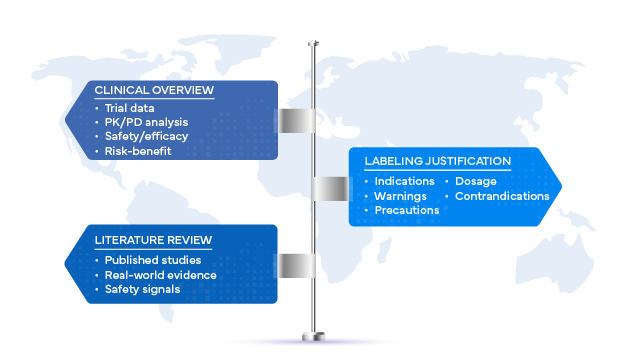
Die Rolle des klinischen Überblicks
Der klinische Überblick im Sinne von ICH (R2) ist mehr als nur eine behördliche Formalität. Es handelt sich um eine strukturierte, kritische Analyse aller verfügbaren klinischen Daten, die die Entwicklung eines Produkts untermauern. In Verbindung mit der Produktinformation spielt er eine entscheidende Rolle dabei, sicherzustellen, dass die Sicherheit, die Wirksamkeit und das Nutzen-Risiko-Profil in der Verschreibungsinformation klar dargestellt werden.
Zu den wichtigsten Beiträgen des klinischen Überblicks zur Kennzeichnung gehören:
- Die Ergebnisse klinischer Studien direkt mit den Produktversprechen verknüpfen
- Begründung für die Aufnahme von Warnhinweisen, Vorsichtsmaßnahmen und Kontraindikationen
- Gewährleistung der Übereinstimmung zwischen Sicherheitsergebnissen und Kennzeichnungsentscheidungen
- Den Aufsichtsbehörden eine transparente, faktenbasierte Nutzen-Risiko-Analyse vorlegen
Wenn beispielsweise Studiendaten ein statistisch signifikantes unerwünschtes Ereignis in einer Untergruppe aufzeigen, stützt die klinische Übersicht die Begründung für die Aufnahme untergruppenspezifischer Warnhinweise in die Produktinformation.
Warum Literaturrecherchen unverzichtbar sind
Während Daten aus klinischen Studien die Grundlage für die Begründung der Produktkennzeichnung bilden, erweitern systematische Literaturübersichten die Evidenzbasis, indem sie Erkenntnisse einbeziehen, die über die vom Sponsor durchgeführten Studien hinausgehen. Diese Übersichten fassen begutachtete Publikationen, Erkenntnisse aus der Praxis und Sicherheitsdaten aus der Zeit nach der Markteinführung zusammen, um den Zulassungsbehörden eine umfassendere und unvoreingenommene Perspektive zu bieten.
Eine fundierte Literaturrecherche hilft Unternehmen dabei,
- Sicherheitsangaben durch unabhängige Quellen überprüfen
- Frühwarnsignale oder Nebenwirkungen erkennen, die in klinischen Studien nicht erkennbar waren
- Ergebnisse im Vergleich zu Konkurrenzprodukten oder klassenweiten Effekten
- Die Kern-Datenblätter (CCDS) mit den regionsspezifischen lokalen Produktdokumenten (LPD) abstimmen
So können beispielsweise veröffentlichte Studien oder Metaanalysen seltene, aber schwerwiegende unerwünschte Ereignisse aufzeigen, was die Begründung für die Aufnahme oder Aktualisierung einer Sicherheitshinweis in der Packungsbeilage untermauert.
Regulatorische Anforderungen an die Begründung der Kennzeichnung
Internationale Gesundheitsbehörden, darunter die US FDA, EMA, MHRA und PMDA, erwarten, dass die Begründungen für die Kennzeichnung wissenschaftliche Genauigkeit, Transparenz und Konsistenz widerspiegeln. Die Prüfbeamten der Zulassungsbehörden bewerten häufig:
- Evidenzhierarchie: Vorrang für Daten aus randomisierten kontrollierten Studien, unter Berücksichtigung relevanter Beobachtungsstudien oder Studien aus der Praxis
- Dokumentübergreifende Konsistenz: Sicherstellung der Übereinstimmung zwischen der klinischen Übersicht, der Zusammenfassung der klinischen Sicherheit (SCS) und dem vorgeschlagenen Beipackzettel
- Eindeutige Begründung: Darlegung, warum jede Indikation, Dosierungsempfehlung oder Warnung aufgenommen (oder ausgeschlossen) wurde
Wird keine klare wissenschaftliche Grundlage für die Kennzeichnung vorgelegt, kann dies zu Rückfragen der Zulassungsbehörde, verlängerten Prüfungsfristen oder sogar zur Ablehnung führen.
Bewährte Verfahren zur Begründung von Kennzeichnungsentscheidungen
Pharmazeutische Unternehmen können ihre Zulassungsanträge durch die Anwendung dieser bewährten Verfahren verbessern:
- Funktionsübergreifende Zusammenarbeit: Einbeziehung der Teams aus den Bereichen Klinik, Sicherheit und Zulassung für eine ganzheitliche Interpretation
- Technologie nutzen: Setzen Sie KI-gestützte Tools für Literaturrecherchen ein, um die Sichtung und Extraktion zu beschleunigen
- Dokumentationspfade pflegen: Die Gründe für die Einbeziehung bzw. den Ausschluss von Studien dokumentieren, um den Anforderungen behördlicher Prüfungen gerecht zu werden
- Weltweiter Vergleich: Passen Sie sich an Konkurrenzprodukte und sich weiterentwickelnde Richtlinien an, um Compliance-Lücken zu schließen
- Kontinuierliche Aktualisierung: Einbeziehung neuer wissenschaftlicher Erkenntnisse und Pharmakovigilanzdaten in die laufenden Strategien zur Kennzeichnung
Fazit
Angesichts der beispiellos strengen behördlichen Kontrollen und der steigenden Kosten bei Nichteinhaltung der Vorschriften können es sich Unternehmen nicht leisten, sich bei der Erstellung von Produktkennzeichnungen auf Annahmen zu verlassen. Eine fundierte klinische Übersicht in Verbindung mit umfassenden Literaturrecherchen stellt sicher, dass jede Angabe durch transparente, wissenschaftliche Belege untermauert ist.
Wir bei Freyr Solutions unterstützen globale Pharmaunternehmen dabei, diese Komplexität zu bewältigen. Dank unserer end-to-end in den Bereichen regulatorische Kennzeichnung, klinische Dokumentation und Compliance-Strategien stellen wir sicher, dass Ihre Kennzeichnungsentscheidungen wissenschaftlich fundiert, behördlich konform und weltweit einheitlich sind.
Arbeiten Sie noch heute mit Freyr zusammen, um Ihre Kennzeichnungsstrategie mit wissenschaftlich fundierten Begründungen zu untermauern, denen die Aufsichtsbehörden vertrauen und auf die sich Patienten verlassen.










