Einreichungen geplant für den 24. September 2016.
Nachdem die zweite Phase der UDI-Konformität für Medizinprodukte der Klasse III I/LS/LS umgesetzt wurde, fragen sich viele Hersteller von Medizinprodukten, insbesondere solche der Klasse II, wie sie sich am besten auf die Frist für die Einreichung von Daten für Medizinprodukte der Klasse II am 24. September 2016 vorbereiten können. Um ihnen einen Vorsprung zu verschaffen, haben wir bei Freyr einige Voraussetzungen identifiziert, die sie berücksichtigen sollten, um Medizinprodukte der Klasse II für die Einhaltung des UDI-Mandats der FDA vorzubereiten.
Die neue Verordnung verlangt, dass alle Medizinprodukte der Klasse II mit einem Unique Device Identifier (UDI) gekennzeichnet und verpackt und in die Global Unique Device Identification Database (GUDID) der FDA eingetragen werden. Angesichts der Volatilität der Compliance-Anforderungen und kürzerer Einreichungsfristen besteht die Herausforderung für Medizinproduktehersteller darin, die Feinheiten der Compliance-Prozesse genau zu kennen. Gleichzeitig müssen sie sicherstellen, dass keine der wichtigen Produktmerkmale übersehen wird, wenn sie die verstreuten Produktdaten aus verschiedenen Systemen zusammenführen und in Tabellenkalkulationen abgleichen, um Compliance-Berichte zu erstellen.
Um Medizinprodukteherstellern zu helfen, diesen zeitkritischen und komplexen Compliance-Prozess fehlerfrei zu durchlaufen, hat Freyr die folgenden Voraussetzungen zusammengestellt, die zu beachten sind.
Das UDI-Konformitätsdatum bestimmen: Seit die FDA ihre endgültige Vorschrift erlassen hat, wurden einige der Konformitätsfristen für Produkte geändert und verlängert. Um Konformitätsstrategien und -prozesse sorgfältig im Voraus zu planen und übereilte Änderungen in letzter Minute zu vermeiden, sollten Kennzeichnungspflichtige das genaue Konformitätsdatum ermitteln.
Frist zur Einhaltung der Vorschriften für Medizinprodukte der Klasse II Anforderungen an die Einhaltung der Vorschriften 24. September 2016Medizinprodukte der Klasse III, die mit einer UDI gekennzeichnet werden müssen, müssen eine UDI als dauerhafte Kennzeichnung auf dem Produkt selbst tragen, sofern das Produkt mehrfach verwendet und vor jeder Verwendung wiederaufbereitet werden soll. Die Etiketten und Verpackungen von Medizinprodukten der Klasse II müssen eine UDI tragen Datumsangaben auf den Etiketten dieser Produkte müssen wie vorgeschrieben formatiert sein Eigenständige Software der Klasse II muss ihre UDI wie vorgeschrieben bereitstellen Daten für Medizinprodukte der Klasse II, die mit einer UDI gekennzeichnet werden müssen, müssen an die GUDID-Datenbank übermittelt werden Für die meisten Produkte unterscheidet sich die Frist für die Direktkennzeichnung von den anderen Anforderungen. Je nachdem, ob Ihr Produkt zur Wiederverwendung oder Wiederaufbereitung vorgesehen ist, bestimmen Sie das Compliance-Datum für die UDI-Direktkennzeichnung wie hier gezeigt:
Fristen für die Direktkennzeichnung Produktkategorie – Wiederverwendet und wiederaufbereitet 24. September 2015 Lebenserhaltende und lebensunterstützende Produkte, unabhängig von der Produktklasse 24. September 2016 Medizinprodukte der Klasse III und Produkte, die gemäß dem Public Health Service Act zugelassen sind 24. September 2018 Medizinprodukte der Klasse II 24. September 2020 Medizinprodukte der Klasse I und nicht klassifizierte Produkte Bewerten Sie die Notwendigkeit einer Direktkennzeichnung der UDI-Nummer: Alle Medizinprodukte, die mehr als einmal verwendet oder vor jeder Verwendung wiederaufbereitet werden, müssen eine Direktkennzeichnung der UDI aufweisen. Eine Ausnahme bilden implantierbare Produkte, die gemäß der UDI-Regel keine Direktkennzeichnung benötigen. Produkte, die zum einmaligen Gebrauch bestimmt sind, auch wenn sie wiederaufbereitet werden, müssen ebenfalls keine dauerhafte UDI tragen – 21 CFR 801.45(d)(3). Bewerten Sie daher die Notwendigkeit einer Direktkennzeichnung basierend auf der Kategorie der von Ihnen hergestellten Medizinprodukte.
- Plan für umfassende Compliance: Überprüfen Sie die FDA-Anforderungen für Ihre spezifischen Produkte, die eingehalten werden müssen. Führen Sie eine umfassende Lückenanalyse durch, um Mängel in Bezug auf Daten oder Technologie zu identifizieren und einige der größten Herausforderungen bei der Einhaltung der strengen FDA-Fristen zu bewältigen. Zu den Herausforderungen könnten die Beschaffung von DI- oder PI-Informationen sowie die Verarbeitung großer Mengen unstrukturierter Daten aus verschiedenen Quellen gehören. Anstatt in letzter Minute unter Hochdruck alle Daten zu Medizinprodukten abzugleichen, planen Sie eine umfassende Konformität im Voraus mithilfe validierter Systeme und Tools, die Datenintegration, Datenqualität und Datenmanagement unterstützen.
![]()
DI-Nummer und Agenturmitgliedschaft erhalten: Die UDI setzt sich zusammen aus dem Device Identifier (DI – eine eindeutige Nummer, die auf der Version oder dem Modell des Produkts basiert) und dem Product Identifier (PI – enthält Chargennummer, Seriennummer oder Verfallsdatum). Der DI-Teil der UDI dient als Primärschlüssel, um Informationen über das Produkt in der GUDID nachzuschlagen. Zur Zuweisung des DI hat die FDA drei Vergabestellen akkreditiert – GS1, HIBCC und ICCBBA. In diesem Szenario müssen Kennzeichnungspflichtige Mitgliedschaft bei einer dieser Agenturen erwerben, um die DI-Nummer zu erhalten, die in die GUDID der FDA eingegeben werden muss.
![]()
Identifikator Merkmale Ausgebende Stellen UDI DI (Device Identifier – Statische Daten)
Muss mit GUDID synchronisiert werdenEindeutige Nummer von
Hersteller
Gerätehersteller
Gerätemodell
GSI
HIBCC
ICCBBAPI (Produktidentifikator – Dynamische Daten)
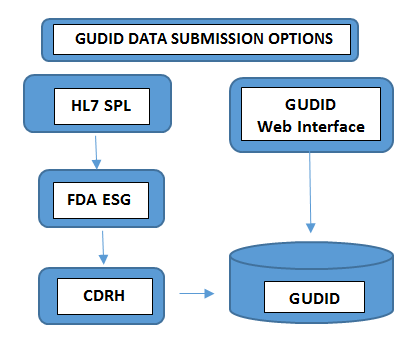
Auf allen Verpackungsebenen erforderlichChargennummer, Seriennummer, Herstellungsdatum, Verfallsdatum, - Daten übermitteln: Die Art und Weise, wie Sie Daten an die GUDID übermitteln, hängt vom Umfang Ihrer Produktportfolios ab. Hersteller mit einer geringen Anzahl von Produkten entscheiden sich dafür, die UDI-Informationen manuell über die kostenlose GUDID-Webschnittstelle der FDA einzureichen. In diesem Fall kann jeweils nur ein DI-Datensatz über eine gesicherte GUDID-Webschnittstelle eingereicht werden. Im anderen Fall wählen Hersteller mit größeren Produktportfolios die HL7 SPL-Einreichungsoption, um Daten elektronisch zu erfassen und die konsolidierten Daten in das SPL-Format zu konvertieren, bevor sie diese unter Verwendung der DUNS-Nummer an das Electronic Submission Gateway (ESG) der FDA übermitteln. Bitte beachten Sie, dass das GUDID-Konto nicht vom Einreichungstyp abhängt. Das Konto dient dazu, Sie als Kennzeichnungspflichtigen zu identifizieren und die Einreichung von Produktdaten über beide Optionen zu ermöglichen.
![]()
- Ein GUDID-Konto einrichten: Ein Kennzeichnungspflichtiger / Produkthersteller benötigt ein oder mehrere GUDID-Konten, abhängig von der Anzahl der zuzuweisenden Rollen; zum Beispiel GUDID-Koordinator, Dateneingabe-Benutzer usw. Um jedoch jede Rolle für die Dateneingabe zu autorisieren, benötigt der Hersteller eine Genehmigung der FDA vor der Kontoerstellung. Der Prozess zur Erstellung eines geeigneten GUDID-Kontos beinhaltet das Senden einer E-Mail-Anfrage an die FDA, woraufhin Sie als Antragsteller ein Dokument zur Kontoanfrage erhalten, das Sie ausfüllen müssen. Sobald Sie das ausgefüllte Dokument per E-Mail an die FDA zurücksenden, prüft die Behörde das Formular und sendet Ihnen dann eine E-Mail mit den Anmeldeinformationen für das GUDID-Konto.
Die UDI-Implementierung ist ein komplexer und zeitaufwändiger Prozess. Dabei stehen Hersteller von Medizinprodukten bei der Erfüllung der UDI-Anforderungen der FDA vor vielen Herausforderungen in Bezug auf Datenmanagement, Datenintegration und Datenübermittlung. Da die Frist für die Einhaltung der Vorschriften für Medizinprodukte der Klasse II nur noch ein Jahr entfernt ist, empfiehlt Freyr den Unternehmen, sofort damit zu beginnen.
Um Ihr Unternehmen durch diesen komplexen Konformitätsprozess zu führen, bietet Freyr das Beste aus zwei Welten – eine bedarfsgerechte, vollständig konfigurierbare UDI-Softwarelösung, Freyr IDENTITY, sowie ein Kompetenzzentrum (CoE), das erstklassige, kostengünstige und anpassbare UDI-Dienstleistungen anbietet, die auf Ihre einzigartigen und anspruchsvollen Anforderungen zugeschnitten sind.