
Kombinationsprodukte, also Produkte, die Medikamente, Medizinprodukte oder Biologika kombinieren, stellen besondere Herausforderungen bei der regulatorischen Kennzeichnung dar. Da diese Produkte aus mehreren Komponenten und unterschiedlichen regulatorischen Standards bestehen, müssen Hersteller sicherstellen, dass sie alle individuellen Anforderungen erfüllen und Sicherheitsinformationen korrekt übermitteln.
Dieser Blog beleuchtet die Herausforderungen bei der Kennzeichnung von Kombinationsprodukten und bietet Strategien zur Bewältigung der regulatorischen Kennzeichnungsanforderungen, wobei Patientensicherheit und Compliance im Vordergrund stehen. Abbildung 1 unten zeigt die größten Herausforderungen bei der Kennzeichnung von Kombinationsprodukten.
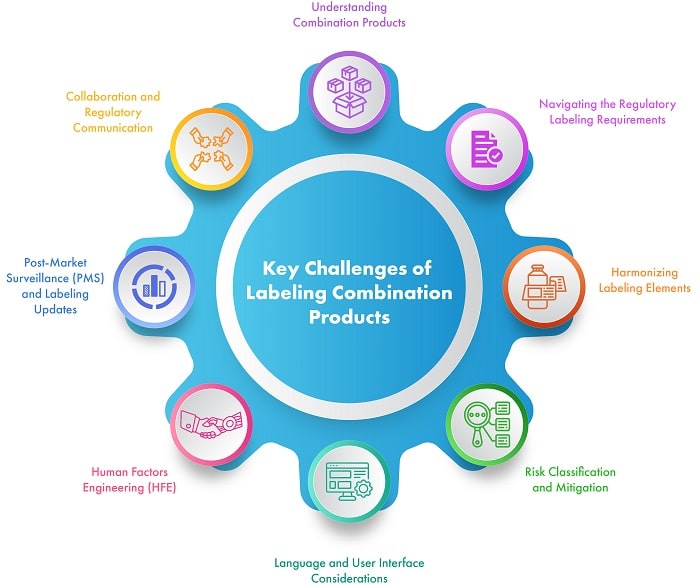
Abbildung 1: Hauptprobleme bei der Kennzeichnung von Kombinationsprodukten
Betrachten wir nun jede Herausforderung im Detail:
- Kombinationsprodukte verstehen: Kombinationsprodukte vereinen verschiedene Komponenten, zum Beispiel ein Produkt aus einem Arzneimittel und einem Medizinprodukt, um innovative Behandlungsoptionen anzubieten. Die Zusammenführung unterschiedlicher regulatorischer Rahmenbedingungen und Anforderungen kann jedoch den Kennzeichnungsprozess erschweren. Es ist daher entscheidend, die grundlegende Funktionsweise und die relevanten Vorschriften für jede Komponente zu kennen.
- Umgang mit den regulatorischen Kennzeichnungsvorschriften: Kombinationsprodukte müssen sowohl Arzneimittel- als auch Medizinproduktgesetze einhalten, was die Einhaltung verschiedener regulatorischer Vorgaben erfordert. Arbeiten Sie eng mit Experten für Regulatory Affairs zusammen, um die spezifischen Kennzeichnungsvorschriften von Behörden wie der USFDA, der EMA und anderen relevanten Stellen zu verstehen und zu erfüllen.
- Harmonisierung der Kennzeichnungselemente: Die Harmonisierung der Kennzeichnungselemente über verschiedene Komponenten von Kombinationsprodukten hinweg ist entscheidend, um medizinischem Fachpersonal und Patienten klare und konsistente Informationen zu liefern. Stellen Sie sicher, dass die Kennzeichnung die kombinierte Funktionalität genau wiedergibt und wesentliche Anweisungen, Warnhinweise und Gebrauchsanweisungen (IFUs) vermittelt.
- Risikoklassifizierung und -minderung: Identifizieren und klassifizieren Sie die Risiken, die mit jeder Komponente des Kombinationsprodukts verbunden sind. Bewerten Sie die potenziellen Risiken und legen Sie geeignete Minderungsstrategien fest. Kommunizieren Sie diese Risiken zusammen mit den entsprechenden Vorsichtsmaßnahmen und Warnhinweisen auf dem Produktetikett, um die Patientensicherheit und die Einhaltung der regulatorischen Kennzeichnungsanforderungen zu gewährleisten.
- Sprach- und Benutzeroberflächenaspekte: Berücksichtigen Sie die sprachlichen Anforderungen für die Kennzeichnung, wenn Kombinationsprodukte international vermarktet werden. Übersetzen und lokalisieren Sie den Kennzeichnungsinhalt, um den Vorschriften in verschiedenen Regionen zu entsprechen und die Sprachpräferenzen der Zielgruppe zu berücksichtigen. Gestalten Sie außerdem benutzerfreundliche Schnittstellen, die die sichere und effektive Nutzung von Kombinationsprodukten erleichtern.
- Human Factors Engineering (HFE): Die Benutzerfreundlichkeit von Kombinationsprodukten ist entscheidend für die Patientensicherheit. Wenden Sie HFE-Prinzipien an, um sicherzustellen, dass die Kennzeichnung und die Gebrauchsanweisungen intuitiv, leicht verständlich und mit der Benutzeroberfläche der Medizinproduktkomponente kompatibel sind. Führen Sie Usability-Tests durch und überarbeiten Sie das Design, um das Fehlerrisiko zu reduzieren und die Benutzererfahrung zu optimieren.
- Überwachung nach dem Inverkehrbringen (PMS) und Aktualisierungen der Kennzeichnung: Überwachen Sie kontinuierlich die Sicherheit und Leistung von Kombinationsprodukten durch PMS. Erfassen und analysieren Sie umgehend unerwünschte Ereignisse und neu auftretende Sicherheitsbedenken. Aktualisieren Sie die Kennzeichnung bei Bedarf, um neue Informationen, Sicherheitshinweise oder Änderungen der Indikationen widerzuspiegeln.
- Zusammenarbeit und regulatorische Kommunikation: Die Kennzeichnung von Kombinationsprodukten erfordert eine enge Zusammenarbeit zwischen den Teams für Regulierung, Qualität und Marketing. Etablieren Sie effektive Kommunikationskanäle mit den Aufsichtsbehörden, um Leitlinien einzuholen, Anforderungen zu klären und die Compliance während des gesamten Kennzeichnungsprozesses sicherzustellen. Nutzen Sie das Fachwissen funktionsübergreifender Teams, um eine umfassende und konforme Kennzeichnung zu entwickeln.
Fazit
Die Kennzeichnung von Kombinationsprodukten erfordert die Navigation durch komplexe regulatorische Rahmenbedingungen, die Berücksichtigung der Risikoklassifizierung und die Sicherstellung einer effektiven Kommunikation von Sicherheitsinformationen. Durch das Verständnis der einzigartigen Herausforderungen, die Harmonisierung der Kennzeichnungselemente und die Nutzung von regulatorischem Fachwissen können Hersteller die Herausforderungen problemlos bewältigen und Compliance sowie Patientensicherheit priorisieren.
Achten Sie sorgfältig auf die regulatorischen Anforderungen und kennzeichnen Sie Ihre Kombinationsprodukte präzise, damit medizinisches Fachpersonal und Patienten diese sicher und effektiv anwenden können. Eine Partnerschaft mit einem Experten wie Freyr kann Ihren Aufwand minimieren. Kontaktieren Sie uns, um mehr zu erfahren!










