Die Gesundheitsbehörden aller Länder – mit Ausnahme Kanadas – verlangen von allen ausländischen Medizinprodukteherstellern, einen lokalen, im Land ansässigen oder bevollmächtigten Vertreter zu benennen. Die Aufgabe eines gesetzlichen Vertreters besteht darin, den Hersteller und das Produkt im Zielland zu vertreten und als Verbindungsstelle zwischen den Gesundheitsbehörden und den ausländischen Herstellern zu fungieren. Für einen lokalen Vertreter gibt es länderspezifische Bezeichnungen. Der lokale Vertreter in den USA wird als US bezeichnet, während er im Vereinigten Königreich als UKRP United Kingdom Responsible Person) bezeichnet wird. In Sri Lanka wird der lokale Vertreter als Sri Lanka Local Agent oder Sri Lanka Authorized Representative bezeichnet, der gleichzeitig der Inhaber der Marktzulassung (MAH) für das Produkt ist.
Ausländische Medizinproduktehersteller können ihren Vertriebspartner als lokalen Vertreter benennen, der dann standardmäßig auch als Inhaber der Marktzulassung (MAH) fungiert. Es wird jedoch empfohlen, einen unabhängigen Dienstleister ohne geschäftliche Interessenkonflikte als MAH zu benennen. Die Vorteile der Benennung eines unabhängigen Dienstleisters als MAH nachstehend aufgeführt. Ein MAH :
- Kompetenz in länderspezifischen regulatorischen Angelegenheiten und PMS-Anforderungen
- Geschäftsziele durch die Ernennung mehrerer Distributoren zur Marktdurchdringung erreichen
- Fähigkeit, sich auf die Einhaltung regulatorischer Vorschriften zu konzentrieren
- Technisch kompetent, um die von der Agentur gestellten Fragen zu beantworten
- Einheitliche Etiketten für einen einzigen MAH Land
- Vermeiden Sie den Aufwand, Etiketten aktualisieren zu müssen, falls es zu einem Wechsel des Vertriebshändlers kommt, der gleichzeitig als Zulassungsinhaber MAH Vertreter fungiert
In einigen Ländern, z. B. in Indien, gibt es keine Regelung zur Übertragung der Marktzulassung, sodass ein neuer Antrag gestellt werden muss. Im Gegensatz dazu erlaubt die Nationale Arzneimittelbehörde (NMRA) in Sri Lankadie Übertragung MAH . Die größte Herausforderung für ausländische Medizinproduktehersteller beim Wechsel des MAH die Anforderung, eine Unbedenklichkeitsbescheinigung (NoC/NoL) des derzeitigen aktiven MAH vorzulegen. Die NMRA erleichtert zudem die MAH , selbst wenn ein MAH , eine Unbedenklichkeitsbescheinigung auszustellen.
Eine Änderung des Namens und/oder der Anschrift des Inhabers MAH in Sri Lanka MAH nicht als Übertragung der Marktzulassung, sofern es sich bei dem Inhaber um dieselbe Person oder Einrichtung handelt; eine solche Änderung ist im Rahmen eines Antrags auf Änderung nach der Zulassung mitzuteilen. Der Hersteller muss sich direkt an die NMRA wenden, wenn er beabsichtigt, die Angaben zum MAH zu ändern, MAH in dem Antrag MAH , der sich noch in der Prüfung durch die NMRA befindet.
Die Notwendigkeit einer Übertragung der MAH aus Situationen, in denen der Hersteller beschließt, sich von der bestehenden Zulassung zu trennen, oder wenn die bestehende Zulassung von einer anderen juristischen Person übernommen wird. Der MAH übertragende MAH wird als „Übertragender“ bezeichnet, während das Unternehmen, die Personengesellschaft, die natürliche Person oder die juristische Person, an die die Übertragung erfolgen soll, als „Übernehmer“ bezeichnet wird.
Damit der Prozess MAH eingeleitet werden kann, muss der Übertragende eine Einverständniserklärung (No Objection Letter, NOL) ausstellen, in der er der Übertragung zustimmt. Verweigert der Übertragende die Ausstellung der Einverständniserklärung, räumt die Behörde eine Frist von 14 Tagen ein, um Einwände gegen die Benennung des Übernehmers (neuer MAH) einzureichen. Ist der Grund für den Einwand stichhaltig und betrifft er den Hersteller, fordert die Behörde den Hersteller auf, den Einwand auszuräumen, und setzt den Übertragungsprozess fort. Sollte der Übertragende in einem geschäftlichen Konflikt mit dem Übernehmer oder dem Hersteller stehen, wird die NMRA den Übertragungsprozess fortsetzen, da die Behörde vorrangig die Verfügbarkeit des Produkts auf dem srilankischen Markt im Blick hat und nicht etwaige geschäftliche Verpflichtungen zwischen den verschiedenen Beteiligten.
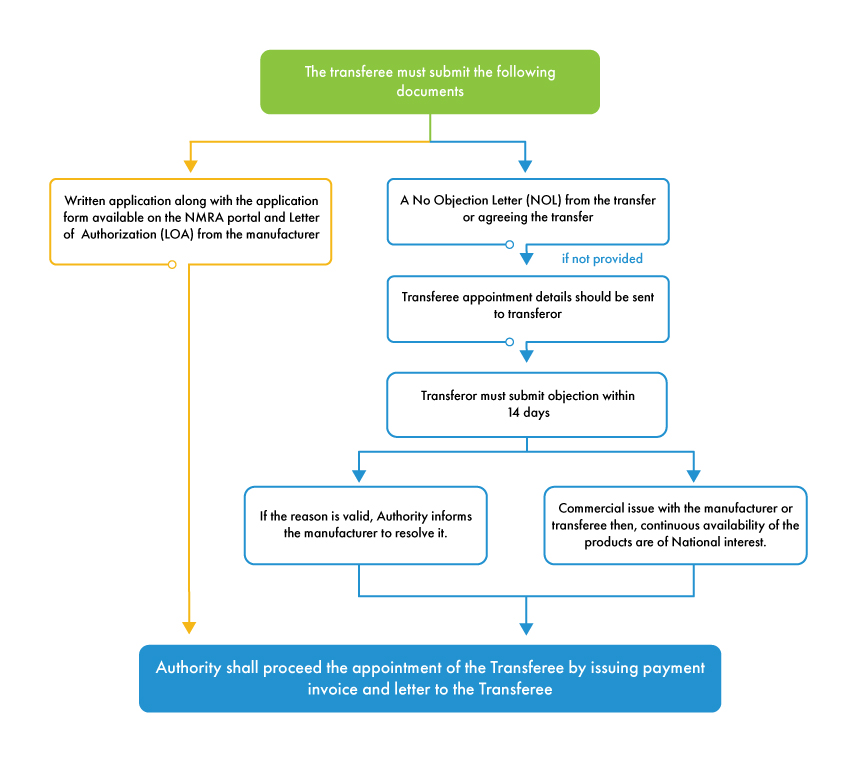
Im Gegensatz zu anderen Ländern sind die Vorschriften der NMRA hinsichtlich MAH für ausländische Hersteller vorteilhaft. Die NMRA gestattet MAH bei Vorlage aller erforderlichen Unterlagen, sofern der vom Übertragenden vorgebrachte Einwand nicht wesentlich und begründet ist. Für alle ausländischen Hersteller ist es von Vorteil, einen unabhängigen MAH zu benennen, MAH Komplikationen beim Zulassungsverfahren für ihre Produkte in Sri Lanka zu vermeiden. Die Unterstützung durch lokale Vertreter für Medizinprodukte in Sri Lanka bietet allen ausländischen Herstellern eine Plattform, um den MAH und mit den entsprechenden Unterlagen zu benennen und zu wechseln.
Wenn SieMAH eines lokalen Vertreters oder eines Inhabers der MAH (MAH ) oder Dienstleistungen im Zusammenhang mit MAH in Sri Lanka benötigen, reach einen regionalen Experten für Zulassungsfragen. Bleiben Sie auf dem Laufenden. Halten Sie die Vorschriften ein.









