
Da die Verwendung von Arzneimitteln erhebliche Auswirkungen auf die Gesundheit und das Wohlbefinden eines Patienten haben kann, müssen die Informationen auf dem Etikett klar und korrekt sein. Dies gilt insbesondere für Gebrauchsanweisungen, Verfallsdaten und Inhaltsstofflisten. Daher ist eine Überprüfung der pharmazeutischen Kennzeichnungsprozesse erforderlich.
Als wichtiger Bestandteil der Einhaltung regulatorischer Vorschriften ist die Datenrichtigkeit eines der wichtigsten Kriterien bei der Kennzeichnung von Arzneimitteln. Laut Studien der FDA und MHRA sind etwa 51 Prozent der Audit-Probleme mit kennzeichnungsbezogenen Dokumenten verbunden.
Die fünf (05) häufigsten Audit-Probleme, die in den wichtigsten Audit-Ergebnissen der Gesundheitsbehörden zur Kennzeichnung hervorgehoben wurden, sind folgende:
- Abweichung von SOPs
- CCDS & CSI Informationen
- Versionsverwaltung
- Unzureichende Nachverfolgung
- Dezentralisierung
Die oben genannten Probleme können bei Fusionen und Übernahmen, bei mehreren in verschiedenen Ländern zugelassenen Produkten und bei Änderungen in der lokalen Kennzeichnung auftreten.
Hauptgründe für Probleme bei Audits zur pharmazeutischen Kennzeichnung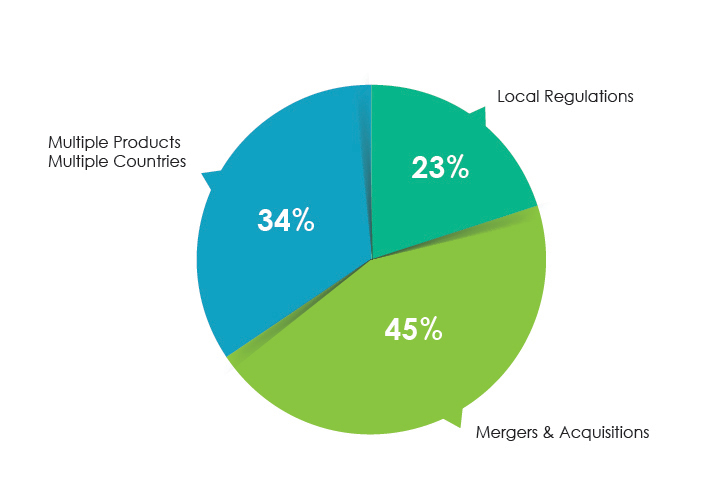
Die Nichteinhaltung der Anforderungen regulatorischer Standards zur Offenlegung von Produktsicherheitsinformationen oder die Weitergabe solcher Informationen kann:
- Die Patientensicherheit gefährden: Jegliche Ungenauigkeiten in der Kennzeichnung könnten zur falschen Anwendung eines Medikaments führen, was negative Auswirkungen haben und in einigen Fällen tödlich sein kann.
- Für Unternehmen kostspielig sein: Der Rückruf eines Produkts aufgrund eines Kennzeichnungsfehlers ist ein kostspieliger Prozess, der sich negativ auf das Geschäftsergebnis eines Unternehmens auswirken kann, sei es auf die Rentabilität oder das Markenimage.
- Zeitaufwändig: Wenn es eine Lücke in den Kennzeichnungsinformationen gibt, kann die Untersuchung eines Kennzeichnungsproblems für die Gesundheitsbehörde zeitaufwändig sein.
- Reputationsschaden: Wird ein Produkt vom Markt zurückgerufen, kann dies sogar das Markenimage beeinträchtigen und sich anschließend nachteilig auf den Ruf eines Unternehmens auswirken.
In solchen Szenarien, wie stellen Sie sicher, dass Ihr Verfahren zur Kennzeichnung pharmazeutischer Produkte die erforderlichen Kriterien erfüllt?
Automatisierung für die Einhaltung der Kennzeichnungsvorschriften nutzen
Automatisierung ist, wie in vielen anderen Bereichen auch, entscheidend für die Sicherstellung der globalen Einhaltung von Kennzeichnungsvorschriften. Darüber hinaus reduziert Automatisierung menschliches Eingreifen und gewährleistet die Entwicklung hochwertiger Ergebnisse, die die gesamten Betriebskosten erheblich senken und die Markteinführungszeit der Produktlinien eines Unternehmens verbessern.
Heute ist die beste Methode, um die Einhaltung der regulatorischen Kennzeichnungsvorschriften erfolgreich zu gewährleisten, in ein umfassendes Tool für das Etiketten-Lebenszyklus-Management zu investieren. Durch die Auslagerung globaler Kennzeichnungsvorgänge an spezialisierte Anbieter von End-to-End-Software für das Etikettenmanagement können Pharmahersteller auf ein effektives und optimiertes Etikettenmanagement setzen.










