
Zamienność z referencyjnym produktem biologicznym jest kluczowym krokiem w procesie zatwierdzania leków biopodobnych. Zapewnia to, że lek biopodobny może być zastąpiony produktem referencyjnym bez znaczącego ryzyka zmniejszonej skuteczności lub zwiększonych obaw dotyczących bezpieczeństwa. Ten blog ma na celu zrozumienie najnowszej aktualizacji FDA dotyczącej kwestii osiągnięcia zamienności oraz najlepszych praktyk branżowych w osiąganiu doskonałości regulacyjnej.
Definiowanie zamienności
Osiągnięcie zamienności to złożony i rygorystyczny proces, który wymaga spełnienia surowych wymogów regulacyjnych. Wyzwanie polega na wykazaniu, że lek biopodobny nie tylko odpowiada produktowi referencyjnemu pod względem bezpieczeństwa i skuteczności, ale także zapewnia te same wyniki kliniczne u każdego pacjenta. Niespełnienie tych wymagań może skutkować opóźnieniami lub odmowami zatwierdzenia, co wpływa na dostęp do rynku i opiekę nad pacjentem.
Wymogi regulacyjne dotyczące zamienności
FDA określa szczegółowe kryteria wykazania zamienności w swoich dokumentach wytycznych. Kryteria te obejmują:
- Porównawcze badania analityczne: Wymagane są obszerne badania analityczne, aby wykazać, że lek biopodobny jest bardzo podobny do produktu referencyjnego. Badania te oceniają strukturę molekularną, funkcję i skład leku biopodobnego.
- Badania kliniczne: Badania kliniczne są potrzebne, aby potwierdzić, że lek biopodobny nie różni się w sposób klinicznie istotny od produktu referencyjnego pod względem bezpieczeństwa, czystości i siły działania. Często obejmuje to porównawcze badania farmakokinetyczne (PK) i farmakodynamiczne (PD).
- Badania zamienności: FDA wymaga badań zamienności w celu oceny wpływu naprzemiennego stosowania leku biopodobnego i referencyjnego. Badania te są kluczowe, aby upewnić się, że zmiana nie wpływa na skuteczność ani bezpieczeństwo leczenia.
- Strategie Oceny i Łagodzenia Ryzyka (REMS): W stosownych przypadkach należy uwzględnić REMS, aby zapewnić, że lek biopodobny może być stosowany zamiennie bez dodatkowych obaw o bezpieczeństwo.
Etapy strategicznego osiągnięcia zamienności
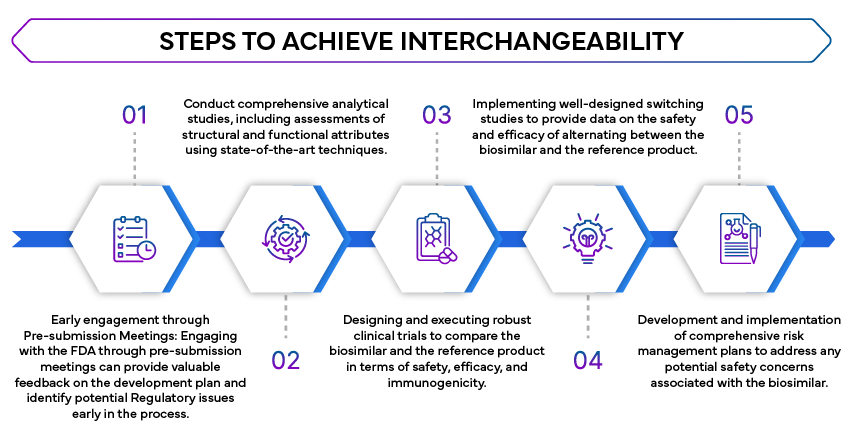
Rola partnera regulacyjnego
Partnerstwa regulacyjne mogą znacząco zwiększyć prawdopodobieństwo osiągnięcia zamienności. Oto, jak partner regulacyjny może pomóc:
- Doradztwo eksperckie: Zapewnia fachowe doradztwo w zakresie wymagań regulacyjnych i strategii spełniających wytyczne FDA.
- Wsparcie w zakresie dokumentacji: Wsparcie w przygotowaniu wysokiej jakości dokumentów zgłoszeniowych, zgodnych ze standardami regulacyjnymi.
- Projektowanie Badań Klinicznych: Wspiera projektowanie i realizację solidnych badań klinicznych i badań dotyczących zmiany leczenia.
- Interakcje z HA: Ułatwia skuteczną komunikację z HA, zapewniając terminowe i konstruktywne informacje zwrotne.
- Zarządzanie ryzykiem: Opracowanie kompleksowych strategii zarządzania ryzykiem w celu łagodzenia potencjalnych obaw dotyczących bezpieczeństwa.
Zalety posiadania partnera regulacyjnego
| Zalety | Opis | |
| 1. | Ekspertyza w wymaganiach regulacyjnych. | Dogłębne zrozumienie globalnych uwarunkowań regulacyjnych i wymagań. |
| 2. | Usprawniona Dokumentacja | Zapewnia dokładne i zgodne przygotowanie dokumentacji. |
| 3. | Sprawny proces zgłoszeniowy | Skraca czas i obniża koszty dzięki efektywnemu zarządzaniu zgłoszeniami. |
| 4. | Zwiększona zgodność. | Minimalizuje ryzyko opóźnień i odrzuceń dzięki dokładnej zgodności z przepisami. |
| 5. | Skuteczne zarządzanie ryzykiem | Proaktywne identyfikowanie i łagodzenie potencjalnego ryzyka. |
Podsumowanie
Osiągnięcie zamienności z produktem referencyjnym jest wymagającym, ale kluczowym procesem dla pomyślnego zatwierdzenia leków biopodobnych. Wymaga to kompleksowego zrozumienia wymogów regulacyjnych, skrupulatnego planowania i solidnych danych klinicznych. Współpraca z doświadczonym dostawcą usług regulacyjnych może znacznie zwiększyć szanse na sukces, zapewniając, że lek biopodobny spełnia surowe kryteria określone przez organy regulacyjne. Wykorzystując fachowe doradztwo, dokładną dokumentację i strategiczne zarządzanie ryzykiem, sponsorzy mogą skuteczniej poruszać się po złożonej ścieżce do zamienności.










