
W ostatnich latach krajobraz spraw regulacyjnych przeszedł znaczącą transformację. U podstaw tej zmiany leży rosnący nacisk na podejście skoncentrowane napacjencie, a organy ds. zdrowia (HA) na całym świecie uznają nieocenioną rolę, jaką pacjenci odgrywają w rozwoju i zatwierdzaniu nowych produktów leczniczych. Ta zmiana to nie tylko trend; to fundamentalne przemyślenie sposobu, w jaki podchodzimy do wniosków regulacyjnych i, ostatecznie, w jaki służymy tym, którzy są najważniejsi – pacjentów.
Problem:
Tradycyjnie, zgłoszenia regulacyjne koncentrowały się głównie na spełnianiu wymagań technicznych i naukowych, często pomijając bezpośredni wpływ na doświadczenia i wyniki pacjentów. To podejście, choć dokładne, czasami nie uwzględniało niuansów potrzeb pacjentów, ich preferencji i rzeczywistego stosowania produktów leczniczych. W rezultacie istniała rozbieżność między zatwierdzeniami regulacyjnymi a rzeczywistą wartością dostarczaną pacjentom.
Podejścia regulacyjne skoncentrowane na pacjencie:
Organy regulacyjne, zwłaszcza FDA i EMA, poczyniły znaczące postępy we włączaniu perspektyw pacjentów do swoich ram regulacyjnych.
To podejście zorientowane na pacjenta jest widoczne w kilku kluczowych obszarach:
- Rozwój leków skoncentrowany na pacjencie (PFDD):
Program PFDD FDA to przełomowa inicjatywa, która systematycznie zbiera opinie pacjentów w celu informowania o rozwoju leków i podejmowaniu decyzji regulacyjnych. Program ten obejmuje sesje wysłuchiwania pacjentów, spotkania publiczne oraz opracowywanie dokumentów wytycznych w celu zwiększenia zaangażowania pacjentów przez cały cykl życia produktu. - Dowody ze świata rzeczywistego (RWE):
Rośnie uznanie wartości danych ze świata rzeczywistego w rozumieniu działania produktu w różnych populacjach pacjentów. HAs są obecnie bardziej otwarte na uwzględnianie RWE w zgłoszeniach regulacyjnych, zapewniając bardziej kompleksowy obraz korzyści i ryzyka związanego z produktem. - Wyniki Zgłaszane przez Pacjentów (PROs):
Włączenie PROs do badań klinicznych i zgłoszeń regulacyjnych staje się coraz ważniejsze. Środki te bezpośrednio odzwierciedlają doświadczenia pacjentów, dostarczając cennych informacji na temat objawów, jakości życia i satysfakcji z leczenia. - Wczesne Zaangażowanie i Doradztwo Naukowe:
Organy zdrowia zachęcają sponsorów do wczesnego zaangażowania w proces rozwoju, często włączając przedstawicieli pacjentów w te dyskusje. Ten wczesny dialog pomaga dostosować plany rozwoju do potrzeb pacjentów i oczekiwań regulacyjnych. - Udział pacjentów w ocenie korzyści i ryzyka:
Zarówno FDA, jak i EMA opracowały ramy, aby uwzględnić perspektywy pacjentów w ocenie korzyści i ryzyka, zapewniając, że decyzje regulacyjne odzwierciedlają to, co jest najważniejsze dla pacjentów.
Tabela: Kluczowe inicjatywy zorientowane na pacjenta głównych organów ds. zdrowia
| Organ ds. Zdrowia | Inicjatywa | Opis |
|---|---|---|
| FDA | Rozwój leków skoncentrowany na pacjencie (PFDD) | Systematyczne podejście do gromadzenia opinii pacjentów |
| EMA | Grupa Robocza ds. Pacjentów i Konsumentów (PCWP) | Forum dialogu z organizacjami pacjentów i konsumentów |
| MHRA | Zaangażowanie pacjentów i społeczeństwa | Strategia zaangażowania pacjentów w procesy regulacyjne |
| Health Canada | Kanadyjskie Ramy Współpracy w zakresie Leków i Produktów Zdrowotnych | Zwiększa zaangażowanie pacjentów w działania regulacyjne |
Rola Dostawców Usług Regulacyjnych:
W tym zmieniającym się otoczeniu rola specjalistów ds. Spraw regulacyjnych i partnerów stała się ważniejsza niż kiedykolwiek. Stanowią oni pomost między sponsorami, organami ds. zdrowia i pacjentami, zapewniając, że strategie regulacyjne są zgodne z podejściami skoncentrowanymi na pacjencie.
Kluczowe obowiązki obejmują:
- Opracowywanie strategii angażowania pacjentów
- Włączenie wkładu pacjentów do zgłoszeń regulacyjnych.
- Doradztwo w zakresie gromadzenia i prezentacji danych zorientowanych na pacjenta
- Ułatwianie wczesnego kontaktu z organami ds. zdrowia
- Bycie na bieżąco z ewoluującymi wymogami regulacyjnymi zorientowanymi na pacjenta
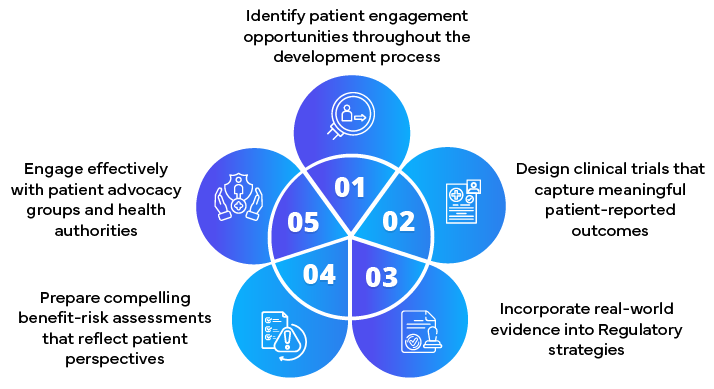
Rola partnerów regulacyjnych w realizacji zgłoszeń zorientowanych na pacjenta
Podsumowanie:
Przejście w kierunku podejścia skoncentrowanego na pacjencie w sprawach regulacyjnych stanowi znaczącą okazję do opracowywania i zatwierdzania produktów medycznych, które naprawdę odpowiadają potrzebom pacjentów. Przyjmując to podejście, sponsorzy mogą nie tylko skuteczniej poruszać się po ścieżkach regulacyjnych, ale także dostarczać produkty, które znacząco zmieniają życie pacjentów. W miarę jak organy ds. zdrowia nadal udoskonalają swoje podejścia skoncentrowane na pacjencie, wiedza dostawców usług regulacyjnych lub partnerów staje się bezcenna w zapewnianiu, że zgłoszenia nie tylko spełniają wymagania techniczne, ale także odpowiadają doświadczeniom i priorytetom pacjentów.
W tej nowej erze Spraw regulacyjnych, stawianie pacjentów na pierwszym miejscu to nie tylko dobra praktyka – to klucz do sukcesu.









